早教吧作业答案频道 -->化学-->
往100克含有盐酸和氯化钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算:(1)a→b段表示碳酸钠与混合溶液中的反应;(2)反
题目详情
往100克含有盐酸和氯化钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算:
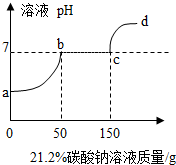
(1)a→b段表示碳酸钠与混合溶液中的___反应;
(2)反应到c点时,所得溶液的溶质质量分数是多少?(写出计算过程,精确到0.1%)


(1)a→b段表示碳酸钠与混合溶液中的___反应;
(2)反应到c点时,所得溶液的溶质质量分数是多少?(写出计算过程,精确到0.1%)

▼优质解答
答案和解析
(1)盐酸和氯化钙的混合溶液中,滴加稀盐酸,盐酸会先于碳酸钠,溶液的pH值升高,然后碳酸钠再与氯化钙反应,溶液的pH值不变,反应结束,溶液的pH值会继续的增大,所以a→b段表示碳酸钠与混合溶液中的稀盐酸反应;
(2)设盐酸和碳酸钠反应时,生成氯化钠质量为x,生成二氧化碳质量为y
2HCl+Na22CO33=2NaCl+H22O+CO22↑
106 117 44
21.2%×50g x y
=
=
x=11.7g
y=4.4g
碳酸钠和氯化钙反应生成氯化钠质量为m,生成碳酸钙沉淀质量为n
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100 117
21.2%×100g n m
=
=
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
×100%=15.6%.
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
106 21.2%×50g 106 106 10621.2%×50g 21.2%×50g 21.2%×50g=
=
x=11.7g
y=4.4g
碳酸钠和氯化钙反应生成氯化钠质量为m,生成碳酸钙沉淀质量为n
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100 117
21.2%×100g n m
=
=
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
×100%=15.6%.
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
117 x 117 117 117x x x=
x=11.7g
y=4.4g
碳酸钠和氯化钙反应生成氯化钠质量为m,生成碳酸钙沉淀质量为n
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100 117
21.2%×100g n m
=
=
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
×100%=15.6%.
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
44 y 44 44 44y y y
x=11.7g
y=4.4g
碳酸钠和氯化钙反应生成氯化钠质量为m,生成碳酸钙沉淀质量为n
CaCl22+Na22CO33=CaCO33↓+2NaCl
106 100 117
21.2%×100g n m
=
=
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
×100%=15.6%.
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
106 21.2%×100g 106 106 10621.2%×100g 21.2%×100g 21.2%×100g=
=
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
×100%=15.6%.
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
100 n 100 100 100n n n=
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
×100%=15.6%.
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
117 m 117 117 117m m m
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
×100%=15.6%.
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
23.4g+11.7g 100g+150g-20g-4.4g 23.4g+11.7g 23.4g+11.7g 23.4g+11.7g100g+150g-20g-4.4g 100g+150g-20g-4.4g 100g+150g-20g-4.4g×100%=15.6%.
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
(2)设盐酸和碳酸钠反应时,生成氯化钠质量为x,生成二氧化碳质量为y
2HCl+Na22CO33=2NaCl+H22O+CO22↑
106 117 44
21.2%×50g x y
| 106 |
| 21.2%×50g |
| 117 |
| x |
| 44 |
| y |
x=11.7g
y=4.4g
碳酸钠和氯化钙反应生成氯化钠质量为m,生成碳酸钙沉淀质量为n
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100 117
21.2%×100g n m
| 106 |
| 21.2%×100g |
| 100 |
| n |
| 117 |
| m |
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
| 23.4g+11.7g |
| 100g+150g-20g-4.4g |
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
| 106 |
| 21.2%×50g |
| 117 |
| x |
| 44 |
| y |
x=11.7g
y=4.4g
碳酸钠和氯化钙反应生成氯化钠质量为m,生成碳酸钙沉淀质量为n
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100 117
21.2%×100g n m
| 106 |
| 21.2%×100g |
| 100 |
| n |
| 117 |
| m |
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
| 23.4g+11.7g |
| 100g+150g-20g-4.4g |
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
| 117 |
| x |
| 44 |
| y |
x=11.7g
y=4.4g
碳酸钠和氯化钙反应生成氯化钠质量为m,生成碳酸钙沉淀质量为n
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100 117
21.2%×100g n m
| 106 |
| 21.2%×100g |
| 100 |
| n |
| 117 |
| m |
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
| 23.4g+11.7g |
| 100g+150g-20g-4.4g |
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
| 44 |
| y |
x=11.7g
y=4.4g
碳酸钠和氯化钙反应生成氯化钠质量为m,生成碳酸钙沉淀质量为n
CaCl22+Na22CO33=CaCO33↓+2NaCl
106 100 117
21.2%×100g n m
| 106 |
| 21.2%×100g |
| 100 |
| n |
| 117 |
| m |
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
| 23.4g+11.7g |
| 100g+150g-20g-4.4g |
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
| 106 |
| 21.2%×100g |
| 100 |
| n |
| 117 |
| m |
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
| 23.4g+11.7g |
| 100g+150g-20g-4.4g |
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
| 100 |
| n |
| 117 |
| m |
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
| 23.4g+11.7g |
| 100g+150g-20g-4.4g |
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
| 117 |
| m |
m=23.4g
n=20g
所以所得溶液的溶质质量分数是
| 23.4g+11.7g |
| 100g+150g-20g-4.4g |
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
| 23.4g+11.7g |
| 100g+150g-20g-4.4g |
故答案为:(1)稀盐酸;
(2)所得溶液的溶质质量分数是15.6%.
看了 往100克含有盐酸和氯化钙的...的网友还看了以下:
某保健品主要成分为碳酸钙,请计算下列问题:(要求写出计算过程)(1)碳酸钙化学式量是多少?(2)碳 2020-04-11 …
根据(KIO3)化学式计算:(1)计算碘酸钾的相对分子质量;(2)计算碘酸钾中各元素的质量比;(3 2020-05-14 …
某同学在实验室作酸碱中和反应实验.将稀硫酸滴入到8克10%的氢氧化钠溶液中至恰好完全反应,共消耗稀 2020-05-14 …
计算:已知硝酸铵的化学式为NH4NO3(4)多少克硝酸铵中含氮元素70克?(5)480克硝酸铵与多 2020-05-16 …
32克铜和一定量的浓硝酸反应计算?32克铜和一定量的浓硝酸反应,当铜完全溶解时,产生的气体再标准状 2020-05-16 …
把56.1克氯酸钾和高锰酸钾的混合物放入试管中充分加热至不再有气体生成为止,冷却后称的剩余固体物质 2020-06-14 …
取黄酮屑(铜锌合金)32.5克,放入盛有180克稀硫酸的容器中充分反应,生成氢气0.4克.试计算1 2020-06-25 …
求纯碱里碳酸钠的质量分数?取纯碱样品11克,全部溶解在100克水中,再加入氯化钙溶液141克,恰好 2020-07-18 …
溶解度计算1.已知硝酸钾在20°时的溶解度是222克/100克水.计算在20°时,将0.02克硝酸 2020-07-19 …
将碳酸钠和氯化钠固体混合物32.9克放入烧杯中,此时总质量为202.9克,加入326.9克稀盐酸, 2020-07-19 …