早教吧作业答案频道 -->化学-->
为探究测定中和热的实验,小明利用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液,在如图所示的装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热(中和热数值为57.3kJ/mo
题目详情
为探究测定中和热的实验,小明利用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液,在如图所示的装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热(中和热数值为57.3kJ/mol).
(1)写出实验所进行的中和反应的热化学方程式___.
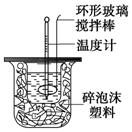
(2)实验装置中,烧杯间填满碎纸条的作用为___.
(3)该实验中,使用浓度略大于盐酸的NaOH溶液的原因是___,若改用60mL 0.50mol•L-1盐酸跟50mL 0.55mol•L-1,NaOH溶液进行反应,所求中和热的数值___(填“相等”或“不相等”),理由是___.
(4)小明利用上述装置做实验,测得中和热的数值偏低,请你分析可能的原因是___.
A.测量盐酸的温度后,温度计没有用水冲洗干净 B.做本实验的当天室温较高
C.将量筒中的NaOH(aq)倒入小烧杯时动作迟缓 D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大.为探究测定中和热的实验,小明利用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液,在如图所示的装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热(中和热数值为57.3kJ/mol).

(1)写出实验所进行的中和反应的热化学方程式___.
(2)实验装置中,烧杯间填满碎纸条的作用为___.
(3)该实验中,使用浓度略大于盐酸的NaOH溶液的原因是___,若改用60mL 0.50mol•L-1盐酸跟50mL 0.55mol•L-1,NaOH溶液进行反应,所求中和热的数值___(填“相等”或“不相等”),理由是___.
(4)小明利用上述装置做实验,测得中和热的数值偏低,请你分析可能的原因是___.
A.测量盐酸的温度后,温度计没有用水冲洗干净 B.做本实验的当天室温较高
C.将量筒中的NaOH(aq)倒入小烧杯时动作迟缓 D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大.-1-1

-1-1

(1)写出实验所进行的中和反应的热化学方程式___.
(2)实验装置中,烧杯间填满碎纸条的作用为___.
(3)该实验中,使用浓度略大于盐酸的NaOH溶液的原因是___,若改用60mL 0.50mol•L-1盐酸跟50mL 0.55mol•L-1,NaOH溶液进行反应,所求中和热的数值___(填“相等”或“不相等”),理由是___.
(4)小明利用上述装置做实验,测得中和热的数值偏低,请你分析可能的原因是___.
A.测量盐酸的温度后,温度计没有用水冲洗干净 B.做本实验的当天室温较高
C.将量筒中的NaOH(aq)倒入小烧杯时动作迟缓 D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大.为探究测定中和热的实验,小明利用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液,在如图所示的装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热(中和热数值为57.3kJ/mol).

(1)写出实验所进行的中和反应的热化学方程式___.
(2)实验装置中,烧杯间填满碎纸条的作用为___.
(3)该实验中,使用浓度略大于盐酸的NaOH溶液的原因是___,若改用60mL 0.50mol•L-1盐酸跟50mL 0.55mol•L-1,NaOH溶液进行反应,所求中和热的数值___(填“相等”或“不相等”),理由是___.
(4)小明利用上述装置做实验,测得中和热的数值偏低,请你分析可能的原因是___.
A.测量盐酸的温度后,温度计没有用水冲洗干净 B.做本实验的当天室温较高
C.将量筒中的NaOH(aq)倒入小烧杯时动作迟缓 D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大.-1-1

-1-1
▼优质解答
答案和解析
(1)稀的强酸与强碱溶液反应的中和热数值为57.3kJ/mol,则稀盐酸与稀NaOH溶液中和反应的热化学方程式:HCl (aq)+NaOH (aq)=H22O (l)+NaCl (aq)△H=-57.3kJ/mol;
故答案为:HCl (aq)+NaOH (aq)=H22O (l)+NaCl (aq)△H=-57.3kJ/mol;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是保温隔热、减少热量损失;
故答案为:保温隔热、减少热量损失;
(3)实验中,所用NaOH稍过量的原因是确保定量的HCl反应完全;反应放出的热量和所用酸以及碱的量的多少有关,用60mL 0.50mol•L-1-1盐酸跟50mL 0.55mol•L-1 -1 NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用60mL 0.50mol•L-1-1盐酸跟50mL 0.55mol•L-1 -1 NaOH溶液,测得中和热数值相等;
故答案为:确保定量的HCl反应完全;相等;因中和热是指稀强酸与稀强碱发生中和反应生成1 mol H22O放出的热量,与酸碱的用量无;
(4)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和,温度计示数变化值减小,导致实验测得中和热的数值偏小,故A正确;
B、做本实验的室温和反应热的数据之间无关,故B错误;
C、将量筒中的NaOH(aq)倒入小烧杯时动作迟缓,会导致一部分能量的散失,导致实验测得中和热的数值偏小,故C正确;
D、在量取盐酸时仰视读数,会使得实际量取体积高于所要量的体积,算过量,可以保证碱全反应,导致实验测得中和热的数值偏高,故D错误;
E、大烧杯的盖板中间小孔太大,会导致一部分能量散失,所以测的数值降低,故E正确.
故答案为:A C E.
故答案为:HCl (aq)+NaOH (aq)=H22O (l)+NaCl (aq)△H=-57.3kJ/mol;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是保温隔热、减少热量损失;
故答案为:保温隔热、减少热量损失;
(3)实验中,所用NaOH稍过量的原因是确保定量的HCl反应完全;反应放出的热量和所用酸以及碱的量的多少有关,用60mL 0.50mol•L-1-1盐酸跟50mL 0.55mol•L-1 -1 NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用60mL 0.50mol•L-1-1盐酸跟50mL 0.55mol•L-1 -1 NaOH溶液,测得中和热数值相等;
故答案为:确保定量的HCl反应完全;相等;因中和热是指稀强酸与稀强碱发生中和反应生成1 mol H22O放出的热量,与酸碱的用量无;
(4)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和,温度计示数变化值减小,导致实验测得中和热的数值偏小,故A正确;
B、做本实验的室温和反应热的数据之间无关,故B错误;
C、将量筒中的NaOH(aq)倒入小烧杯时动作迟缓,会导致一部分能量的散失,导致实验测得中和热的数值偏小,故C正确;
D、在量取盐酸时仰视读数,会使得实际量取体积高于所要量的体积,算过量,可以保证碱全反应,导致实验测得中和热的数值偏高,故D错误;
E、大烧杯的盖板中间小孔太大,会导致一部分能量散失,所以测的数值降低,故E正确.
故答案为:A C E.
看了 为探究测定中和热的实验,小明...的网友还看了以下:
将木炭和铜绿[Cu2(OH)2CO3]按一定比例混合,在密闭容器中加强热,该变化过程中发生的有关化 2020-05-13 …
某一分解反应,当反应物浓度为0.20mol.L-1时反应速率为0.30mol.L-1.s-1.若该 2020-05-14 …
以下有关牛鞭效应论述错误的有?A:牛鞭效应发生于信息流从原始供应商向最终客户端传递的过程中B:牛鞭 2020-05-16 …
∵EM是⊙O的切线,怎么推出EB•EC=EM2①?,看题后回答.(2005•温州)如图,已知四边形 2020-05-21 …
法拉第电磁感应:感应电动势怎样以图形的方法显示出来?闭合的线圈由于磁通量的变化产生感应电动势,但是 2020-06-05 …
化学反应的反应平衡在物理化学的热力学的解释中是说吉布斯函数变等于0;而在动力学中说是反应的正反应的 2020-06-06 …
学校的走廊、消防通道内都应安装应急灯(如图甲所示).外接电源断电时,应急灯自动点亮,此时由蓄电池供 2020-06-15 …
解方程.|x-1|+|x+2|=5由绝对值的几何意义知,该方程表示求在数轴上与1和-2的距离之和为 2020-06-29 …
应激反应与非条件反射我做到一题:“人在寒冷环境中的即时反应之一是皮肤起鸡皮疙瘩.该反应属于:A神经 2020-07-03 …
某反应在反应过程中的能量变化如图所示(图中E1表示反应物总能量E2表示生成物总能量)。下列有关叙述正 2020-10-31 …