用50mL0.50mol/L的盐酸与50mL0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:(1)烧杯间填满碎泡沫塑料
用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题: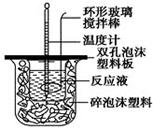
(1)烧杯间填满碎泡沫塑料的作用是___________________________
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替?_____(填“能”或“不能”),
其原因是_______________________________________________________。
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是______________________。
实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量_______ _____(填“相等”“不相等”),若实验操作均正确,则所求中和热________________(填“相等”“不相等”)。
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H 2 O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:__________________________________。
用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)烧杯间填满碎泡沫塑料的作用是___________________________
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替?_____(填“能”或“不能”),
其原因是_______________________________________________________。
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是______________________。
实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量_______ _____(填“相等”“不相等”),若实验操作均正确,则所求中和热________________(填“相等”“不相等”)。
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H 2 O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:__________________________________。
用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)烧杯间填满碎泡沫塑料的作用是___________________________
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替?_____(填“能”或“不能”),
其原因是_______________________________________________________。
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是______________________。
实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量_______ _____(填“相等”“不相等”),若实验操作均正确,则所求中和热________________(填“相等”“不相等”)。
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H 2 O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:__________________________________。

2
(1)减少热量损失
(2)不能 ①铁会和盐酸反应 ②铁导热性好,热量损失较大
(3)为了确保盐酸完全被中和 不相等 相等
(4)NaOH(aq)+HCl(aq)= NaCl(aq)+H 2 O(l) △H="-57.3kJ/mol"
解析
分 析:
(1)烧杯间填满碎泡沫塑料的作用是减少热量损失;
(2)环形铁质搅拌棒一是能导热,产生热损失,二是可以与盐酸反应,放热且减少HCl的量,故不能用环形铁质搅拌棒代替环形玻璃搅拌棒;
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是为了确保盐酸完全被中和。实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应,与上述实验相比,实验反应的物的量增大,所放出的热量最多;但中和热是定值,若实验操作均正确,中和热不会变化。
(4)因为在稀溶液中,强酸和强碱发生中和反应生成1 mol H 2 O时,放出57.3 kJ的热量,所以上述反应的热化学方程式为:NaOH(aq)+HCl(aq)= NaCl(aq)+H 2 O(l) △H=-57.3kJ/mol。
考点:
中和热实验的测定原理及评价。
(1)减少热量损失
(2)不能 ①铁会和盐酸反应 ②铁导热性好,热量损失较大
(3)为了确保盐酸完全被中和 不相等 相等
(4)NaOH(aq)+HCl(aq)= NaCl(aq)+H 2 O(l) △H="-57.3kJ/mol"
(2)不能 ①铁会和盐酸反应 ②铁导热性好,热量损失较大
(3)为了确保盐酸完全被中和 不相等 相等
(4)NaOH(aq)+HCl(aq)= NaCl(aq)+H 2 O(l) △H="-57.3kJ/mol" (1)减少热量损失
(2)不能 ①铁会和盐酸反应 ②铁导热性好,热量损失较大
(3)为了确保盐酸完全被中和 不相等 相等
(4)NaOH(aq)+HCl(aq)= NaCl(aq)+H 2 2 O(l) △H="-57.3kJ/mol"
解析
分 析:
(1)烧杯间填满碎泡沫塑料的作用是减少热量损失;
(2)环形铁质搅拌棒一是能导热,产生热损失,二是可以与盐酸反应,放热且减少HCl的量,故不能用环形铁质搅拌棒代替环形玻璃搅拌棒;
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是为了确保盐酸完全被中和。实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应,与上述实验相比,实验反应的物的量增大,所放出的热量最多;但中和热是定值,若实验操作均正确,中和热不会变化。
(4)因为在稀溶液中,强酸和强碱发生中和反应生成1 mol H 2 O时,放出57.3 kJ的热量,所以上述反应的热化学方程式为:NaOH(aq)+HCl(aq)= NaCl(aq)+H 2 O(l) △H=-57.3kJ/mol。
考点:
中和热实验的测定原理及评价。
分 析:
(1)烧杯间填满碎泡沫塑料的作用是减少热量损失;
(2)环形铁质搅拌棒一是能导热,产生热损失,二是可以与盐酸反应,放热且减少HCl的量,故不能用环形铁质搅拌棒代替环形玻璃搅拌棒;
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是为了确保盐酸完全被中和。实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应,与上述实验相比,实验反应的物的量增大,所放出的热量最多;但中和热是定值,若实验操作均正确,中和热不会变化。
(4)因为在稀溶液中,强酸和强碱发生中和反应生成1 mol H 2 O时,放出57.3 kJ的热量,所以上述反应的热化学方程式为:NaOH(aq)+HCl(aq)= NaCl(aq)+H 2 O(l) △H=-57.3kJ/mol。
考点:
中和热实验的测定原理及评价。
分 析:
(1)烧杯间填满碎泡沫塑料的作用是减少热量损失;
(2)环形铁质搅拌棒一是能导热,产生热损失,二是可以与盐酸反应,放热且减少HCl的量,故不能用环形铁质搅拌棒代替环形玻璃搅拌棒;
(3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是为了确保盐酸完全被中和。实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应,与上述实验相比,实验反应的物的量增大,所放出的热量最多;但中和热是定值,若实验操作均正确,中和热不会变化。
(4)因为在稀溶液中,强酸和强碱发生中和反应生成1 mol H 2 2 O时,放出57.3 kJ的热量,所以上述反应的热化学方程式为:NaOH(aq)+HCl(aq)= NaCl(aq)+H 2 2 O(l) △H=-57.3kJ/mol。
考点:
中和热实验的测定原理及评价。
泥石流是由什么原因引起的?山上不是都是石块什么的吗?泥石流是像洪水一样的冲下来的,就和搅碎过的石块一 2020-03-30 …
英语翻译把破碎、除石、细碎过的原料(已经过晒矿并加纯碱),用装载车运到料斗.由于需要把钙性土加工成 2020-04-26 …
人体食物消化经过的路线 有什么作用 2020-05-16 …
固体石蜡的粉碎过程中加入dryice,此粉碎过程属于()A.混合粉碎B.开路粉碎C.低温粉碎D.湿法 2020-05-31 …
小明用毛皮摩擦过的橡胶棒靠近碎纸屑,发现碎纸屑被吸引,但过一会儿发现碎纸屑又掉下来,为什么? 2020-06-15 …
请教水葫芦的一些问题和生态养殖水葫芦净化水质,吸收河里的重金属后,它的叶子还能拿去喂养吗?根部什么 2020-06-21 …
宁夏红枸杞果酒是经科学生物提炼而成,含有丰富的多糖、维生素和20多种人体必需的常量元素及微量元素, 2020-06-27 …
如图甲所示,小董同学用此装置探究冰熔化过程中温度的变化情况.(1)装有碎冰的烧杯直接放置在空气中, 2020-06-27 …
碎松香熔化成形的问题我想把一块被弄碎的乐器松香加热熔化并重新定型,请问是应该一次熔化成型(有技术难度 2020-11-28 …
谁可以告诉我初三化学上半学期学过的所有的化学方程式,急用的,包括钙系的,置换反应零零碎碎的等的全都要 2020-12-27 …