科学家在-100℃合成了化合物X(分子模型如图,其中代表碳原子,代表氢原子).下列说法正确的是()A.X是有机高分子化合物B.X中碳元素的质量分数为93.75%C.X中氢原子与碳原子的个
科学家在-100℃合成了化合物X(分子模型如图,其中 代表碳原子,
代表碳原子, 代表氢原子).下列说法正确的是( )
代表氢原子).下列说法正确的是( )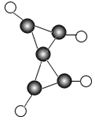
A. X是有机高分子化合物
B. X中碳元素的质量分数为93.75%
C. X中氢原子与碳原子的个数比为5:4
D. 等质量的X与甲烷完全燃烧,X消耗的氧气多
科学家在-100℃合成了化合物X(分子模型如图,其中 代表碳原子,
代表碳原子, 代表氢原子).下列说法正确的是( )
代表氢原子).下列说法正确的是( )
 代表碳原子,
代表碳原子, 代表氢原子).下列说法正确的是( )
代表氢原子).下列说法正确的是( )

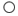

A. X是有机高分子化合物
B. X中碳元素的质量分数为93.75%
C. X中氢原子与碳原子的个数比为5:4
D. 等质量的X与甲烷完全燃烧,X消耗的氧气多
A.该物质的相对分子质量=12×5+4=64,而有机高分子化合物的相对分子质量大到几万甚至几十万,所以该物质不属于有机高分子化合物,故错误;
B.物质中碳元素的质量分数=
| 12×5 |
| 12×5+1×4 |
C.该物质的分子中含有设有5个碳原子,4个氢原子,即X中氢原子与碳原子的个数比为4:5,故错误;
D.要解答这个问题,可根据方程式中两种物质与氧气的质量比求解,化学方程式如下:
CH4+2O2
| ||
16 64
C5H4 +6O2
| ||
64 192
甲烷燃烧的化学反应中甲烷与氧气的质量比是16:64=1:4,C5H4燃烧的反应中C5H4与氧气的质量比是64:192=1:3,相当于每1克的两种物质燃烧,甲烷消耗氧气的质量是4克、该化合物消耗氧气的质量是3克,显然等质量的该物质与甲烷相比,燃烧时消耗的氧气少,故错误.
故选B.
| 12×5 |
| 12×5+1×4 |
C.该物质的分子中含有设有5个碳原子,4个氢原子,即X中氢原子与碳原子的个数比为4:5,故错误;
D.要解答这个问题,可根据方程式中两种物质与氧气的质量比求解,化学方程式如下:
CH44+2O22
| ||
16 64
C5H4 +6O2
| ||
64 192
甲烷燃烧的化学反应中甲烷与氧气的质量比是16:64=1:4,C5H4燃烧的反应中C5H4与氧气的质量比是64:192=1:3,相当于每1克的两种物质燃烧,甲烷消耗氧气的质量是4克、该化合物消耗氧气的质量是3克,显然等质量的该物质与甲烷相比,燃烧时消耗的氧气少,故错误.
故选B.
| ||
| 点燃 |
. |
| 点燃 |
. |
| 点燃 |
. |
| 点燃 |
. |
16 64
C55H4 4 +6O22
| ||
64 192
甲烷燃烧的化学反应中甲烷与氧气的质量比是16:64=1:4,C5H4燃烧的反应中C5H4与氧气的质量比是64:192=1:3,相当于每1克的两种物质燃烧,甲烷消耗氧气的质量是4克、该化合物消耗氧气的质量是3克,显然等质量的该物质与甲烷相比,燃烧时消耗的氧气少,故错误.
故选B.
| ||
| 点燃 |
. |
| 点燃 |
. |
| 点燃 |
. |
| 点燃 |
. |
64 192
甲烷燃烧的化学反应中甲烷与氧气的质量比是16:64=1:4,C55H44燃烧的反应中C55H44与氧气的质量比是64:192=1:3,相当于每1克的两种物质燃烧,甲烷消耗氧气的质量是4克、该化合物消耗氧气的质量是3克,显然等质量的该物质与甲烷相比,燃烧时消耗的氧气少,故错误.
故选B.
英语翻译世界科技百年1900年,普朗克提出了量子论.后经爱因斯坦于1905年提出光量子概念、玻尔于 2020-04-27 …
细胞代谢是指[]A.细胞内的同化作用B.细胞内的能量代谢C.细胞内的异化作用D.细胞内全部有序的化 2020-05-14 …
在决定鲸的捕捞量时.需研究如图.该图表示了生殖数量、死亡数量与种群大小的关系.图中哪条线表示生殖的 2020-05-14 …
无氧呼吸与有氧呼吸释放二氧化碳的总量代表有机物的消耗量为什么错? 2020-05-14 …
为了子孙后代,你们要献出全部的力量和情感来保护大地意思为了子孙后代,你们要献出全部的力量和情感来保 2020-06-04 …
用3种试剂探究甲、乙、丙三种植物种子的成分,颜色反应结果如表.下列有关说法中错误的是(“+”的数量 2020-06-10 …
用3种试剂探究甲、乙、丙三种植物种子的成分,颜色反应结果如表.下列有关说法中错误的是(“+”的数量 2020-06-10 …
又遇到一个解方程的问题,好多地方无从下手,编写一个函数quadzero01.m,其输出输入的格式如 2020-06-13 …
x+yy'=x(x^2+y^2)用适当的变量代换求解方程的解 2020-06-14 …
零乘以负无穷大也等于任何数吗?0×(±∞)=a-->a÷0=±∞-->a÷(±∞)=0.除数就是0 2020-06-14 …