早教吧作业答案频道 -->化学-->
25℃时,三种酸的电离平衡常数如表所示.化学式CH3COOHHClOH3PO3名称醋酸次氯酸亚磷酸电离平衡常数(25℃)1.8×10-53.0×10-8K1=8.3×10-3K2=5.6×10-6
题目详情
25℃时,三种酸的电离平衡常数如表所示.
回答下列问题:
(1)亚磷酸(H3PO3) 为二元中强酸,具有较强的还原性,可将银离子还原成银单质,在空气可缓慢氧化成H3PO4.H3PO3的电离方程式为___.
(2)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.NaClO c.NaHPO3
它们的pH由小到大排列顺序是___(用字母表示).
(3)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是___(填字母).
A.c(H+) B.
C.c(H+)•c(OH-) D.
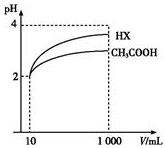
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“等于”或“小于”)醋酸的平衡常数.25℃时,三种酸的电离平衡常数如表所示.
回答下列问题:

(1)亚磷酸(H3PO3) 为二元中强酸,具有较强的还原性,可将银离子还原成银单质,在空气可缓慢氧化成H3PO4.H3PO3的电离方程式为___.
(2)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.NaClO c.NaHPO3
它们的pH由小到大排列顺序是___(用字母表示).
(3)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是___(填字母).
A.c(H+) B.
C.c(H+)•c(OH-) D.
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“等于”或“小于”)醋酸的平衡常数.
化学式 CH3COOH HClO H3PO3 名称 醋酸 次氯酸 亚磷酸 电离平衡常数(25℃) 1.8×10-5 3.0×10-8 K1=8.3×10-3
K2=5.6×10-6 化学式 CH3COOH HClO H3PO3 化学式 CH3COOH 3HClO H3PO3 33 名称 醋酸 次氯酸 亚磷酸 名称 醋酸 次氯酸 亚磷酸 电离平衡常数(25℃) 1.8×10-5 3.0×10-8 K1=8.3×10-3
K2=5.6×10-6 电离平衡常数(25℃) 1.8×10-5 -53.0×10-8 -8K1=8.3×10-3
K2=5.6×10-6 1-3
2-6

333433
-133
-13
+
C.c(H+)•c(OH-) D.
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“等于”或“小于”)醋酸的平衡常数.
c(H+) c(CH3COOH) c(H+) c(H+) H+)H+)+) c(CH3COOH) c(CH3COOH) H3COOH)H3COOH)3COOH)+-
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“等于”或“小于”)醋酸的平衡常数.
c(OH-) c(H+) c(OH-) c(OH-) H-)H-)-) c(H+) c(H+) H+)H+)+)
| 化学式 | CH3COOH | HClO | H3PO3 |
| 名称 | 醋酸 | 次氯酸 | 亚磷酸 |
| 电离平衡常数(25℃) | 1.8×10-5 | 3.0×10-8 | K1=8.3×10-3 K2=5.6×10-6 |

(1)亚磷酸(H3PO3) 为二元中强酸,具有较强的还原性,可将银离子还原成银单质,在空气可缓慢氧化成H3PO4.H3PO3的电离方程式为___.
(2)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.NaClO c.NaHPO3
它们的pH由小到大排列顺序是___(用字母表示).
(3)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是___(填字母).
A.c(H+) B.
| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“等于”或“小于”)醋酸的平衡常数.25℃时,三种酸的电离平衡常数如表所示.
| 化学式 | CH3COOH | HClO | H3PO3 |
| 名称 | 醋酸 | 次氯酸 | 亚磷酸 |
| 电离平衡常数(25℃) | 1.8×10-5 | 3.0×10-8 | K1=8.3×10-3 K2=5.6×10-6 |

(1)亚磷酸(H3PO3) 为二元中强酸,具有较强的还原性,可将银离子还原成银单质,在空气可缓慢氧化成H3PO4.H3PO3的电离方程式为___.
(2)物质的量浓度均为0.1mol•L-1的三种溶液:a.CH3COONa b.NaClO c.NaHPO3
它们的pH由小到大排列顺序是___(用字母表示).
(3)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是___(填字母).
A.c(H+) B.
| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“等于”或“小于”)醋酸的平衡常数.
| 化学式 | CH3COOH | HClO | H3PO3 |
| 名称 | 醋酸 | 次氯酸 | 亚磷酸 |
| 电离平衡常数(25℃) | 1.8×10-5 | 3.0×10-8 | K1=8.3×10-3 K2=5.6×10-6 |
K2=5.6×10-6
K2=5.6×10-6
K2=5.6×10-6
2-6

333433
-133
-13
+
| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“等于”或“小于”)醋酸的平衡常数.
| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
(4)体积为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“等于”或“小于”)醋酸的平衡常数.
| c(OH-) |
| c(H+) |
▼优质解答
答案和解析
(1)亚磷酸(H3PO3) 为二元中强酸,分步电离且电离可逆,电离方程式为H3PO3⇌H2PO3-+H+ (H2PO3-⇌HPO32-+H+),故答案为:H3PO3⇌H2PO3-+H+ (H2PO3-⇌HPO32-+H+);(2)据电离平衡常数可知,三...
看了 25℃时,三种酸的电离平衡常...的网友还看了以下:
s=(a+b)h/2变成h的公式梯形的面积公式S=(a+b)h/2,其中s表示梯形面积,a表示梯形 2020-05-13 …
将梯形的面积公式S=(a+b)h/2形成已知S,a,b,h的形式,若a:b:s=2:3:4,求h的 2020-05-13 …
氨基酸通式中的H是什么除了R基,羧基,氨基,剩下一个H是什么 2020-05-17 …
当C、H、O、BR等元素的原子量均取整数时,为什么能推出烃及烃的含氧衍生物的式量均为偶数为什么得不 2020-05-21 …
醇酸酯化时,是醇去OH酸去H,还是是醇去H酸去OH 2020-05-22 …
28km/h=S/[=(2/3S)/V1+(1/3S)/20km/h]这个式子怎么解?怎么化简以至 2020-06-03 …
树苗高度用h表示,生长年数用a表示(树苗原高是100cm)a=1,h=100+5,a=2,h=10 2020-06-05 …
下列关于柠檬酸循环的叙述,正确的是()A.全过程在线粒体基质中进行B.不消耗氧气,但有CO2产生C 2020-07-02 …
氨基酸通式可以这样写么为什么R|H2N——C——COOH|H就是这种形式的可以是H2N这种形式么如果 2020-12-05 …
H+酸根离子可以构成无氧酸,念氢某酸,在HCl(离子化合物)是不是H++Cl-就构成了HCl(氢氯酸 2021-01-27 …