早教吧作业答案频道 -->化学-->
氧化铁是重要的工艺颜料,用废铁屑制备它的流程如下:回答下列问题:(1)①加碳酸钠溶液并小火加热的操作目的是;②操作Ⅰ的名称是,操作Ⅱ的名称是;(2)①流程所发生的
题目详情
氧化铁是重要的工艺颜料,用废铁屑制备它的流程如下:回答下列问题:
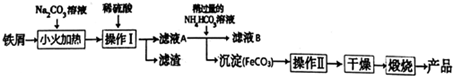
(1)①加碳酸钠溶液并小火加热的操作目的是___;
②操作Ⅰ的名称是___,操作Ⅱ的名称是___;
(2)①流程所发生的反应为FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O过程中,加入稍过量的NH4HCO3溶液后,且要控制溶液的为6.8~7.2之间.加入稍过量的目的是___,溶液的pH不能过低的原因是___.
②检验滤液B中含有NH4+的方法是___.
(3)有些同学认为KMnO4溶液滴定能进行铁元素含量的测定.
a、称取2.85g绿矾(FeSO4•7H2O)产品,配成250mL溶液;
b、量取25.00mL待测溶液于锥形瓶中;
c、用硫酸化的0.0100mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①写出酸性KMnO4溶液与FeSO4溶液反应的离子方程式___.
②用KMnO4标准溶液滴定时应选用___滴定管(填“酸式”或“碱式”).
③计算上述样品中FeSO4•7H2O的质量分数为___[已知M(FeSO4•7H2O)=278g/mol].

(1)①加碳酸钠溶液并小火加热的操作目的是___;
②操作Ⅰ的名称是___,操作Ⅱ的名称是___;
(2)①流程所发生的反应为FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O过程中,加入稍过量的NH4HCO3溶液后,且要控制溶液的为6.8~7.2之间.加入稍过量的目的是___,溶液的pH不能过低的原因是___.
②检验滤液B中含有NH4+的方法是___.
(3)有些同学认为KMnO4溶液滴定能进行铁元素含量的测定.
a、称取2.85g绿矾(FeSO4•7H2O)产品,配成250mL溶液;
b、量取25.00mL待测溶液于锥形瓶中;
c、用硫酸化的0.0100mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①写出酸性KMnO4溶液与FeSO4溶液反应的离子方程式___.
②用KMnO4标准溶液滴定时应选用___滴定管(填“酸式”或“碱式”).
③计算上述样品中FeSO4•7H2O的质量分数为___[已知M(FeSO4•7H2O)=278g/mol].
▼优质解答
答案和解析
碳酸钠溶液显碱性,可以除去铁屑表面的油污,用稀硫酸溶解铁,再通过过滤分离得到滤液A,滤液A中加入碳酸氢铵,将溶液中亚铁离子转化为FeCO3沉淀,再通过过滤分离滤液B与FeCO3,滤液B中含有硫酸铵,FeCO3表面附着杂质,在干燥前应先洗涤除去杂质,在空气中煅烧分解,且+2价铁在空气中加热易被氧化为+3价,最终得到Fe2O3.
(1)①碳酸钠溶液显碱性,促进酯的水解,可以除去铁屑表面的油污,故答案为:去除油污;
②操作I分离互不相溶的固体与液体,采取过滤;碳酸亚铁表面附着杂质,沉淀干燥前应先洗涤除去杂质,故答案为:过滤;洗涤;
(2)①加入少过量的碳酸氢铵,使溶液中亚铁离子完全转化为FeCO3沉淀;pH过低,碳酸氢铵能与酸反应,碳酸亚铁沉淀减少,
故答案为:使溶液中亚铁离子完全转化为FeCO3沉淀;碳酸氢铵能与酸反应,碳酸亚铁沉淀减少;
②检验铵根离子的实验方法为:取少许B溶液于试管中,加入足量浓氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明滤液B中含有铵根离子,
故答案为:取少许B溶液于试管中,加入足量浓氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明滤液B中含有铵根离子;
(3)①高锰酸根具有强氧化性,亚铁离子具有还原性,酸性条件下,高锰酸根将亚铁离子氧化为铁离子,自身被还原为锰离子,同时有水生成,反应离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,
故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
②高锰酸钾溶液具有强氧化性,可以腐蚀橡皮管,且为硫酸酸化,应盛放在酸式滴定管中,故答案为:酸式;
③25mL样品溶液消耗高锰酸钾的物质的量为0.02L×0.0100mol/L=2×10-4mol,可知250mL溶液可以消耗高锰酸钾的物质的量为2×10-4mol×
=2×10-3mol,由5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,可知250mL溶液中亚铁离子离子的物质的量为2×10-3mol×5=0.01mol,由Fe元素守恒可得FeSO4•7H2O的物质的量为0.01mol,故FeSO4•7H2O的质量分数为
×100%=97.54%,
故答案为:97.54%.
(1)①碳酸钠溶液显碱性,促进酯的水解,可以除去铁屑表面的油污,故答案为:去除油污;
②操作I分离互不相溶的固体与液体,采取过滤;碳酸亚铁表面附着杂质,沉淀干燥前应先洗涤除去杂质,故答案为:过滤;洗涤;
(2)①加入少过量的碳酸氢铵,使溶液中亚铁离子完全转化为FeCO3沉淀;pH过低,碳酸氢铵能与酸反应,碳酸亚铁沉淀减少,
故答案为:使溶液中亚铁离子完全转化为FeCO3沉淀;碳酸氢铵能与酸反应,碳酸亚铁沉淀减少;
②检验铵根离子的实验方法为:取少许B溶液于试管中,加入足量浓氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明滤液B中含有铵根离子,
故答案为:取少许B溶液于试管中,加入足量浓氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明滤液B中含有铵根离子;
(3)①高锰酸根具有强氧化性,亚铁离子具有还原性,酸性条件下,高锰酸根将亚铁离子氧化为铁离子,自身被还原为锰离子,同时有水生成,反应离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,
故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
②高锰酸钾溶液具有强氧化性,可以腐蚀橡皮管,且为硫酸酸化,应盛放在酸式滴定管中,故答案为:酸式;
③25mL样品溶液消耗高锰酸钾的物质的量为0.02L×0.0100mol/L=2×10-4mol,可知250mL溶液可以消耗高锰酸钾的物质的量为2×10-4mol×
| 250mL |
| 25mL |
| 0.01mol×278g/mol |
| 2.85g |
故答案为:97.54%.
看了 氧化铁是重要的工艺颜料,用废...的网友还看了以下:
下列说法正确的是()A.实验室制取乙烯时浓硫酸是催化剂和吸水剂B.硝基苯制备时浓硫酸作催化剂和脱水 2020-04-08 …
关于阿司匹林合成的思考题帮我回答一下1.阿司匹林的制备取6250px3干燥锥形瓶一只,先后加入2. 2020-05-16 …
有关中断的论述不正确的是()。A.CPU及I/O设备可实现并行工作,但设备不可并行工作B.可以实现多 2020-05-24 …
有关中断的论述不正确的是( )。A.CPU及I/O设备可实现并行工作,但设备主动申请前不可并行工作B 2020-05-24 …
实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO 2020-06-10 …
1.氢氧化钙、碳酸钙、碳酸氢钠等常用于制作抗酸药,它们必须具备两个条件:一是能与胃酸作用;二是(2 2020-07-06 …
甲酸铜[Cu(HCOO)2∙4H2O]是一种重要的化工原料,可以用碱式碳酸铜与甲酸作用来制备。实验 2020-07-24 …
某系统由甲乙两人监控,甲的操作可靠度为0.9,乙为0.8,机械设备的可靠度为0.95,当两人并联工作 2020-11-03 …
实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2 2020-11-28 …
实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2 2021-02-01 …