早教吧作业答案频道 -->化学-->
第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减少温室气体排放量.Ⅰ.CO2加氢合成甲醇是合理利用CO2的有效途径.由CO2制备甲醇过程可能涉及反应如下:反应①:CO2(g
题目详情
第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减少温室气体排放量.
Ⅰ.CO2加氢合成甲醇是合理利用 CO2的有效途径.由 CO2制备甲醇过程可能涉及反应如下:
反应①:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-49.58kJ•mol-1
反应②:CO2(g)+H2(g)⇌CO (g)+H2O(g)△H2
反应③:CO(g)+2H2(g)⇌CH3OH(g)△H3=-90.77kJ•mol-1,回答下列问题:
(1)反应②的△H2=___,反应 ①自发进行条件是___(填“较低温”、“较高温”或“任何温度”).
(2)某温度下,在体积为2L的恒容密闭容器中,按如下方式加入反应物,仅发生反应①.一段时间后达到平衡.
测得甲中CO2和CH3OH(g)的浓度随时间变化如图所示.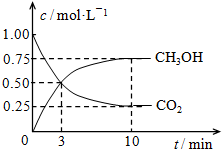
①前3min内,平均反应速率v(H2)=___mol•L-1•min-1.此温度下该反应的平衡常数为
___(结果保留两位小数).
②下列措施中,既能使反应速率加快,又能使n(CH3OH)/n(CO2)增大是___.
A.升高温度 B.充入惰性气体 C.将H2O(g)从体系中分离
D.再充入1mol H2 E.再充入1mol CO2 F.加入催化剂
③反应达到平衡后,若向反应体系再加入CO2(g)、H2(g)、CH3OH(g)、H2O(g)各1mol,化学平衡___(填“正向”、“逆向”或“不”)移动.
④要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为___.
Ⅱ.工业上可用CO2与NH3合成制尿素的原料氨基甲酸铵(H2NCOONH4).氨基甲酸铵极易发生:H2NCOONH4+2H2O⇌NH4HCO3+NH3•H2O,该反应酸性条件下更彻底.25℃,向l L 0.1mol•L-1的盐酸中逐渐加入氨基甲酸铵粉末至溶液呈中性(忽略溶液体积变化),共用去0.052mol氨基甲酸铵.若此时溶液中几乎不含碳元素,则该溶液中 c(NH4+)=___,NH4+水解常数Kh=___.
Ⅰ.CO2加氢合成甲醇是合理利用 CO2的有效途径.由 CO2制备甲醇过程可能涉及反应如下:
反应①:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-49.58kJ•mol-1
反应②:CO2(g)+H2(g)⇌CO (g)+H2O(g)△H2
反应③:CO(g)+2H2(g)⇌CH3OH(g)△H3=-90.77kJ•mol-1,回答下列问题:
(1)反应②的△H2=___,反应 ①自发进行条件是___(填“较低温”、“较高温”或“任何温度”).
(2)某温度下,在体积为2L的恒容密闭容器中,按如下方式加入反应物,仅发生反应①.一段时间后达到平衡.
| 容器 | 甲 | 乙 |
| 反应物投入量 | 2mol CO2、6mol H2 | a mol CO2、b mol H2 c mol CH3OH(g)、c mol H2O(g) |

①前3min内,平均反应速率v(H2)=___mol•L-1•min-1.此温度下该反应的平衡常数为
___(结果保留两位小数).
②下列措施中,既能使反应速率加快,又能使n(CH3OH)/n(CO2)增大是___.
A.升高温度 B.充入惰性气体 C.将H2O(g)从体系中分离
D.再充入1mol H2 E.再充入1mol CO2 F.加入催化剂
③反应达到平衡后,若向反应体系再加入CO2(g)、H2(g)、CH3OH(g)、H2O(g)各1mol,化学平衡___(填“正向”、“逆向”或“不”)移动.
④要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为___.
Ⅱ.工业上可用CO2与NH3合成制尿素的原料氨基甲酸铵(H2NCOONH4).氨基甲酸铵极易发生:H2NCOONH4+2H2O⇌NH4HCO3+NH3•H2O,该反应酸性条件下更彻底.25℃,向l L 0.1mol•L-1的盐酸中逐渐加入氨基甲酸铵粉末至溶液呈中性(忽略溶液体积变化),共用去0.052mol氨基甲酸铵.若此时溶液中几乎不含碳元素,则该溶液中 c(NH4+)=___,NH4+水解常数Kh=___.
▼优质解答
答案和解析
(1)反应Ⅰ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=-49.58kJ•mol-1
反应Ⅱ:CO2(g)+H2(g)⇌CO (g)+H2O(g)△H2
反应Ⅲ:CO(g)+2H2(g)⇌CH3OH(g)△H3=-90.77kJ•mol-1
根据盖斯定律,反应Ⅱ可以是Ⅰ-Ⅲ得到,所以反应Ⅱ的焓变△H2=(-49.58kJ•mol-1)-(-90.77kJ•mol-1)=+41.19 kJ•mol-1;根据反应自发行的判据:△H-T△S<0,反应Ⅲ是熵减的放热的反应,所以要自发进行需要在较低温下进行,
故答案为:+41.19 kJ•mol-1;较低温;
(2)①前3min内,平均反应速率v(CO2)=
mol/(L.min)=
mol/(L.min);
平均反应速率v(H2)=3v(CO2)=
mol/(L.min)×3=0.5mol/(Lmin);
平衡时,c(CO2)=0.25mol/L、c(CH3OH)=c(H2O)=0.75mol/L、c(H2)=3mol/L-0.75mol/L×3=0.75mol/L,
化学平衡常数K=
=
=5.33,
故答案为:0.5;5.33;
②A.升高温度增大反应速率,但平衡逆向移动,则n(CH3OH)/n(CO2)减小,故错误;
B.充入惰性气体,反应物和生成物浓度不变,平衡不移动,n(CH3OH)/n(CO2)不变,反应速率不变,故错误;
C.将H2O(g)从体系中分离,平衡正向移动,但反应速率减小,故错误;
D.再充入1mol H2 ,平衡正向移动,二氧化碳的物质的量减小、甲醇的物质的量增大,反应速率增大且n(CH3OH)/n(CO2)增大,故正确;
E.再充入1mol CO2,平衡正向移动,但n(CH3OH)/n(CO2)减小,故错误;
F.加入催化剂增大反应速率但平衡不移动,则n(CH3OH)/n(CO2)不变,故错误;
故选D;
③反应达到平衡后,若向反应体系再加入CO2(g)、H2(g)、CH3OH(g)、H2O(g)各1mol,
c(CO2)=0.25mol/L+0.5mol/L=0.75mol/L、c(CH3OH)=c(H2O)=0.75mol/L+0.5mol/L=1.25mol/L、c(H2)=3mol/L-0.75mol/L×3+0.5mol/L=1.25mol/L,
浓度商=
=1.1<5.33,平衡正向移动,
故答案为:正向;
④甲中反应达到平衡状态时n(CO2)=0.5mol、c(CH3OH)=c(H2O)=1.5mol、c(H2)=1.5mol,
如果乙中反应达到平衡状态时各物质与甲中相同,则a+c=2mol,且起始时维持化学反应向逆反应方向进行,b应该大于甲中转化的二氧化碳物质的量,属于c的取值范围为1.5 mol/L<c≤2 mol/L,
故答案为:1.5 mol/L<c≤2 mol/L;
(3)因为氨基甲酸铵极易水解成碳酸铵,即反应式为NH2COONH4(s)+H2O⇌(NH4)2CO3,加入1L0.1mol/L的盐酸溶液中直到溶液pH=7并且溶液中几乎不含碳元素,所以溶液中只有H+、NH4+、OH-、Cl-,根据电荷守恒c(NH4+)=c(Cl-)=0.1mol/L,又用去0.052mol氨基甲酸铵,所以开始溶液中的铵根离子浓度为0.052mol/L×2=0.104mol/L,
该反应NH4++H2O⇌NH3•H2O+H+;
开始 0.104mol/L 0
转化 0.004mol/L 0.004mol/L
平衡 0.1mol/L 0.004mol/L
又溶液为pH=7,所以氢离子浓度为10-7mol/L,则NH4+水解平衡常数Kh=
=
mol/L=4×10-9mol/L,
故答案为:0.1mol/L;4×10-9 mol/L.
反应Ⅱ:CO2(g)+H2(g)⇌CO (g)+H2O(g)△H2
反应Ⅲ:CO(g)+2H2(g)⇌CH3OH(g)△H3=-90.77kJ•mol-1
根据盖斯定律,反应Ⅱ可以是Ⅰ-Ⅲ得到,所以反应Ⅱ的焓变△H2=(-49.58kJ•mol-1)-(-90.77kJ•mol-1)=+41.19 kJ•mol-1;根据反应自发行的判据:△H-T△S<0,反应Ⅲ是熵减的放热的反应,所以要自发进行需要在较低温下进行,
故答案为:+41.19 kJ•mol-1;较低温;
(2)①前3min内,平均反应速率v(CO2)=
| 1.00-0.50 |
| 3 |
| 1 |
| 6 |
平均反应速率v(H2)=3v(CO2)=
| 1 |
| 6 |
平衡时,c(CO2)=0.25mol/L、c(CH3OH)=c(H2O)=0.75mol/L、c(H2)=3mol/L-0.75mol/L×3=0.75mol/L,
化学平衡常数K=
| c(CH3OH).c(H2O) |
| c(CO2).c3(H2) |
| 0.75×0.75 |
| 0.25×0.753 |
故答案为:0.5;5.33;
②A.升高温度增大反应速率,但平衡逆向移动,则n(CH3OH)/n(CO2)减小,故错误;
B.充入惰性气体,反应物和生成物浓度不变,平衡不移动,n(CH3OH)/n(CO2)不变,反应速率不变,故错误;
C.将H2O(g)从体系中分离,平衡正向移动,但反应速率减小,故错误;
D.再充入1mol H2 ,平衡正向移动,二氧化碳的物质的量减小、甲醇的物质的量增大,反应速率增大且n(CH3OH)/n(CO2)增大,故正确;
E.再充入1mol CO2,平衡正向移动,但n(CH3OH)/n(CO2)减小,故错误;
F.加入催化剂增大反应速率但平衡不移动,则n(CH3OH)/n(CO2)不变,故错误;
故选D;
③反应达到平衡后,若向反应体系再加入CO2(g)、H2(g)、CH3OH(g)、H2O(g)各1mol,
c(CO2)=0.25mol/L+0.5mol/L=0.75mol/L、c(CH3OH)=c(H2O)=0.75mol/L+0.5mol/L=1.25mol/L、c(H2)=3mol/L-0.75mol/L×3+0.5mol/L=1.25mol/L,
浓度商=
| 1.25×1.25 |
| 0.75×1.253 |
故答案为:正向;
④甲中反应达到平衡状态时n(CO2)=0.5mol、c(CH3OH)=c(H2O)=1.5mol、c(H2)=1.5mol,
如果乙中反应达到平衡状态时各物质与甲中相同,则a+c=2mol,且起始时维持化学反应向逆反应方向进行,b应该大于甲中转化的二氧化碳物质的量,属于c的取值范围为1.5 mol/L<c≤2 mol/L,
故答案为:1.5 mol/L<c≤2 mol/L;
(3)因为氨基甲酸铵极易水解成碳酸铵,即反应式为NH2COONH4(s)+H2O⇌(NH4)2CO3,加入1L0.1mol/L的盐酸溶液中直到溶液pH=7并且溶液中几乎不含碳元素,所以溶液中只有H+、NH4+、OH-、Cl-,根据电荷守恒c(NH4+)=c(Cl-)=0.1mol/L,又用去0.052mol氨基甲酸铵,所以开始溶液中的铵根离子浓度为0.052mol/L×2=0.104mol/L,
该反应NH4++H2O⇌NH3•H2O+H+;
开始 0.104mol/L 0
转化 0.004mol/L 0.004mol/L
平衡 0.1mol/L 0.004mol/L
又溶液为pH=7,所以氢离子浓度为10-7mol/L,则NH4+水解平衡常数Kh=
| c(NH3.H2O).c(H+) |
| c(NH4+) |
| 0.004×10-7 |
| 0.1 |
故答案为:0.1mol/L;4×10-9 mol/L.
看了 第21届联合国气候大会于20...的网友还看了以下:
物质H俗称衣康酸,是制备高效粘合剂等多种精细化学品的重要原理,可经下列反应路线得到:答案回答下列问 2020-05-12 …
空气源热泵的实际节能效率到底能达到多少看了很多空气源热泵的介绍,包括数据分析,都显示很节能,能效比 2020-05-17 …
设备的综合精度可用( )来衡量。 A.综合效率B.精度指数C.设备能力使用率D.系统效率 2020-05-19 …
Windows 98的设备管理程序负责组织和管理系统中的各种I/O设备,有效地处理用户(程序)对这 2020-05-23 …
Windows 98的设备管理程序负责组织和管理系统中的各种I/O设备,有效地处理用户(程序)对这些 2020-05-23 …
Windows98的设备管理程序负责组织和管理系统中的各种I/O设备,有效地处理用户(程序)对这些设 2020-05-23 …
在网络管理的5个功能中,确定设备的地理位置、名称、记录并维护设备参数表的功能属于()。A.配置管理B 2020-05-24 …
电是社会发展的必备能源,有关人士呼吁请社会有序有效用电,做好节约用电工作.就家庭、学校和社会如何节 2020-06-11 …
同业拆借市场的功能是( )。 A.准备金管理B.高效率和低成本的结算机制C.及时发现货币 2020-06-27 …
为什么说制备氢气能量损耗大?看网上关于新能源汽车技术路线的介绍.在提到锂空气电池和氢燃料电池时,都提 2020-12-05 …