早教吧作业答案频道 -->化学-->
硝酸铝Al(NO3)3是一种常用媒染剂.工业上用铝灰(主要含Al、Al2O3、Fe2O3等),制取硝酸铝晶体[A1(NO3)3•9H2O]的流程如图(1)写出反应I的离子方程式:(任写一个)(2)若在实
题目详情
硝酸铝【Al (NO3) 3】是一种常用媒染剂.工业上用铝灰(主要含Al、Al2O3、Fe2O3等),制取硝酸铝晶体[A1 (NO3)3•9H2O]的流程如图
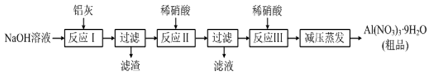
(1)写出反应I的离子方程式:___(任写一个)
(2)若在实验室中完成反应II,为避免铝的损失,需要解决的问题是___,可采取的措施为___
(3)上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的___
(4)实验室可以用图所示实验装置制取Al(NO3)3.
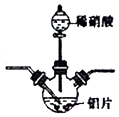
①下列措施可以用来提高反应速率的是___
A.从右端导管通入热的水蒸气 B.改用浓硝酸 C.适当加热
②随着反应的进行,硝酸被消耗,当硝酸浓度低到一定程度时,硝酸中的氮元素会被还原到最低价态,写出此时反应的离子方程式___.

(1)写出反应I的离子方程式:___(任写一个)
(2)若在实验室中完成反应II,为避免铝的损失,需要解决的问题是___,可采取的措施为___
(3)上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的___
(4)实验室可以用图所示实验装置制取Al(NO3)3.

①下列措施可以用来提高反应速率的是___
A.从右端导管通入热的水蒸气 B.改用浓硝酸 C.适当加热
②随着反应的进行,硝酸被消耗,当硝酸浓度低到一定程度时,硝酸中的氮元素会被还原到最低价态,写出此时反应的离子方程式___.
▼优质解答
答案和解析
(1)反应I的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑、Al2O3+2OH-═2AlO2-+H2O,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑或Al2O3+2OH-═2AlO2-+H2O;
(2)若在实验室中完成反应II,为避免铝的损失,由氢氧化铝具有两性可知,溶于强酸、强碱,则需要解决的问题是如何控制反应终点(或硝酸的用量),可采取的措施为将加入稀硝酸改为通入过量二氧化碳,
故答案为:如何控制反应终点(或硝酸的用量);将加入稀硝酸改为通入过量二氧化碳;
(3)硝酸铝为强酸弱碱盐,可发生水解,则上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的防止硝酸铝水解,
故答案为:防止硝酸铝水解;
(4)①升高温度可加快反应速率,则AC均可升高温度、加快反应速率,而B中Al与浓硝酸发生钝化,反应速率减小,故答案为:AC;
②当硝酸浓度低到一定程度时,硝酸中的氮元素会被还原到最低价态,可知Al与硝酸反应生成铵根离子、铝离子,该反应的离子反应为8Al+3NO3-+30 H+═8Al3++3NH4++9H2O,
故答案为:8Al+3NO3-+30 H+═8Al3++3NH4++9H2O.
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑或Al2O3+2OH-═2AlO2-+H2O;
(2)若在实验室中完成反应II,为避免铝的损失,由氢氧化铝具有两性可知,溶于强酸、强碱,则需要解决的问题是如何控制反应终点(或硝酸的用量),可采取的措施为将加入稀硝酸改为通入过量二氧化碳,
故答案为:如何控制反应终点(或硝酸的用量);将加入稀硝酸改为通入过量二氧化碳;
(3)硝酸铝为强酸弱碱盐,可发生水解,则上述流程中采用减压蒸发,并控制反应Ⅲ中加入的稀硝酸稍过量,其目的防止硝酸铝水解,
故答案为:防止硝酸铝水解;
(4)①升高温度可加快反应速率,则AC均可升高温度、加快反应速率,而B中Al与浓硝酸发生钝化,反应速率减小,故答案为:AC;
②当硝酸浓度低到一定程度时,硝酸中的氮元素会被还原到最低价态,可知Al与硝酸反应生成铵根离子、铝离子,该反应的离子反应为8Al+3NO3-+30 H+═8Al3++3NH4++9H2O,
故答案为:8Al+3NO3-+30 H+═8Al3++3NH4++9H2O.
看了 硝酸铝Al(NO3)3是一种...的网友还看了以下:
用完全一样的正方体白几何体.从上往下,第一层放1个,第二层放4个,第三层放9个,依次类推.直到放带第 2020-03-30 …
碳酸镁(MgCO3)与碳酸钙(CaCO3)同属于碳酸盐,化学性质相似,人的胃液里含有适量盐酸,服用 2020-04-11 …
如果m是2013的算术平方根,那么2013/100的平方根用含m的式子表示为 2020-06-13 …
(2014•营口一模)如图是胃得乐牌胃药的部分标识.胃药中所含的物质中和胃里过多的胃酸.某患者按标 2020-06-23 …
如图在长方形的钢板上,从中挖去两个小长方形,用含a,b的代数式表示剩余的部分面积 2020-07-11 …
硝酸钾和硫酸钾配置水培营养液时K2O怎么计算?营养液配方肥料名称用量(毫克/升)硝酸钾333硫酸钾 2020-07-19 …
已知x=5的m次方+1,y=3+25m次方,用含x的代数式表示y已知x=5的m次方+1,y=3+2 2020-07-31 …
已知m等于八的九次方,n等于九的八次方,用含m,n的式子表示七十二的七十二次方 2020-11-07 …
(2012•仙桃)胃溃疡病人要治疗胃酸(主要含稀盐酸)过多症不宜服用含NaHCO3的药片,可服用含A 2020-11-13 …
全市至少有6×l05个水龙头,2×l05个抽水马桶漏水,如果一个关不紧的水龙头,一个月能漏掉a立方米 2020-12-09 …