早教吧作业答案频道 -->化学-->
钢铁工业是一个国家的支柱产业之一.某同学采集了一些生铁样品(含杂质,杂质不溶于水,不与稀硫酸反应)采用如图甲所示装置进行分析,分别称得锥形瓶与棉花的质量为44.1g,生铁样
题目详情
钢铁工业是一个国家的支柱产业之一.某同学采集了一些生铁样品(含杂质,杂质不溶于水,不与稀硫酸反应)采用如图甲所示装置进行分析,分别称得锥形瓶与棉花的质量为44.1g,生铁样品的质量为9.0g.在锥形瓶中加入足量稀硫酸后,立即开始记录电子天平的示数,记录数据如图乙,请认真分析数据,回答下列问题.(锥形瓶中发生的化学反应为:Fe+H2SO4═FeSO4+H2↑)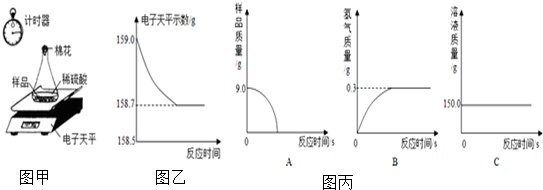
(1)如何判断试验中生铁样品已经完全反应.___.
(2)根据电子天平的数据变化进行分析,如图丙图象中正确的是___.
(3)计算反应后所得溶液中硫酸亚铁的质量分数.

(1)如何判断试验中生铁样品已经完全反应.___.
(2)根据电子天平的数据变化进行分析,如图丙图象中正确的是___.
(3)计算反应后所得溶液中硫酸亚铁的质量分数.
▼优质解答
答案和解析
(1)铁可以与盐酸反应产生氢气,所以继续向反应后的滤渣中加入稀硫酸,如果没有气泡冒出,则说明生铁样品已经完全反应;故答案为:继续向反应后的滤渣中加入稀硫酸,如果没有气泡冒出,则说明生铁样品已经完全反应;
(2)A、反应结束后,样品中的杂质仍然存在,该选项不正确;
B、生成氢气的质量为:159.0g-158.7g=0.3g,该选项正确;
C、随着反应的进行,溶液质量在增加,该选项不正确.
故填:B.
(2)设铁的质量为x,生成硫酸亚铁的质量为y,
Fe+H2SO4═FeSO4+H2↑,
56 152 2
x y 0.3g
=
=
,
x=8.4g,y=22.8g,
稀硫酸的质量为:159.0g-44.1g-9.0g=105.9g,
形成溶液的质量为:8.4g+105.9g-0.3g=114g,
反应后所得溶液中硫酸亚铁的质量分数为:
×100%=20%,
答:反应后所得溶液中硫酸亚铁的质量分数为20%
(2)A、反应结束后,样品中的杂质仍然存在,该选项不正确;
B、生成氢气的质量为:159.0g-158.7g=0.3g,该选项正确;
C、随着反应的进行,溶液质量在增加,该选项不正确.
故填:B.
(2)设铁的质量为x,生成硫酸亚铁的质量为y,
Fe+H2SO4═FeSO4+H2↑,
56 152 2
x y 0.3g
| 56 |
| x |
| 152 |
| y |
| 2 |
| 0.3g |
x=8.4g,y=22.8g,
稀硫酸的质量为:159.0g-44.1g-9.0g=105.9g,
形成溶液的质量为:8.4g+105.9g-0.3g=114g,
反应后所得溶液中硫酸亚铁的质量分数为:
| 22.8g |
| 114g |
答:反应后所得溶液中硫酸亚铁的质量分数为20%
看了 钢铁工业是一个国家的支柱产业...的网友还看了以下:
如图甲、乙、丙三图中的装置完全相同.燃料的质量都是10g,烧杯内的液体质量也相同.(1)比较不同燃 2020-05-02 …
catia装配问题一个由两部分组成的图,每个部分由若干个部分组成,我先把每个部分分别装配,得到两个 2020-05-13 …
某学生在进行二氧化碳的制取和性质实验时经过认真分析研究对课本中的气体发生装置(如图A)进行了改进( 2020-05-13 …
某学生在进行二氧化碳的制取和性质实验时,经过认真分析研究,对课本中的气体发生装置(图A)进行了改进 2020-05-13 …
某学生在进行二氧化碳的制取和性质实验时,经过认真分析研究,对课本中的气体发生装置(图A)进行了改进 2020-05-13 …
某学生在进行二氧化碳的制取和性质实验时,经过认真分析研究,对教材中的气体发生装置(如图A所示)进行 2020-05-13 …
某课外小组设计了下图所示的实验装置(图中固定装置已略去),进行SO2性质的研究.(1)从物质分类的 2020-06-10 …
关于solidworks干涉问题我先用CAD做好的设计图,装配都没有问题,但是转到solidwor 2020-06-27 …
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验.主要实验步 2020-07-21 …
已知Mg能在CO2中燃烧生成碳和一种白色固体物质,某化学兴趣小组用如图所示装置制备CO2并对Mg在C 2020-11-01 …