早教吧作业答案频道 -->化学-->
完成下列方程式(1)在298K,101KPa条件下,1mol氢气在氧气中燃烧生成液态水放出285.8kJ热量,写出该反应的热化学方程式:(2)如图所示,写出①固体C和氧气生成CO2气体的热化学方程式:
题目详情
完成下列方程式
(1)在298K,101KPa条件下,1mol氢气在氧气中燃烧生成液态水放出285.8kJ热量,写出该反应的热化学方程式:___
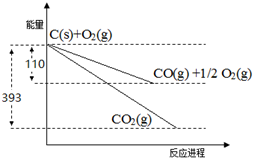
(2)如图所示,写出①固体C和氧气生成CO2气体的热化学方程式:___
②固体C和CO2气体生成CO气体的热化学方程式:___
(3)电解质为H2SO4溶液的CH4和O2燃料电池负极电极反应式:___
(4)某碱性电池的电池反应为3Zn+2K2FeO4
Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:___.

(1)在298K,101KPa条件下,1mol氢气在氧气中燃烧生成液态水放出285.8kJ热量,写出该反应的热化学方程式:___
(2)如图所示,写出①固体C和氧气生成CO2气体的热化学方程式:___
②固体C和CO2气体生成CO气体的热化学方程式:___
(3)电解质为H2SO4溶液的CH4和O2燃料电池负极电极反应式:___
(4)某碱性电池的电池反应为3Zn+2K2FeO4
| 放电 |
| |
| 充电 |
▼优质解答
答案和解析
(1)在298K,101KPa时,1molH2完全燃烧生成液态水释放出285.8KJ的能量,则表示H2燃烧热的化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol,
故答案为:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol;
(2)①由图1molC和氧气完全反应生成1molCO2气体,放出热量为:393KJ的热量,C(s)+O2(g)=CO2(g)△H=-393KJ/mol,故答案为:C(s)+O2(g)=CO2(g)△H=-393KJ/mol;
②C(s)+O2(g)=CO2(g)△H=-393KJ/mol…Ⅰ;C(s)+
O2(g)=CO(g)△H=-110kJ/mol…Ⅱ;由盖斯定律:2Ⅱ-Ⅰ可知:C(s)+CO2(g)=2CO(g),△H=-110×2+393=+173KJ/mol,故答案为:C(s)+CO2(g)=2CO(g),△H=+173KJ/mol;
(3)在CH4燃料电池中,负极上是燃料CH4发生失电子的氧化反应,在酸性环境下,电极反应为:CH4-8e-+2H2O=CO2+8H+,总反应式为CH4+2O2=CO2+2H2O,故答案为:CH4-8e-+2H2O=CO2+8H+;
(4)电池充电时阳极发生氧化反应,化合价升高,电极反应式为:Fe2O3-6e-+10OH-=2FeO42-+5H2O,故答案为:Fe2O3-6e-+10OH-=2FeO42-+5H2O.
故答案为:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol;
(2)①由图1molC和氧气完全反应生成1molCO2气体,放出热量为:393KJ的热量,C(s)+O2(g)=CO2(g)△H=-393KJ/mol,故答案为:C(s)+O2(g)=CO2(g)△H=-393KJ/mol;
②C(s)+O2(g)=CO2(g)△H=-393KJ/mol…Ⅰ;C(s)+
| 1 |
| 2 |
(3)在CH4燃料电池中,负极上是燃料CH4发生失电子的氧化反应,在酸性环境下,电极反应为:CH4-8e-+2H2O=CO2+8H+,总反应式为CH4+2O2=CO2+2H2O,故答案为:CH4-8e-+2H2O=CO2+8H+;
(4)电池充电时阳极发生氧化反应,化合价升高,电极反应式为:Fe2O3-6e-+10OH-=2FeO42-+5H2O,故答案为:Fe2O3-6e-+10OH-=2FeO42-+5H2O.
看了 完成下列方程式(1)在298...的网友还看了以下:
allow后动词的形式是什么只能加todo吗?但参考书上有allowdoings.th,allow 2020-05-17 …
设直线L分别与X轴Y轴交与点AB,如果直线M:Y=KX+T(T大于0)与直线L平行且交X轴于C,求 2020-06-12 …
关于DNA的拓扑结构L=T+WDNA拓扑结构中有意个公式L=T+W,书上说在DNA任何拓扑状态下L 2020-06-14 …
300m l 某浓度的NaOH溶液中含有60克溶质,现欲配置1m o l/LNaOH溶液,应取原溶 2020-06-27 …
(S="Student;"T=Teacher)S:Excuseme,Mr.Lee.31youhelp 2020-10-30 …
英语翻译Oneday,whileIwasplayingwithmynewdoll,MissSulli 2020-11-01 …
刚才你帮我写的这句公式有错误哦!(H-MAX(C,O))>(MIN(C,O)-L)or((H-MAX 2020-11-04 …
请教英语中的姓名经常在英语的参考文献中看到:O.L.V.CostaandM.D.FragosoM.A 2020-11-06 …
完全竞争厂商的生产函数是Q=12L-L2(O≤L≤6),其中L是每天的劳动投入,Q是每天的产出。若产 2020-11-30 …
英语单词排列以下字母排列成一个单词,1.e,n,a,l,r2.a,o,o,l,l,b,f,t3.i, 2020-12-24 …