早教吧作业答案频道 -->化学-->
(1)在一定条件下N2和H2完全反应生成1molNH3放热46.0kJ热量.写出氨分解为氢气和氮气的热化学方程式(2)已知下列两个热化学方程式:H2O(I)═H2O(g)△H═+285.8kJ/molC3H8(g)+5O2(g)═3C
题目详情
(1)在一定条件下N2和H2完全反应生成1molNH3放热46.0kJ热量.写出氨分解为氢气和氮气的热化学方程式___
(2)已知下列两个热化学方程式:H2O(I)═H2O(g)△H═+285.8kJ/mol
C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220kJ/mol
则0.5mol丙烷燃烧生成CO2和气态水时释放的热量为___.
(3)(1)已知:TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ•mol-1
2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:___.
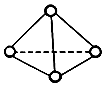
(4)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体如图所示),与白磷分子相似.已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则 1mol N4气体转化为2mol N2时要放出___kJ能量
(5)有机化合物常用作燃料电池,甲烷是常用的燃料之一,若甲烷燃料电池中电解质溶液为KOH溶液,电池放电时是将___能转化为___能,其负极反应式为:___.
(2)已知下列两个热化学方程式:H2O(I)═H2O(g)△H═+285.8kJ/mol
C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220kJ/mol
则0.5mol丙烷燃烧生成CO2和气态水时释放的热量为___.
(3)(1)已知:TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ•mol-1
2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:___.
(4)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体如图所示),与白磷分子相似.已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则 1mol N4气体转化为2mol N2时要放出___kJ能量
(5)有机化合物常用作燃料电池,甲烷是常用的燃料之一,若甲烷燃料电池中电解质溶液为KOH溶液,电池放电时是将___能转化为___能,其负极反应式为:___.

▼优质解答
答案和解析
(1)N2和H2完全反应生成1molNH3放热46.0kJ热量,生成2mol氨气放热92KJ,氨气分解为吸热反应,反应的焓变为+92KJ,反应的热化学方程式为:2NH3(g)=N2(g)+3H2(g)△H=+92KJ/mol;
故答案为:2NH3(g)=N2(g)+3H2(g)△H=+92KJ/mol;
(2)①C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220.0kJ•mol-1
②H2O(l)═H2O(g)△H=+44.0kJ•mol-1
则丙烷燃烧生成CO2和气态水时的反应为:C3H8(g)+5O2(g)═3CO2(g)+4H2O(g),△H=①+②×4=-2220.0kJ•mol-1+4×44.0kJ•mol-1=2044kJ•mol-1,所以
0.5mol丙烷燃烧生成CO2和气态水时释放的热量为1022kJ,故答案为:1022kJ;
(3)①TiO2 (s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ•mol-1
②2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
依据盖斯定律①+②得到:TiO2(s)+2C(s)+2Cl2(g)═TiCl4(l)+2CO(g)△H=-81kJ•mol-1;
故答案为:TiO2(s)+2C(s)+2Cl2(g)═TiCl4(l)+2CO(g)△H=-81kJ•mol-1;
(4)根据原子守恒知,一个N4分子生成2个N2分子,一个N4分子中含有6个N-N键,破坏1molN4分子中含有6molN-N键需要吸收193kJ/mol×6mol=1158KJ能量;
生成2molN≡N键放出941kJ/mol×2mol=1882KJ能量,所以该反应放出1884KJ-1158KJ=724KJ能量,所以热化学反应方程式为N4(g)=2N2(g)△H=-724KJ/mol,
故答案为:724;
(5)电池放电时是原电池,将化学能转化为电能,负极发生氧化反应,电极反应式为:CH4+10OH--8e-=CO32-+7H2O,故答案为:化学;电;CH4+10OH--8e-=CO32-+7H2O.
故答案为:2NH3(g)=N2(g)+3H2(g)△H=+92KJ/mol;
(2)①C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220.0kJ•mol-1
②H2O(l)═H2O(g)△H=+44.0kJ•mol-1
则丙烷燃烧生成CO2和气态水时的反应为:C3H8(g)+5O2(g)═3CO2(g)+4H2O(g),△H=①+②×4=-2220.0kJ•mol-1+4×44.0kJ•mol-1=2044kJ•mol-1,所以
0.5mol丙烷燃烧生成CO2和气态水时释放的热量为1022kJ,故答案为:1022kJ;
(3)①TiO2 (s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ•mol-1
②2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
依据盖斯定律①+②得到:TiO2(s)+2C(s)+2Cl2(g)═TiCl4(l)+2CO(g)△H=-81kJ•mol-1;
故答案为:TiO2(s)+2C(s)+2Cl2(g)═TiCl4(l)+2CO(g)△H=-81kJ•mol-1;
(4)根据原子守恒知,一个N4分子生成2个N2分子,一个N4分子中含有6个N-N键,破坏1molN4分子中含有6molN-N键需要吸收193kJ/mol×6mol=1158KJ能量;
生成2molN≡N键放出941kJ/mol×2mol=1882KJ能量,所以该反应放出1884KJ-1158KJ=724KJ能量,所以热化学反应方程式为N4(g)=2N2(g)△H=-724KJ/mol,
故答案为:724;
(5)电池放电时是原电池,将化学能转化为电能,负极发生氧化反应,电极反应式为:CH4+10OH--8e-=CO32-+7H2O,故答案为:化学;电;CH4+10OH--8e-=CO32-+7H2O.
看了 (1)在一定条件下N2和H2...的网友还看了以下:
智能化设备的安装应在( )进行。A.土建工程完工后B.装饰工程完工后C.机电工程施工时D.土建 2020-05-18 …
某城市计划分三期修建绿荫大道,第一期工程完工后,还剩全部工程的1419没有完成,第二期工程完成的路 2020-05-21 …
某城市计划分三期修建绿荫大道,第一期工程完工后,还剩全部工程的1419没有完成,第二期工程完成的路 2020-05-21 …
下列有关光合作用的叙述,正确的是A.光合作用全过程都需要光B.光合作用全过程都需要酶的催化C.光合 2020-05-23 …
阅读下列解方程的过程,并完成(1)、(2)小题的解答.解方程:|x-1|=2当x-1<0,即x<1 2020-07-19 …
红树林对污染的净化作用是通过物理沉降,化学分解和等过程完成的.1:红树林对污染的净化作用是通过物理沉 2020-11-04 …
秋天,小草走完了生命的旅程,化为一撮泥土,融进了大地的血脉。解释一下~~秋天,小草走完了生命的旅程, 2020-12-05 …
阅读下边的文字,完成15―18题。(18分)短信文化的流行原因短信这种民俗文化,可以看作是“大众文化 2020-12-15 …
阅读下文,完成文后各题。短信文化的流行原因短信这种民俗文化,可以看作是“大众文化”对“精英文化”的又 2020-12-15 …
在内燃机的四个冲程中,只有两个冲程完成了能量转化,在做功冲程中,是将能转化为能. 2021-01-14 …