早教吧作业答案频道 -->化学-->
已知下列数据:物质熔点(℃)沸点(℃)密度(g•cm-3)乙醇-117.078.00.79乙酸16.6117.91.05乙酸乙酯-83.677.50.90浓硫酸(98%)-338.01.84
题目详情
已知下列数据:
学生在实验室制取乙酸乙酯的主要步骤如下:
①在30mL的大试管A中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合溶液;
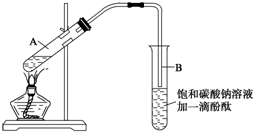
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10min;
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥.
请根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为___写出制取乙酸乙酯的化学方程式:___
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)___.
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热操作,其主要理由是___
(4)分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为(填字母)___.
A.P2O5 B.无水Na2SO4 C.碱石灰 D.NaOH固体.
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.0 | 78.0 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | - | 338.0 | 1.84 |
①在30mL的大试管A中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合溶液;
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10min;
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥.
请根据题目要求回答下列问题:

(1)配制该混合溶液的主要操作步骤为___写出制取乙酸乙酯的化学方程式:___
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)___.
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热操作,其主要理由是___
(4)分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为(填字母)___.
A.P2O5 B.无水Na2SO4 C.碱石灰 D.NaOH固体.
▼优质解答
答案和解析
(1)乙酸和乙醇在浓硫酸的催化作用下反应生成乙酸乙酯和水,其反应方程式为:CH3COOH+C2H5OH
CH3COOC2H5+H2O,
故答案为:CH3COOH+C2H5OH
CH3COOC2H5+H2O;
(2)乙酸具有酸性,能和饱和碳酸钠溶液反应而把被吸收,乙酸乙酯在饱和碳酸钠溶液中的溶解度较小,易于分离,
故答案为:BC;
(3)反应物中乙醇、乙酸的沸点较低,若用大火加热,大量反应物随产物蒸发而损失原料,温度过高还可能发生其他副反应,所以为防止乙醇、乙酸挥发,造成原料的损失,应小火加热,
故答案为:防止反应物随生成物一起大量被蒸出来,导致原料损失及发生副反应;
(4)干燥乙酸乙酯,用无水硫酸钠除去少量的水,无水硫酸钠吸水形成硫酸钠结晶水合物;不能选择P2O5、碱石灰和NaOH等固体干燥剂,以防乙酸乙酯在酸性(P2O5遇水生成酸)或碱性条件下水解.
故答案为:B.
| 浓硫酸 |
| △ |
故答案为:CH3COOH+C2H5OH
| 浓硫酸 |
| △ |
(2)乙酸具有酸性,能和饱和碳酸钠溶液反应而把被吸收,乙酸乙酯在饱和碳酸钠溶液中的溶解度较小,易于分离,
故答案为:BC;
(3)反应物中乙醇、乙酸的沸点较低,若用大火加热,大量反应物随产物蒸发而损失原料,温度过高还可能发生其他副反应,所以为防止乙醇、乙酸挥发,造成原料的损失,应小火加热,
故答案为:防止反应物随生成物一起大量被蒸出来,导致原料损失及发生副反应;
(4)干燥乙酸乙酯,用无水硫酸钠除去少量的水,无水硫酸钠吸水形成硫酸钠结晶水合物;不能选择P2O5、碱石灰和NaOH等固体干燥剂,以防乙酸乙酯在酸性(P2O5遇水生成酸)或碱性条件下水解.
故答案为:B.
看了 已知下列数据:物质熔点(℃)...的网友还看了以下:
两个容器,甲装有11kg硫酸,乙有15kg水.先把甲的硫酸倒入乙一部分,搅匀,乙再倒入甲一部分.要 2020-05-05 …
取甲种盐酸200克,乙种盐酸150克,再加上纯盐酸200克,可混合成浓度为80%的盐酸;如果取甲盐 2020-05-13 …
关于乙酸乙酸钠缓冲溶液PH值的问题因需要配制PH4.5乙酸乙酸钠缓冲溶液,在网站上找了很多方法,请 2020-05-17 …
解释为何乙酸和乙酸钠混合溶液pH=4.71,急实验的题目.实验中用10ml,1mol/L的乙酸和同 2020-06-27 …
向20ML氢离子浓度为0.001MOL/L乙酸逐滴加入0.2MOL/L氨水当加入10ML时导电性最 2020-06-27 …
甲走的路程是乙的4/5,乙用的时间是甲的4/5,甲、乙速度比是().有人说(4/5)*(4/5)= 2020-07-17 …
化学反应速率和化学平衡应用题乙酸和乙醇生成乙酸乙酯的反应在室温下按下式达到平衡:CH3COOH+C 2020-07-29 …
如何将冰乙酸变成乙酸我需要的是乙酸,但是实验室就只有冰乙酸了,纯度大,不知道如何稀释至乙酸.1对, 2020-07-29 …
NA2SO4与乙谜反应么分离出的乙酸乙酯常常带有一定量的乙醇水与乙醚应先加入无水CACL2分离出水和 2020-11-29 …
乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.有关数据及副反应:乙酸乙醇乙酸乙酯乙醚沸 2021-01-26 …