向盛有10mLlmol/LNH4Al(SO4)2溶液的烧杯中滴加1mol/LNaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如图.下列有关说法正确的是()A.当加入50mLNaOH时,溶液中的溶质为NaAlO2B.m点反应的
向盛有10mLlmol/LNH4Al(SO4)2溶液的烧杯中滴加1mol/LNaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如图.下列有关说法正确的是( )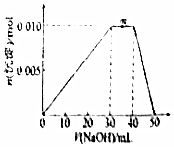
A. 当加入50mLNaOH时,溶液中的溶质为NaAlO2
B. m点反应的离子方程式:NH4++OH-═NH3•H2O
C. NH4Al(SO4)2溶液中离子浓度由大到小的顺序是:c(SO42-)>c(Al3+)>c(NH4+)>c(H+)>c(OH-)
D. 若向NH4Al(SO4)2溶液改加20mL1.2mol/L Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为0.02mol
A.当加入50mLNaOH时,溶液中的溶质为NaAlO2、NH3.H2O,而不是单一的偏铝酸钠,故A错误;
B.m点NaOH溶液体积在30-40mL之间,所以发生第二个离子方程式,方程式为:NH4++OH-═NH3•H2O,故B正确;
C.NH4Al(SO4)2溶液中铵根离子、铝离子都易发生水解反应,且铝离子水解程度大于铵根离子,所以离子浓度由大到小的顺序是:c(SO42-)>c(NH4+)>c(Al3+)>c(H+)>c(OH-),故C错误;
D.n[NH4Al(SO4)2]=1mol/L×0.01L=0.01mol、n[Ba(OH)2]=1.2mol/L×0.02L=0.024mol,而硫酸根离子的物质的量为0.02mol,而钡离子的物质的量为0.024mol,所以钡离子过量,硫酸根离子完全反应,生成0.02mol硫酸钡;又知0-40mL时铝离子和铵根离子消耗氢氧根离子的物质的量为0.04mol,而氢氧根离子的总物质的量是0.048mol,此时溶解0.008mol的氢氧化铝,所以沉淀的物质的量为0.022mol,故D错误;
故选B.
从Ca、Mg、O、H、N中选择适当的元素,按要求写出相应物质的化学式:(1)一种酸性氧化物;(2) 2020-04-11 …
(1)由H、N、O三种元素可组成单质,氧化物、酸、碱、盐等不同类别的物质,用化学式填空.①产生温室 2020-04-11 …
已知可逆反应:M(g)+N(g)===(可逆符号)P(g)+Q(g);△H>0.(为?.已知可逆反 2020-04-27 …
100克h硫酸溶液与一定量的锌粒恰好完全反应,反应后总质量比反应前少0.5克100克h⑵so⑷溶液 2020-06-03 …
PH相等即C(H+)相等1:HCL与2:HAC比较大小①C(HCL)C(HAC)②开始时Mg反应V 2020-06-04 …
下列离子方程式书写不正确的是()A.AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)= 2020-07-20 …
电解质溶液中的守恒关系.电荷守恒:电解质溶液中所有阳离子所带有的正电荷数与所有的阴离子所带的负电荷 2020-07-29 …
若数字滤波器的单位脉冲响应h(n)是对称的,长度为N,则它的对称中心是为啥 2020-08-02 …
H,C,N,O四种元素按顺序可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠 2020-11-03 …
常温下,将含0.1molCH3COONa的溶液和0.04molHCl的溶液混合(1)混合后溶液中有两 2021-02-18 …