早教吧作业答案频道 -->化学-->
用化学知识回答下列问题:(1)R原子的3p轨道上只有一个未成对电子,则R原子可能是、;(填元素符号)Y原子的核电荷数为33,其外围电子排布是,其在元素周期表中的位置是,
题目详情
用化学知识回答下列问题:
(1)R原子的3p轨道上只有一个未成对电子,则R原子可能是___、___;(填元素符号)Y原子的核电荷数为33,其外围电子排布是___,其在元素周期表中的位置是___,是属于___区的元素.
(2)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为___.
(3)与CO分子互为等电子体的分子和离子分别为___和___(填化学式).
(4)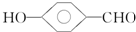 的沸点比
的沸点比 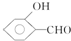 高,原因是___.
高,原因是___.
(5)H+可与H2O形成H3O+,H3O+中O原子采用___杂化,H3O+的空间构型是___.H3O+中H-O-H键角比H2O中H-O-H键角大,原因为___.
(1)R原子的3p轨道上只有一个未成对电子,则R原子可能是___、___;(填元素符号)Y原子的核电荷数为33,其外围电子排布是___,其在元素周期表中的位置是___,是属于___区的元素.
(2)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为___.
(3)与CO分子互为等电子体的分子和离子分别为___和___(填化学式).
(4)
 的沸点比
的沸点比  高,原因是___.
高,原因是___.(5)H+可与H2O形成H3O+,H3O+中O原子采用___杂化,H3O+的空间构型是___.H3O+中H-O-H键角比H2O中H-O-H键角大,原因为___.
▼优质解答
答案和解析
(1)R原子的3p轨道上只有一个未成对电子,则价层电子排布式为3s23p1或3s23p5,则R为Al元素或Cl元素,Y原子的核电荷数为33,则Y是As元素,其4s、4p电子为其外围电子,根据能量最低原理知其外围电子排布式4s24p3,主族元素的电子层数与其周期数相等、最外层电子数与其族序数相等,所以As元素位于第四周期第VA族,该元素最后排入的电子是p电子,所以As位于p区,故答案为:Al,Cl; 4S24P3,第四周期ⅤA,P区;
(2)共价键的键能大于氢键的作用力,氢键的作用力还大于范德华力,故H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为O-H键、氢键、分子间的范德华力,
故答案为:O-H键、氢键、范德华力;
(3)根据等电子体的定义,CO的等电子体必须是双原子分子或离子,且电子总数相等.对于原子,原子序数=原子核外电子总数,所以,如果是分子,只要原子序数之和相等即可.
CO中C是6号元素,O是8号元素,原子序数之和为14,N是7号元素,且可形成双原子分子,所以分子是N2.
如果是阳离子离子,原子序数之和减去所带电荷数值,如果是阴离子,原子序数之和加上所带电荷数值,等于CO的原子序数之和即可所以是CN-..
故答案为:N2、CN-;
(4)含分子间氢键的物质的沸点大于分子内氢键物质的沸点,因此原因是前者易形成分子间氢键,后者易形成分子内氢键,
故答案为: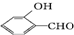 形成分子内氢键,而
形成分子内氢键,而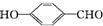 形成分子间氢键,分子间氢键使分子间作用力增大;
形成分子间氢键,分子间氢键使分子间作用力增大;
(5)H3O+价层电子对模型为四面体,氧原子采取sp3杂化,H3O+的空间构型是三角锥形,H2O中O原子有两对孤对电子,H3O+中O原子有一对孤对电子,因为孤电子对间的排斥力>孤电子对与成键电子对间的排斥力>成键电子对间的排斥力,导致H3O+中H-O-H键角比H2O中H-O-H键角大,故答案为:sp3,三角锥形;H2O中O原子有2对孤电子对,H3O+只有1对孤电子对,排斥力较小.
(2)共价键的键能大于氢键的作用力,氢键的作用力还大于范德华力,故H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为O-H键、氢键、分子间的范德华力,
故答案为:O-H键、氢键、范德华力;
(3)根据等电子体的定义,CO的等电子体必须是双原子分子或离子,且电子总数相等.对于原子,原子序数=原子核外电子总数,所以,如果是分子,只要原子序数之和相等即可.
CO中C是6号元素,O是8号元素,原子序数之和为14,N是7号元素,且可形成双原子分子,所以分子是N2.
如果是阳离子离子,原子序数之和减去所带电荷数值,如果是阴离子,原子序数之和加上所带电荷数值,等于CO的原子序数之和即可所以是CN-..
故答案为:N2、CN-;
(4)含分子间氢键的物质的沸点大于分子内氢键物质的沸点,因此原因是前者易形成分子间氢键,后者易形成分子内氢键,
故答案为:
 形成分子内氢键,而
形成分子内氢键,而 形成分子间氢键,分子间氢键使分子间作用力增大;
形成分子间氢键,分子间氢键使分子间作用力增大;(5)H3O+价层电子对模型为四面体,氧原子采取sp3杂化,H3O+的空间构型是三角锥形,H2O中O原子有两对孤对电子,H3O+中O原子有一对孤对电子,因为孤电子对间的排斥力>孤电子对与成键电子对间的排斥力>成键电子对间的排斥力,导致H3O+中H-O-H键角比H2O中H-O-H键角大,故答案为:sp3,三角锥形;H2O中O原子有2对孤电子对,H3O+只有1对孤电子对,排斥力较小.
看了 用化学知识回答下列问题:(1...的网友还看了以下:
圆周上放置有7个空盒子,按顺时针方向依次编号为1,2,3,4,5,6,7.小明首先将第1枚白色棋子 2020-05-13 …
圆周上放置有7个空盒子,按顺时针方向依次编号为1,2,3,4,5,6,7.小明首先将第1枚白色棋子 2020-05-17 …
1.甲骨文,金文(铭文),篆体的书写载体和朝代各是什么?2.(1)长太息以掩涕兮,哀民生之多艰!( 2020-05-21 …
如图所示,一根不可伸长的细绳一端固定在O点,另一端系一小球,O点的正下方固定有一根钉子P.位置1在 2020-05-23 …
氢原子中,电子是处于基态么?按照量子力学,电子的位置是不可知的,那电子就未必在基态了.可是如果在激 2020-06-02 …
在元旦联欢会上,3名小朋友分别站在△ABC三个顶点的位置上,他们在玩抢凳子游戏,要求在他们中间放一 2020-07-10 …
欧米茄三个小表盘什么意思3.6.9指针分别有三个表盘3位置是1020316位置是61218249位 2020-07-19 …
如图所示,一根不可伸长的细绳一端固定在O点,另一端系一小球,O点的正下方固定有一根钉子P.位置1在O 2020-11-01 …
如图所示,一根不可伸长的细绳一端固定在O点,另一端系一小球,O点的正下方固定有一根钉子P.位置1在O 2020-11-01 …
如图是测定发芽种子的细胞呼吸速率所用的实验装置(假设呼吸底物只有葡萄糖),装置1、2中分别放入等量的 2020-11-05 …