早教吧作业答案频道 -->化学-->
下列图象与对应的说法正确的是()A、向NaOH溶液中加水稀释B、等质量的Al、Zn与足量的稀硫酸反应C、向稀硫酸中加入Ba(OH)2溶液D、向NaOH
题目详情
下列图象与对应的说法正确的是( )
A、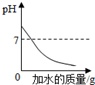 向NaOH溶液中加水稀释 |
B、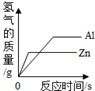 等质量的Al、Zn与足量的稀硫酸反应 |
C、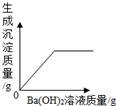 向稀硫酸中加入Ba(OH) 2 溶液 |
D、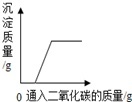 向NaOH和Ca(OH) 2 混合溶液中通入CO 2 |
▼优质解答
答案和解析
考点:
酸碱溶液的稀释 金属的化学性质 溶液的导电性及其原理分析
专题:
元素化合物知识型
分析:
A、向酸或碱溶液中不断的加水时,溶液的酸性或碱性就会不断的减小,但溶液不会变成中性,更不会变成碱性或酸性;B、在金属活动性顺序中,越靠前的金属化学性质越活泼,和稀酸溶液反应时表现出来的现象就越剧烈,在等同条件下,反应需要的时间也就越短,再就是得到1克氢气所需要的金属的质量为该金属的相对原子质量化合价;C、根据硫酸和氢氧化钡反应生成硫酸钡沉淀,随着反应的进行沉淀不断增加,当硫酸反应完毕后沉淀不再增加为一定值进行解答;D、根据二氧化碳同时与NaOH和Ca(OH)2发生反应解答.
A、由于是加水稀释碱溶液,因此无论加多少水,溶液仍为碱性溶液,pH值不会小于等于7,故A错误;B、由于在金属活动性顺序中,铝在锌前,因此铝反应需要的时间短,而该图象中时间和斜线的斜率有冲突,应该是斜率越大的,时间越短,金属的活动性越强,故B错误;C、硫酸和氢氧化钡反应生成硫酸钡沉淀,随着反应的进行沉淀不断增加,当硫酸反应完毕后沉淀不再增加为一定值,故C正确;D、二氧化碳同时与NaOH和Ca(OH)2,并且与氢氧化钙反应生成沉淀,所以从开始通二氧化碳时就有沉淀生成,故D错误.故选:C.
点评:
本题难度较大,主要考查了金属活动性顺序的应用、酸碱的有关的化学性质、酸碱溶液的稀释等,培养学生分析问题、解决问题的能力.
考点:
酸碱溶液的稀释 金属的化学性质 溶液的导电性及其原理分析
专题:
元素化合物知识型
分析:
A、向酸或碱溶液中不断的加水时,溶液的酸性或碱性就会不断的减小,但溶液不会变成中性,更不会变成碱性或酸性;B、在金属活动性顺序中,越靠前的金属化学性质越活泼,和稀酸溶液反应时表现出来的现象就越剧烈,在等同条件下,反应需要的时间也就越短,再就是得到1克氢气所需要的金属的质量为该金属的相对原子质量化合价;C、根据硫酸和氢氧化钡反应生成硫酸钡沉淀,随着反应的进行沉淀不断增加,当硫酸反应完毕后沉淀不再增加为一定值进行解答;D、根据二氧化碳同时与NaOH和Ca(OH)2发生反应解答.
A、由于是加水稀释碱溶液,因此无论加多少水,溶液仍为碱性溶液,pH值不会小于等于7,故A错误;B、由于在金属活动性顺序中,铝在锌前,因此铝反应需要的时间短,而该图象中时间和斜线的斜率有冲突,应该是斜率越大的,时间越短,金属的活动性越强,故B错误;C、硫酸和氢氧化钡反应生成硫酸钡沉淀,随着反应的进行沉淀不断增加,当硫酸反应完毕后沉淀不再增加为一定值,故C正确;D、二氧化碳同时与NaOH和Ca(OH)2,并且与氢氧化钙反应生成沉淀,所以从开始通二氧化碳时就有沉淀生成,故D错误.故选:C.
点评:
本题难度较大,主要考查了金属活动性顺序的应用、酸碱的有关的化学性质、酸碱溶液的稀释等,培养学生分析问题、解决问题的能力.
看了 下列图象与对应的说法正确的是...的网友还看了以下:
关于离子方程式书写问题离子方程式有没有可能一边是H+,一边是OH-?也就是配电荷守恒时为什么一边加 2020-05-13 …
alcl3水溶液为什么不现碱性Alcl3 加H+得Alo2,加OH-得Al(OH)3,为什么水中不 2020-05-14 …
当pH=2的溶液的pH增加了2个单位时,[H+]和[OH]怎样改变?当pH=13的溶液的pH减少3 2020-05-16 …
醋酸钠加热时C(H)的变化由质子守恒C(H)+C(CH3COOH)=C(OH),又c(CH3COO 2020-05-17 …
为什么氢根不可大于阴离子是2010年正定中学月考的一道题:已知一溶液中有4种离子:X+Y-H+OH 2020-05-22 …
强酸弱碱盐加入水常温下,C(H+)*C(OH-)=10-14次方例如,一溶液H离子浓度为10-5次 2020-05-23 …
水溶液的酸碱性与[H+]和[OH-]的相对大小关系[H+]=[OH-]溶液呈性[H+]>[OH-] 2020-06-22 …
为什么加H+或OH-后,水电离的H+和OH-始终相等.H2OH++OH-,加H+后,不会反应一点O 2020-07-08 …
电极反应中什么时候反应两边加上H+,OH-,H2O?是不是正极反应一般加H+,H2O,负极反应一般加 2020-10-31 …
汉语拼音中的加了“h”的声母和没加“h”的声母读音有什么区别?我实在听不出来有什么区别如题, 2020-11-01 …