早教吧作业答案频道 -->化学-->
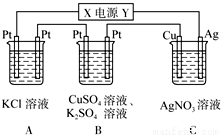
如图所示,若电解5min时,测得铜电极的质量增加2.16g.试回答:(1)电源中X极是(填“正”或“负”)极.(2)通电5min时,B中共收集到224mL(标准状况)气体,溶液体积为200mL(
题目详情
如图所示,若电解5min时,测得铜电极的质量增加2.16g.
试回答:
(1)电源中X极是______(填“正”或“负”)极.
(2)通电5min时,B中共收集到224mL(标准状况)气体,溶液体积为200mL(电解前后溶液的体积变化忽略不计),则通电前c(CuSO 4 )=______.写出B中反应的化学方程式______ 2Cu+O 2 ↑+2H 2 SO 4 ,2H 2 O 2H 2 ↑+O 2 ↑
2H 2 ↑+O 2 ↑
试回答:
(1)电源中X极是______(填“正”或“负”)极.
(2)通电5min时,B中共收集到224mL(标准状况)气体,溶液体积为200mL(电解前后溶液的体积变化忽略不计),则通电前c(CuSO 4 )=______.写出B中反应的化学方程式______ 2Cu+O 2 ↑+2H 2 SO 4 ,2H 2 O
 2H 2 ↑+O 2 ↑
2H 2 ↑+O 2 ↑
▼优质解答
答案和解析
分析:
(1)由铜电极的质量增加,则Cu电极为阴极,可知X为电源的负极;(2)根据电极反应及电子守恒来计算;(3)根据A中的电极反应及与C中转移的电子守恒来计算.
(1)由铜电极的质量增加,发生Ag++e-=Ag,则Cu电极为阴极,可知X为电源的负极,故答案为:负;(2)C中阴极反应为Ag++e-=Ag,n(Ag)==0.02mol,则转移的电子为0.02mol,B中阳极反应为4OH--4e-=2H2O+O2↑,则转移0.02mol电子生成氧气为0.005mol,其体积为0.005mol×22.4L/mol=0.112L=112mL,则在阴极也生成112mL气体,由2H++2e-=H2↑,则氢气的物质的量为0.005mol,该反应转移的电子为0.01mol,则Cu2++2e-=Cu中转移0.01mol电子,所以Cu2+的物质的量为0.005mol,通电前c(CuSO4)==0.025 mol?L-1,B中的反应为2CuSO4+2H2O2Cu+O2↑+2H2SO4,2H2O2H2↑+O2↑,故答案为:0.025 mol?L-1;2CuSO4+2H2O2Cu+O2↑+2H2SO4,2H2O2H2↑+O2↑;(3)由A中发生2KCl+2H2O2KOH+H2↑+Cl2↑~2e-,由电子守恒可知,转移0.02mol电子时生成0.02molKOH,忽略溶液体积的变化,则c(OH-)==0.1mol?L-1,故答案为:0.1mol?L-1.
点评:
本题考查电解原理,明确Cu电极的质量增加是解答本题的突破口,并明确发生的电极反应及电子守恒即可解答,难度不大.
分析:
(1)由铜电极的质量增加,则Cu电极为阴极,可知X为电源的负极;(2)根据电极反应及电子守恒来计算;(3)根据A中的电极反应及与C中转移的电子守恒来计算.
(1)由铜电极的质量增加,发生Ag++e-=Ag,则Cu电极为阴极,可知X为电源的负极,故答案为:负;(2)C中阴极反应为Ag++e-=Ag,n(Ag)==0.02mol,则转移的电子为0.02mol,B中阳极反应为4OH--4e-=2H2O+O2↑,则转移0.02mol电子生成氧气为0.005mol,其体积为0.005mol×22.4L/mol=0.112L=112mL,则在阴极也生成112mL气体,由2H++2e-=H2↑,则氢气的物质的量为0.005mol,该反应转移的电子为0.01mol,则Cu2++2e-=Cu中转移0.01mol电子,所以Cu2+的物质的量为0.005mol,通电前c(CuSO4)==0.025 mol?L-1,B中的反应为2CuSO4+2H2O2Cu+O2↑+2H2SO4,2H2O2H2↑+O2↑,故答案为:0.025 mol?L-1;2CuSO4+2H2O2Cu+O2↑+2H2SO4,2H2O2H2↑+O2↑;(3)由A中发生2KCl+2H2O2KOH+H2↑+Cl2↑~2e-,由电子守恒可知,转移0.02mol电子时生成0.02molKOH,忽略溶液体积的变化,则c(OH-)==0.1mol?L-1,故答案为:0.1mol?L-1.
点评:
本题考查电解原理,明确Cu电极的质量增加是解答本题的突破口,并明确发生的电极反应及电子守恒即可解答,难度不大.
看了 如图所示,若电解5min时,...的网友还看了以下:
共射极固定偏置放大电路由基尔霍夫定律有:集电极电源电压=集电极电流*集电极电阻+集射极电压.无论电 2020-05-17 …
谁告诉我直流有极电源的原理是什么还有有什么元件啊 2020-05-17 …
串联电路两边测电流为何不一样手上有一PCB拼版,每个板是一单独电路,现在把4个PCB板串联接在一起 2020-05-17 …
电动势这一词该怎么理解怎么理解电动势这个概念?定义是:电源力将正电荷从电源负极流回正极.电源力又是 2020-06-22 …
跳闸线圈一般接负极电源.这个负极电源怎么理解? 2020-06-30 …
电源正、负极和公共端接法问题!在一个电路上面只有+电源输入和公共端,这样接电源是不是只要一个正极, 2020-07-06 …
pc电源里有两个共阴二极管做成的三极管,阳端短路,正常吗万用表测量,两边阳极是连通的,正常吗,是这 2020-07-29 …
为什么原电池充电时要电源正极连接电池正极,电源负极连接电池负极?谢谢 2020-07-29 …
用钳流表测得三相五线的电源出线端每根火线的电流都为70A这样,用5小时,如何计算电源共耗电多少?要求 2020-11-11 …
初三物理的计算题有一张图(从电源出发分两路一路经电压表,一路经电阻R2,电流表,开关到分支点一起经电 2020-12-31 …