早教吧作业答案频道 -->化学-->
硼酸(H3BO3)微溶于水,其水溶液显弱酸性,对人体的受伤组织有防腐作用.工业上以硼镁矿(Mg2B2O5•H2O)为原料生产硼酸,同时以硼镁泥为原料制取硫酸镁,可用于印染、造纸、医药等工
题目详情
硼酸(H3BO3)微溶于水,其水溶液显弱酸性,对人体的受伤组织有防腐作用.工业上以硼镁矿(Mg2B2O5•H2O)为原料生产硼酸,同时以硼镁泥为原料制取硫酸镁,可用于印染、造纸、医药等工业.生产工艺流程如下图所示,请回答下列问题:
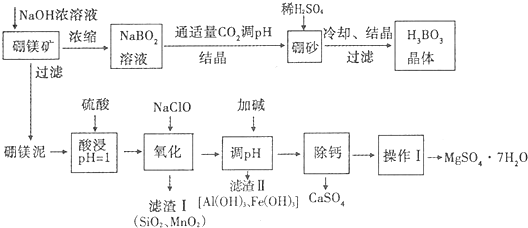
注:
①硼镁泥的主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质.
②硼酸电离平衡常数K=5.8×10-10
③
④已知MgSO4、CaSO4的溶解度如下表:
(1)写出上述流程中生成硼砂(Na2B4O7)的离子方程式___
(2)硼酸根离子可表示为B(OH)4-.写出硼酸电离的方程式___
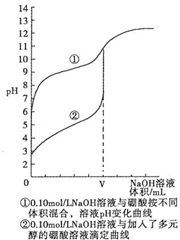
(3)N滴定法测定硼酸晶体的纯度.研究结果表明,用0.1mol•L-1NaOH溶液直接滴定硼酸溶液,滴定过程如曲线①所示,向硼酸溶液中加入多元醇后再滴定如曲线②所示.请分析,能否用强碱直接滴定硼酸溶液,___ (填“能”或“不能”),理由是:___
(4)向硼镁泥酸浸后的溶液中,加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是___.
(5)加碱调节至pH为___时,杂质离子便可完全沉淀.(离子浓度小于或等于1×l0-5mol•L-1时,即可认为该离子沉淀完全)
(6)“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明除钙的操作步骤___、___.

注:
①硼镁泥的主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质.
②硼酸电离平衡常数K=5.8×10-10
③
| 化合物 | Mg(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| Ksp近似值 | 10-11 | 10-16 | 10-38 | 10-33 |
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(2)硼酸根离子可表示为B(OH)4-.写出硼酸电离的方程式___
(3)N滴定法测定硼酸晶体的纯度.研究结果表明,用0.1mol•L-1NaOH溶液直接滴定硼酸溶液,滴定过程如曲线①所示,向硼酸溶液中加入多元醇后再滴定如曲线②所示.请分析,能否用强碱直接滴定硼酸溶液,___ (填“能”或“不能”),理由是:___
(4)向硼镁泥酸浸后的溶液中,加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是___.
(5)加碱调节至pH为___时,杂质离子便可完全沉淀.(离子浓度小于或等于1×l0-5mol•L-1时,即可认为该离子沉淀完全)
(6)“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明除钙的操作步骤___、___.

▼优质解答
答案和解析
硼镁矿加入氢氧化钠浓溶液,过滤分离,硼镁泥用硫酸酸浸,SiO2不反应,再用NaClO将Mg2+氧化生成MnO2沉淀,过滤分离,滤液中含有硫酸镁、硫酸铝、硫酸铁,加入碱调节溶液pH析出氢氧化铝、氢氧化铁沉淀,过滤分离,除钙后,经过蒸发浓缩、冷却结晶、过滤、洗涤得到硫酸镁晶体.NaBO2溶液通入适量二氧化碳气体得到硼砂,常用稀H2SO4调pH得到H3BO3.
(1)NaBO2溶液与二氧化碳反应得到Na2B4O7,二氧化碳起碳酸作用,同时还生成碳酸盐,反应离子方程式为:4BO2-+CO2=B4O72-+CO32-,
故答案为:4BO2-+CO2=B4O72-+CO32-;
(2)H3BO3与水形成配合物后电离出B(OH)4-与H+,电离方程式为:H3BO3+H2O⇌B(OH)4-+H+,
故答案为:H3BO3+H2O⇌B(OH)4-+H+;
(3)没有明显的pH突变区域,无法判断终点,会造成较大的误差,不能用强碱直接滴定硼酸溶液,
故答案为:不能;没有明显的pH突变区域,无法判断终点,会造成较大的误差;
(4)酸性条件下,加入的NaClO可与Mn2+反应产生MnO2沉淀,次氯酸根被还原为氯离子,结合电荷守恒可知有氢离子生成,该反应的离子方程式是:ClO-+Mn2++H2O=MnO2↓+Cl-+2H+,
故答案为:ClO-+Mn2++H2O=MnO2↓+Cl-+2H+;
(5)加入碱调节溶液pH析出氢氧化铝、氢氧化铁沉淀,氢氧化铝的溶度积较大,完全沉淀时碱性较强,铝离子沉淀完全时,溶液中c(OH-)=
mol/L,则溶液pH=-lg
≈4.7,
故答案为:4.7;
(6)硫酸镁与硫酸钙相比,随温度升高,硫酸镁溶解度增大,而硫酸钙溶解度减小,应采取蒸发浓缩结晶出硫酸钙,趁热过滤,减少硫酸镁析出而导致的损失,
故答案为:蒸发浓缩结晶、趁热过滤.
(1)NaBO2溶液与二氧化碳反应得到Na2B4O7,二氧化碳起碳酸作用,同时还生成碳酸盐,反应离子方程式为:4BO2-+CO2=B4O72-+CO32-,
故答案为:4BO2-+CO2=B4O72-+CO32-;
(2)H3BO3与水形成配合物后电离出B(OH)4-与H+,电离方程式为:H3BO3+H2O⇌B(OH)4-+H+,
故答案为:H3BO3+H2O⇌B(OH)4-+H+;
(3)没有明显的pH突变区域,无法判断终点,会造成较大的误差,不能用强碱直接滴定硼酸溶液,
故答案为:不能;没有明显的pH突变区域,无法判断终点,会造成较大的误差;
(4)酸性条件下,加入的NaClO可与Mn2+反应产生MnO2沉淀,次氯酸根被还原为氯离子,结合电荷守恒可知有氢离子生成,该反应的离子方程式是:ClO-+Mn2++H2O=MnO2↓+Cl-+2H+,
故答案为:ClO-+Mn2++H2O=MnO2↓+Cl-+2H+;
(5)加入碱调节溶液pH析出氢氧化铝、氢氧化铁沉淀,氢氧化铝的溶度积较大,完全沉淀时碱性较强,铝离子沉淀完全时,溶液中c(OH-)=
| 3 |
| ||
| 10-14 | |||||
|
故答案为:4.7;
(6)硫酸镁与硫酸钙相比,随温度升高,硫酸镁溶解度增大,而硫酸钙溶解度减小,应采取蒸发浓缩结晶出硫酸钙,趁热过滤,减少硫酸镁析出而导致的损失,
故答案为:蒸发浓缩结晶、趁热过滤.
看了 硼酸(H3BO3)微溶于水,...的网友还看了以下:
根据资料部分列出的“20℃时部分酸、碱、盐的溶解性表”,完成以下任务:OH-Cl-CO32-SO4 2020-04-11 …
在CuO和Fe粉的混合物中,加入一定量的稀硫酸~在CuO和Fe粉的混合物中,加入一定量的稀硫酸,并 2020-05-17 …
关于胶体的题目关于胶体和溶液的区别,下列叙述中正确的是A.溶液成电中性,胶体带有电荷B.通电后,溶 2020-05-23 …
酸碱盐溶解性表是学习化学的重要工具,下表列出了部分酸碱盐在20℃的溶解性.你能利用下表完成下列任务 2020-07-11 …
(2010•新乡一模)酸、碱盐溶解性表示学习化学的重要工具.下表列出了部分酸、碱、盐在20℃时的溶 2020-07-11 …
酸、碱、盐溶解性表是学习化学的重要工具.你表列出m“部分酸、碱、盐在40℃时的溶解性.”O0ˉNO 2020-07-11 …
下列叙述正确的是()A.饱和溶液比不饱和溶液含溶质更多B.与乳化相比,溶解能使物质混合得更均匀C. 2020-07-14 …
根据表格回答:部分酸、碱和盐在水中的溶解性(20℃)部分酸、碱和盐在水中的溶解性(20℃)阴离子阳 2020-07-16 …
下列叙述正确的是()A.与乳化相比,溶解能使物质混合得更均匀B.乳化后形成的乳液与溶液同样稳定C.饱 2020-11-05 …
下列说法正确的是()A.饱和溶液比不饱和溶液含溶质更多B.乳化后形成的乳液与溶液同样稳定C.与乳化相 2020-11-05 …