早教吧作业答案频道 -->化学-->
用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示.(电极材料为石墨)(1)写出用过量的NaOH溶液吸收烟气中的SO2的方程式(2)请
题目详情
用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示.(电极材料为石墨)
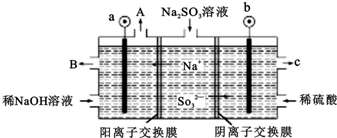
(1)写出用过量的NaOH溶液吸收烟气中的SO2的方程式___
(2)请比较Na2SO3溶液中各离子浓度的大小___
(3)图中a极要连接电源的(填“正”或“负”)___极,C口流出的物质是___.
(4)SO32-放电的电极反应式为___.
(5)电解过程中阴极区碱性明显增强,用平衡移动原理解释原因___.

(1)写出用过量的NaOH溶液吸收烟气中的SO2的方程式___
(2)请比较Na2SO3溶液中各离子浓度的大小___
(3)图中a极要连接电源的(填“正”或“负”)___极,C口流出的物质是___.
(4)SO32-放电的电极反应式为___.
(5)电解过程中阴极区碱性明显增强,用平衡移动原理解释原因___.
▼优质解答
答案和解析
(1)过量的NaOH溶液吸收烟气中的SO2生成正盐亚硫酸钠和水,化学方程式为:2NaOH+SO2=Na2SO3+H2O
故答案为:2NaOH+SO2=Na2SO3+H2O;
(2)Na2SO3水解离子方程式为:SO32-+H2O⇌HSO3-+OH-,钠离子不水解,所以c(Na+)最大,水的电离和亚硫酸根离子水解都生成OH-,所以c(OH-)>c(HSO3-),c(H+) 最小,所以该溶液中离子浓度大小顺序是c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+),
故答案为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+);
(3)图中可知,钠离子移向a极,亚硫酸根离子移向b极,所以b极为阳极,应该接电源的正极,SO32-在阳极失去电子变成SO42-,所以C口流出的物质是H2SO4,
故答案为:负;硫酸;
(4)亚硫酸根离子在阳极失去电子发生氧化反应生成硫酸根离子,电极反应式为:SO32--2e-+H2O=SO42-+2H+;
故答案为:SO32--2e-+H2O=SO42-+2H+;
(5)在阴极H+放电生成H2,c(H+)减小,水的电离平衡H2O⇌H++OH-正向移动,所以碱性增强;
故答案为:水为弱电解质存在H2O⇌H++OH-,在阴极H+放电生成H2,C(H+)减小,水的电离平衡向正向移动,碱性增加.
故答案为:2NaOH+SO2=Na2SO3+H2O;
(2)Na2SO3水解离子方程式为:SO32-+H2O⇌HSO3-+OH-,钠离子不水解,所以c(Na+)最大,水的电离和亚硫酸根离子水解都生成OH-,所以c(OH-)>c(HSO3-),c(H+) 最小,所以该溶液中离子浓度大小顺序是c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+),
故答案为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+);
(3)图中可知,钠离子移向a极,亚硫酸根离子移向b极,所以b极为阳极,应该接电源的正极,SO32-在阳极失去电子变成SO42-,所以C口流出的物质是H2SO4,
故答案为:负;硫酸;
(4)亚硫酸根离子在阳极失去电子发生氧化反应生成硫酸根离子,电极反应式为:SO32--2e-+H2O=SO42-+2H+;
故答案为:SO32--2e-+H2O=SO42-+2H+;
(5)在阴极H+放电生成H2,c(H+)减小,水的电离平衡H2O⇌H++OH-正向移动,所以碱性增强;
故答案为:水为弱电解质存在H2O⇌H++OH-,在阴极H+放电生成H2,C(H+)减小,水的电离平衡向正向移动,碱性增加.
看了 用NaOH溶液吸收烟气中的S...的网友还看了以下:
已知:如图,在平面直角坐标系xOy中,A(4,0),C(0,6),点B在第一象限内,点P从原点O出 2020-05-13 …
O(∩_∩)O哈哈~O(∩_∩)O~(*^__^*)嘻嘻……那个可爱哦?对了撒~大家有一些可爱的网 2020-05-17 …
5.一个机器人从点O出发,每前进1米,就向右转体a°(1<a<180),照这样走下去,如果它恰好能 2020-06-03 …
只蚂蚁从原点O出发,他先向右爬行2个单位长度,到达A点,又向右爬行3个单位长度,到达B点,然后像左 2020-06-06 …
答案已给出,请分析一下.1.(B)Theriverismorethan.A.tenmeterwid 2020-06-10 …
某服装店出售服装,去年按定价的85o/o出售,能获得25o/o的利润.由于今年买入价降低,按同样价 2020-06-14 …
如图所示的四条圆形跑道,每条跑道的长都是1/6千米.A,B,C,D四人同时从交点O出发,分别沿四个 2020-06-22 …
大气臭氧层的反应是:O+O3=2O2△H,该反应的能量变化如图所示,下列叙述中,正确的是()A.O+ 2020-10-31 …
你能猜出这个字吗????请打一字:脱口而出(请打一字)挖空心思(请打一字)纵横交错(请打一字)半推半 2020-11-29 …
已知:如图,在平面直角坐标系xOy中,A(4,0),C(0,6),点B在第一象限内,点P从原点O出发 2020-12-05 …