早教吧作业答案频道 -->化学-->
某金属废料是由Fe、Al、Cu三种金属组成.为测定其中铝的含量,取5.00g样品进行如下实验:请回答:(1)分离A和B的实验操作方法是.(2)向A中通入Cl2,发生反应的离子方程式是.(3)
题目详情
某金属废料是由Fe、Al、Cu三种金属组成.为测定其中铝的含量,取5.00g 样品进行如下实验:
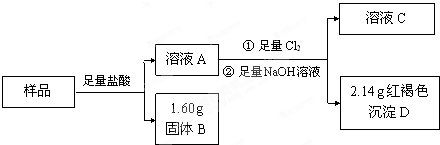
请回答:(1)分离A和B的实验操作方法是___.
(2)向A中通入Cl2,发生反应的离子方程式是.
(3)下列说法正确的是___(填字母).
a.实验中可以用硝酸代替盐酸
b.向A中滴加KSCN溶液,溶液变成红色
c.D受热失水生成的物质常用作红色油漆
(4)金属废料中铝的质量分数为___.

请回答:(1)分离A和B的实验操作方法是___.
(2)向A中通入Cl2,发生反应的离子方程式是.
(3)下列说法正确的是___(填字母).
a.实验中可以用硝酸代替盐酸
b.向A中滴加KSCN溶液,溶液变成红色
c.D受热失水生成的物质常用作红色油漆
(4)金属废料中铝的质量分数为___.
▼优质解答
答案和解析
(1)B为固体,A为液体,分离固液混合物的操作为过滤,故答案为:过滤;
(2)氯气具有氧化性,可把亚铁离子氧化成铁离子,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故答案为:2Fe2++Cl2═2Fe3++2Cl-;
(3)a.硝酸也能和铜反应,无法测定铜和铁的质量,故a错误;
b.盐酸和铁反应生成氯化亚铁和氢气,氯化亚铁和硫氰化钾混合无现象,故b错误;
c.氢氧化铁分解为氧化铁,为红棕色固体,常用作红色染料,故c正确;
故答案为:c;
(4)根据铜和盐酸不反应,可知B为铜,质量为1.60g,D为氢氧化铁沉淀,质量为:2.14g,物质的量为:
-=0.02mol,故铁的质量为:0.02mol×56g/mol=1.12g,铝的质量为:5.00g-1.60g-1.12g=2.28g,铝的质量分数为:
×100%=45.6%,故答案为:45.6%.
(2)氯气具有氧化性,可把亚铁离子氧化成铁离子,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故答案为:2Fe2++Cl2═2Fe3++2Cl-;
(3)a.硝酸也能和铜反应,无法测定铜和铁的质量,故a错误;
b.盐酸和铁反应生成氯化亚铁和氢气,氯化亚铁和硫氰化钾混合无现象,故b错误;
c.氢氧化铁分解为氧化铁,为红棕色固体,常用作红色染料,故c正确;
故答案为:c;
(4)根据铜和盐酸不反应,可知B为铜,质量为1.60g,D为氢氧化铁沉淀,质量为:2.14g,物质的量为:
| 2.14g |
| 107g/mol |
| 2.28g |
| 5.00g |
看了 某金属废料是由Fe、Al、C...的网友还看了以下:
在RT三角形ABC中是否存在相似的三角形在Rt△ABC中,∠BAC=90°,AD是斜边上的高,∠AB 2020-03-30 …
你智商高吗,高你就进来1,下列所给的方程组中,是二元一次方程组的是()3x+2y=72x+y=13分 2020-03-31 …
下列方程组中,是二元一次方程组的是?A.xy=1x-y=-3B.2x-3y=13x+2y=5C.x 2020-04-27 …
remindsbthat......中的从句是什么从句我们老师说是宾语从句,但是这个从句在整个词组 2020-05-13 …
将下列词组中是可数名词的选出来,①animal②rubbish③map④article⑤air⑥w 2020-05-22 …
●文法G=({E},{+,*,(,),a},P,E),其中P由下列产生式组成E->E+E|E*E|( 2020-05-25 …
文法G=({E},{+,*,(,),a},P,E),其中P由下列产生式组成E->E+E|E*E|(E 2020-05-26 …
有A、B、C、D、E、F共6个队进行小组单循环足球赛,小组前两名的队出线,[1]每队进行场比赛,小 2020-06-06 …
下列分组中()是按数量标志分组。A.工人按产量分组B.人口按民族分组C.职工按工龄分组D.企业按所有 2020-06-07 …
下列四组词中,都是同义词的一组中是()a.美好美丽美化秀美b.热爱热情热烈热忱c.神奇神秘神妙奇妙 2020-07-03 …