早教吧作业答案频道 -->化学-->
氧化还原反应在生产生活中有着重要的应用.请按要求写出相应的方程式.(1)将含SO2的废气通入含Fe2+(催化剂)的溶液中,常温下可使SO2转化为SO24-,其总反应为2SO2+O2+2H2O=2H2SO4.上述总
题目详情
氧化还原反应在生产生活中有着重要的应用.请按要求写出相应的方程式.
(1)将含SO2的废气通入含Fe2+(催化剂)的溶液中,常温下可使SO2转化为SO24-,其总反应为2SO2+O2+2H2O=2H2SO4.上述总反应分两步进行,第一步反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,写出第二步反应的离子方程式:___.
(2)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液.若溶液的pH偏高,则碱式硫酸铝产率降低且有气泡产生,用化学方程式表示其原因:___.
(3)ClO2是一种高效安全的杀菌消毒剂.氯化钠电解法生产ClO2工艺原理示意图如下:
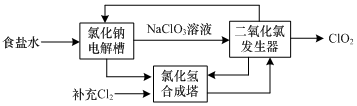
①写出氯化钠电解槽内发生反应的离子方程式:___.
②写出ClO2发生器中的化学方程式,并标出电子转移的方向及数目:___.
③ClO2能将电镀废水中的CN-离子氧化成两种无毒气体,自身被还原成Cl-.写出该反应的离子方程式___.
(1)将含SO2的废气通入含Fe2+(催化剂)的溶液中,常温下可使SO2转化为SO24-,其总反应为2SO2+O2+2H2O=2H2SO4.上述总反应分两步进行,第一步反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,写出第二步反应的离子方程式:___.
(2)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液.若溶液的pH偏高,则碱式硫酸铝产率降低且有气泡产生,用化学方程式表示其原因:___.
(3)ClO2是一种高效安全的杀菌消毒剂.氯化钠电解法生产ClO2工艺原理示意图如下:

①写出氯化钠电解槽内发生反应的离子方程式:___.
②写出ClO2发生器中的化学方程式,并标出电子转移的方向及数目:___.
③ClO2能将电镀废水中的CN-离子氧化成两种无毒气体,自身被还原成Cl-.写出该反应的离子方程式___.
▼优质解答
答案和解析
(1)根据题中反应原理,第一步反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,第二步是铁离子将二氧化硫氧化成硫酸根离子,反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO4 2-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO4 2-+4H+;
(2)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,若溶液的pH偏高,溶液碱性增强,铝离子与碳酸根离子双水解生成氢氧化铝和二氧化碳,反应的化学方程式为3CaCO3+Al2(SO4)3+3H2O=2Al(OH)3↓+3CaSO4↓+3CO2↑,
故答案为:3CaCO3+Al2(SO4)3+3H2O=2Al(OH)3↓+3CaSO4↓+3CO2↑;
(3)根据流程图可知道:食盐水在特定条件下电解得到氯酸钠(NaClO3),NaClO3和HCl反应,生成ClO2,可以写出方程式,并用化合价升降法配平得到,ClO2能将电镀废水中的CN-离子氧化成两种无毒气体,应为二氧化碳和氮气,自身被还原成Cl-,根据电荷守恒和元素守恒写出该反应的离子方程式,
①电解食盐水得到氯酸钠(NaClO3)和H2,电解的离子反应方程式为:Cl-+3H2O
ClO3-+3H2↑,故答案为:Cl-+3H2O
ClO3-+3H2↑;
②ClO2发生器中的反应为,化学方程式NaClO3和盐酸发生歧化反应,生成NaCl、ClO2、Cl2、H2O,用化学方程式表示并标出电子转移的方向及数目为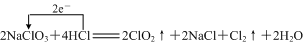 ,
,
故答案为: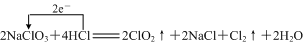 ;
;
③ClO2能将电镀废水中的CN-离子氧化成两种无毒气体,应为二氧化碳和氮气,自身被还原成Cl-,反应的离子方程式为 2ClO2+2CN-=2CO2↑+2Cl-+N2↑,
故答案为:2ClO2+2CN-=2CO2↑+2Cl-+N2↑.
故答案为:2Fe3++SO2+2H2O=2Fe2++SO4 2-+4H+;
(2)pH=3.6时,碳酸钙与硫酸铝反应可制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,若溶液的pH偏高,溶液碱性增强,铝离子与碳酸根离子双水解生成氢氧化铝和二氧化碳,反应的化学方程式为3CaCO3+Al2(SO4)3+3H2O=2Al(OH)3↓+3CaSO4↓+3CO2↑,
故答案为:3CaCO3+Al2(SO4)3+3H2O=2Al(OH)3↓+3CaSO4↓+3CO2↑;
(3)根据流程图可知道:食盐水在特定条件下电解得到氯酸钠(NaClO3),NaClO3和HCl反应,生成ClO2,可以写出方程式,并用化合价升降法配平得到,ClO2能将电镀废水中的CN-离子氧化成两种无毒气体,应为二氧化碳和氮气,自身被还原成Cl-,根据电荷守恒和元素守恒写出该反应的离子方程式,
①电解食盐水得到氯酸钠(NaClO3)和H2,电解的离子反应方程式为:Cl-+3H2O
| ||
| ||
②ClO2发生器中的反应为,化学方程式NaClO3和盐酸发生歧化反应,生成NaCl、ClO2、Cl2、H2O,用化学方程式表示并标出电子转移的方向及数目为
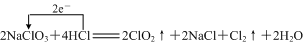 ,
,故答案为:
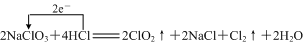 ;
;③ClO2能将电镀废水中的CN-离子氧化成两种无毒气体,应为二氧化碳和氮气,自身被还原成Cl-,反应的离子方程式为 2ClO2+2CN-=2CO2↑+2Cl-+N2↑,
故答案为:2ClO2+2CN-=2CO2↑+2Cl-+N2↑.
看了 氧化还原反应在生产生活中有着...的网友还看了以下:
分别在5根试管里放5枚洁净午休铁钉管1加稀硫酸浸没铁钉倒去液,2中加氯化钠溶液浸没铁钉一半3加少蒸 2020-05-14 …
状语从句翻译2个10分1.Shedidtheworkashewastold2.Hespokeasi 2020-05-17 …
“资料2”中,为证实乙公司是否存在未入账的应付账款,审计人员可使用的方法有: A.抽查应付账款 2020-05-21 …
“资料2”中,为了证实货币资金收支截止期的正确性,审计人员应重点审查的收付款业务期间是: A. 2020-05-21 …
在事件2中,为什么D承建单位联合体被认定不符合投标资格? 2020-05-26 …
例句1:Howdoyoustudyforatese?例句2:Whataboutreadingalo 2020-06-04 …
(x+y)^2中为什么x^2+y^2≥2xy 2020-06-08 …
已知当物体的密度和液体的密度相同的情况下,物体就能悬浮在液体中,为了使540g的空心吕球能悬浮在水 2020-07-02 …
关於蒸馏实验的问题蒸馏中放蒸馏液的试管上面驳著一条滴著蒸馏液的管子,为什麽那个管子不能插入蒸馏液中 2020-07-05 …
请问〔Mn(CO)4(μ2-Cl)〕2中,为什么不存在金属键?其中μ2中的下标2表示什么意思呢? 2020-07-07 …