早教吧作业答案频道 -->化学-->
苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是C8H10(g)⇌C8H8(g)+H2(g)△H>0Ⅰ.某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内物质
题目详情
苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是C8H10(g)⇌C8H8(g)+H2(g)△H>0
Ⅰ.某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内物质的量,得到数据如下表:
(1)当反应进行到20min时,该段时间内H2的平均反应速率是___.
(2)该温度下,该反应的化学平衡常数是___.
(3)已知:
计算上述反应的△H=___ kJ•mol-1.若保持其他条件不变,用0.40mol H2(g)和0.40mol C8H8(g)合成C8H10(g),当有30kJ热量放出时,该反应中H2的转化率是___.此时,该反应是否达到了平衡状态?___(填“是”或“否”).
Ⅱ.工业上以高温水蒸气作为反应体系的稀释剂(不参与反应),C8H10(g)的平衡转化率与水蒸气的用量、体系的温度、压强的关系如图Ⅰ、图Ⅱ所示.
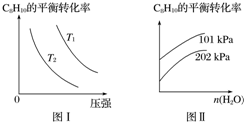
(4)由图Ⅰ可知,T1___T2(填“大于”、“小于”或“等于”).
(5)由图Ⅱ可知,当其他条件不变时,水蒸气的用量越大,C8H10的平衡转化率将___(填“越大”、“越小”或“不变”),原因是___.
Ⅰ.某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内物质的量,得到数据如下表:
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2[来源:] | n3 |
| n(C8H8)/mol | 0.00 | 0.10 | n1 | 0.16 | 0.16 |
(2)该温度下,该反应的化学平衡常数是___.
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•mol‾1 | 412.5 | 348 | 612 | 436 |
计算上述反应的△H=___ kJ•mol-1.若保持其他条件不变,用0.40mol H2(g)和0.40mol C8H8(g)合成C8H10(g),当有30kJ热量放出时,该反应中H2的转化率是___.此时,该反应是否达到了平衡状态?___(填“是”或“否”).
Ⅱ.工业上以高温水蒸气作为反应体系的稀释剂(不参与反应),C8H10(g)的平衡转化率与水蒸气的用量、体系的温度、压强的关系如图Ⅰ、图Ⅱ所示.

(4)由图Ⅰ可知,T1___T2(填“大于”、“小于”或“等于”).
(5)由图Ⅱ可知,当其他条件不变时,水蒸气的用量越大,C8H10的平衡转化率将___(填“越大”、“越小”或“不变”),原因是___.
▼优质解答
答案和解析
I.(1)将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,20min后,剩余0.26mol,减少了0.14mol,
C8H10(g)⇌C8H8(g)+H2(g)
起始(mol) 0.40 0 0
变化(mol) 0.14 0.14 0.14
20min(mol) 0.26 0.14 0.14
v(H2)=
=0.0035mol/(L•min)
故答案为:0.0035mol/(L•min);
(2)C8H10(g)⇌C8H8(g)+H2(g)
起始(mol/L) 0.20 0 0
变化(mol/L) 0.08 0.08 0.08
30min(mol/L) 0.12 0.08 0.08
化学平衡常数K=
=
=0.053;
故答案为:0.053;
(3)C8H10(g)⇌C8H8(g)+H2(g),反应焓变△H=反应物键能总和-生成物键能总和=10×412.5+4×348+3×612-8×412.5-3×348-4×612-436=125KJ/mol,
根据C8H10(g)⇌C8H8(g)+H2(g)△H=125kJ•mol-1,可知 C8H8(g)+H2(g)⇌C8H10(g)△H=-125kJ•mol-1,有30kJ热量放出时,消耗的H2量为0.24mol,所以氢气转化率=
×100%=
×100%=60%;
根据(2)知:平衡常数=0.053,则C8H8(g)+H2(g)⇌C8H10(g)的平衡常数为
=18.75,
C8H8(g)+H2(g)⇌C8H10(g)
起始(mol/L) 0.2 0.2 0
变化(mol/L) 0.12 0.12 0.12
某时刻(mol/L) 0.08 0.08 0.12
=
=18.75=18.75,反应达到平衡状态;
故答案为:125;60%;是;
Ⅱ.(4)C8H10(g)⇌C8H8(g)+H2(g)△H=125kJ•mol-1,温度升高,平衡正向移动,C8H10的转化率增大,由图I可知,压强相同时,T1时C8H10的转化率大于T2时C8H10的转化率,故T1大于T2;
故答案为:大于;
(5)其他条件不变,水蒸气的用量越大,容器的体积越大,相当于减小了原体系的压强,平衡正向移动,转化率增大;
故答案为:越大;水蒸气的用量越大,容器的体积越大,相当于减小了原体系的压强,平衡正向移动,转化率增大.
C8H10(g)⇌C8H8(g)+H2(g)
起始(mol) 0.40 0 0
变化(mol) 0.14 0.14 0.14
20min(mol) 0.26 0.14 0.14
v(H2)=
| ||
| 20min |
故答案为:0.0035mol/(L•min);
(2)C8H10(g)⇌C8H8(g)+H2(g)
起始(mol/L) 0.20 0 0
变化(mol/L) 0.08 0.08 0.08
30min(mol/L) 0.12 0.08 0.08
化学平衡常数K=
| c(C8H8)c(H2) |
| c(C8H10) |
| 0.08×0.08 |
| 0.12 |
故答案为:0.053;
(3)C8H10(g)⇌C8H8(g)+H2(g),反应焓变△H=反应物键能总和-生成物键能总和=10×412.5+4×348+3×612-8×412.5-3×348-4×612-436=125KJ/mol,
根据C8H10(g)⇌C8H8(g)+H2(g)△H=125kJ•mol-1,可知 C8H8(g)+H2(g)⇌C8H10(g)△H=-125kJ•mol-1,有30kJ热量放出时,消耗的H2量为0.24mol,所以氢气转化率=
| 消耗量 |
| 起始量 |
| 0.24mol |
| 0.4mol |
根据(2)知:平衡常数=0.053,则C8H8(g)+H2(g)⇌C8H10(g)的平衡常数为
| 1 |
| 0.053 |
C8H8(g)+H2(g)⇌C8H10(g)
起始(mol/L) 0.2 0.2 0
变化(mol/L) 0.12 0.12 0.12
某时刻(mol/L) 0.08 0.08 0.12
| c(C8H10) |
| c(C8H8)c(H2) |
| 0.12 |
| 0.08×0.08 |
故答案为:125;60%;是;
Ⅱ.(4)C8H10(g)⇌C8H8(g)+H2(g)△H=125kJ•mol-1,温度升高,平衡正向移动,C8H10的转化率增大,由图I可知,压强相同时,T1时C8H10的转化率大于T2时C8H10的转化率,故T1大于T2;
故答案为:大于;
(5)其他条件不变,水蒸气的用量越大,容器的体积越大,相当于减小了原体系的压强,平衡正向移动,转化率增大;
故答案为:越大;水蒸气的用量越大,容器的体积越大,相当于减小了原体系的压强,平衡正向移动,转化率增大.
看了 苯乙烷(C8H10)可生产塑...的网友还看了以下:
关于L-型单糖的哈斯沃式如何把L-单糖的直立环形费歇尔投影式转为平面环形的哈斯沃式?D-的是最右边 2020-05-13 …
下列关于细菌和真菌的叙述中,错误的是()A.细菌的细胞没有成形的细胞核,真菌的细胞有成形的细胞核B 2020-05-14 …
真空管道抽真空1.3×10-4Pa.L/S.现在想降低点真空度,数值要怎么写啊.1.3×10-4P 2020-05-21 …
请问这里有哪一个基督教徒,绕了一圈回来,走入山高水深,最后才发现生命或生活的真缔,而这真缔是什么? 2020-07-06 …
下列有关细菌和真菌的叙述正确的是()A.细菌没有成形的细胞核,缺少遗传物质B.两者都属于单细胞生物, 2020-10-31 …
关于原核生物与真核细胞?缺少隔膜的是原核生物还是真核细胞?无核子的是原核生物还是真核细胞?单细胞或者 2020-11-01 …
题:粉状化合物A和粉状单质B在一定条件下反应生成单质C,和化合物D.C加稀酸L生成单质F和溶液E,溶 2020-11-22 …
比较细菌和真菌,下列判断正确的是()A.细菌都是单细胞生物,真菌都是多细胞生物B.细菌都营寄生生活, 2020-12-25 …
真空管道抽真空1.3×10-4Pa.L/S。。现在想降低点真空度,数值要怎么写啊。1.3×10-4P 2020-12-31 …
下列说法中正确的是()A.细菌和真菌对人类一般都是有害的B.酵母菌和霉菌都属于真菌C.细菌是单细胞生 2021-02-13 …