早教吧作业答案频道 -->化学-->
Ⅰ.在气态二氯化铍中有单体BeCl2和二聚体(BeCl2)2;在晶体中变形成多聚体,试画出各种存在形式的结构简图,并指出铍原子的杂化轨道类型.单体BeCl2二聚体(BeCl2)2多聚体
题目详情
Ⅰ.在气态二氯化铍中有单体BeCl2和二聚体(BeCl2)2;在晶体中变形成多聚体,试画出各种存在形式的结构简图,并指出铍原子的杂化轨道类型.
单体BeCl2 二聚体(BeCl2)2 多聚体(BeCl2)N
结构简图:_________
杂化轨道类型:_________
Ⅱ.Ti、Cr、Fe是周期表中1~36号元素.请回答问题:
(1)它们同属于周期表___区,___周期元素;
(2)其原子结构中单电子数最多的元素名称是___;
(3)写出基态Fe3+M层的电子排布式:___;铁的配合物Fe(CO).中心原子价电子数与配体提供的电子数之和为18,则n为___;
(4)钛被誉为“未来世纪金属”
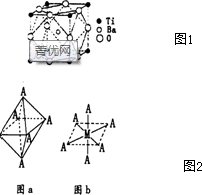
①钛的+4价化合物偏钛酸钡,其热稳定性好,介电常数高,在小型变电器,话筒和扩音器中广泛应用,偏钛酸钡晶体中晶胞的结构示意图如图1所示,它的化学式为___,其中Ti4+的氧配位数为___.
②常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,推断TiCl4属于___晶体;
③一种Ti2+的配合物Ti(NH3)4 Cl2,其空间构型如图2a所示(正八面体),也可用图b表示(M为中心原子,A为配体);Ti2+的该配合物有___种结构.
单体BeCl2 二聚体(BeCl2)2 多聚体(BeCl2)N
结构简图:_________
杂化轨道类型:_________
Ⅱ.Ti、Cr、Fe是周期表中1~36号元素.请回答问题:
(1)它们同属于周期表___区,___周期元素;
(2)其原子结构中单电子数最多的元素名称是___;
(3)写出基态Fe3+M层的电子排布式:___;铁的配合物Fe(CO).中心原子价电子数与配体提供的电子数之和为18,则n为___;
(4)钛被誉为“未来世纪金属”
①钛的+4价化合物偏钛酸钡,其热稳定性好,介电常数高,在小型变电器,话筒和扩音器中广泛应用,偏钛酸钡晶体中晶胞的结构示意图如图1所示,它的化学式为___,其中Ti4+的氧配位数为___.
②常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,推断TiCl4属于___晶体;
③一种Ti2+的配合物Ti(NH3)4 Cl2,其空间构型如图2a所示(正八面体),也可用图b表示(M为中心原子,A为配体);Ti2+的该配合物有___种结构.

▼优质解答
答案和解析
Ⅰ.BeCl2中Be原子成2个Be-Cl,单体BeCl2 结构简图为Cl-Be-Cl,Be原子的杂化轨道数为2,故Be原子采取sp杂化方式,二聚体为氯的孤电子对提供给铍,所以(BeCl2)2 结构简图为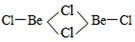 ,杂化轨道数为3,所以碳原子采取sp2杂化; 铍具有空轨道,氯具有孤电子对,所以多聚体(BeCl2)N结构简图为
,杂化轨道数为3,所以碳原子采取sp2杂化; 铍具有空轨道,氯具有孤电子对,所以多聚体(BeCl2)N结构简图为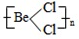 中价层电子对个数=4,中心原子是以sp3杂化;
中价层电子对个数=4,中心原子是以sp3杂化;
故答案为:Cl-Be-Cl;sp杂化; ;Sp2杂化;
;Sp2杂化;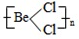 ; Sp3杂化;
; Sp3杂化;
Ⅱ.(1)Ti的原子序数为22,电子排布为1s22s22p63s23p63d24s2,位于第四周期第ⅣB族,最后填充d电子,为d区元素,
Cr的原子序数为24,电子排布为1s22s22p63s23p63d54s1,位于第四周期第ⅥB族,最后填充d电子,为d区元素,
Fe的电子排布式为1s22s22p63s23p63d64s2,位于第四周期第ⅥⅡ族,最后填充d电子,为d区元素,
故答案为:d;四;
(2)Ti的原子序数为22,电子排布为1s22s22p63s23p63d24s2,未成对电子数是2;
24Cr元素为24号元素,其核外电子排布式为:1s22s22p63s23p63d54s1,未成对电子数是6;
Fe的电子排布式为1s22s22p63s23p63d64s2,未成对电子数为4;所以原子结构中单电子数最多的元素为铬,
故答案为:铬;
(3)Fe原子核外有26个电子,核外电子排布为1s22s22p63s23p63d64s2,Fe原子失去4s能级2个电子、3d能级1个电子形成Fe3+,Fe3+电子排布式为1s22s22p63s23p63d5,则M层电子排布式为:3s23p63d5,配合物Fe(CO)x的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,8+2x=18,x=5,
故答案为:3s23p63d5;5;
(4)①由晶胞结构示意图可知,Ba在立方体的中心,完全属于该晶胞;Ti处于立方体的8个顶点,每个Ti有
属于该晶胞;O处于立方体的12条棱的中点,每个O有
属于该晶胞.即晶体中N(Ba):N(Ti):N(O)=1:(8×
):(12×
)=1:1:3,所以化学式为:BaTiO3,
在晶胞中与钛离子距离最近的是氧原子,分布在与钛相连的棱边的中点上,而与一个钛相连的边有六个,所以钛的配位数为6,
故答案为:BaTiO3; 6;
②常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,熔沸点较低,晶体由分子形成,属于分子晶体;
故答案为:分子;
③Ti2+位于正八面体的中心,NH3和Cl-位于正八面体顶点,当两个Cl-相邻时为一种结构,两个Cl-不相邻时为另一种结构,即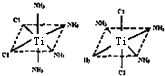 ,共有两种结构,
,共有两种结构,
故答案为:2.
 ,杂化轨道数为3,所以碳原子采取sp2杂化; 铍具有空轨道,氯具有孤电子对,所以多聚体(BeCl2)N结构简图为
,杂化轨道数为3,所以碳原子采取sp2杂化; 铍具有空轨道,氯具有孤电子对,所以多聚体(BeCl2)N结构简图为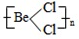 中价层电子对个数=4,中心原子是以sp3杂化;
中价层电子对个数=4,中心原子是以sp3杂化;故答案为:Cl-Be-Cl;sp杂化;
 ;Sp2杂化;
;Sp2杂化;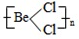 ; Sp3杂化;
; Sp3杂化;Ⅱ.(1)Ti的原子序数为22,电子排布为1s22s22p63s23p63d24s2,位于第四周期第ⅣB族,最后填充d电子,为d区元素,
Cr的原子序数为24,电子排布为1s22s22p63s23p63d54s1,位于第四周期第ⅥB族,最后填充d电子,为d区元素,
Fe的电子排布式为1s22s22p63s23p63d64s2,位于第四周期第ⅥⅡ族,最后填充d电子,为d区元素,
故答案为:d;四;
(2)Ti的原子序数为22,电子排布为1s22s22p63s23p63d24s2,未成对电子数是2;
24Cr元素为24号元素,其核外电子排布式为:1s22s22p63s23p63d54s1,未成对电子数是6;
Fe的电子排布式为1s22s22p63s23p63d64s2,未成对电子数为4;所以原子结构中单电子数最多的元素为铬,
故答案为:铬;
(3)Fe原子核外有26个电子,核外电子排布为1s22s22p63s23p63d64s2,Fe原子失去4s能级2个电子、3d能级1个电子形成Fe3+,Fe3+电子排布式为1s22s22p63s23p63d5,则M层电子排布式为:3s23p63d5,配合物Fe(CO)x的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,8+2x=18,x=5,
故答案为:3s23p63d5;5;
(4)①由晶胞结构示意图可知,Ba在立方体的中心,完全属于该晶胞;Ti处于立方体的8个顶点,每个Ti有
| 1 |
| 8 |
| 1 |
| 4 |
| 1 |
| 8 |
| 1 |
| 4 |
在晶胞中与钛离子距离最近的是氧原子,分布在与钛相连的棱边的中点上,而与一个钛相连的边有六个,所以钛的配位数为6,
故答案为:BaTiO3; 6;
②常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,熔沸点较低,晶体由分子形成,属于分子晶体;
故答案为:分子;
③Ti2+位于正八面体的中心,NH3和Cl-位于正八面体顶点,当两个Cl-相邻时为一种结构,两个Cl-不相邻时为另一种结构,即
 ,共有两种结构,
,共有两种结构,故答案为:2.
看了 Ⅰ.在气态二氯化铍中有单体B...的网友还看了以下:
一定质量的气体,在体积不变时,温度由50℃加热到100℃,气体的压强变化情况是[]A.气体的压强是 2020-04-08 …
气体能量2个容器A体积VA,与容器B相连,B体积VB,大气压强P,常数R,温度为T,求2容器内全部 2020-05-13 …
.将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(气 2020-05-14 …
一只钢瓶内储有压缩气体,气体的密度为ρ,若从瓶中放出一般质量的气体,则瓶内剩余气体的密度将 ()A 2020-05-16 …
汽缸中的气体膨胀时推汽缸中的气体膨胀时推动活塞向外运动,若气体对活塞做的功是2.6×103J,气体 2020-05-17 …
1.同温同压下,某集气瓶充满O2时为116g,充满CO2时为122g,充满气体A时质量为114g, 2020-06-05 …
某非金属单质A和氧气发生化合反应生成B,B为气体,其体积是反应掉的氧气体积的两倍(同温同压).以下 2020-06-25 …
一定质量的理想气体,从状态A经过状态B变化到状态C,如图所示,图中BC是平行于横轴的直线,已知气体 2020-07-30 …
如图,可自由移动的活塞将密闭气缸分为体积相等的上下两部分A和B,初始时A、B中密封的理想气体温度均为 2020-11-03 …
(2010•鸡西模拟)点燃H2,O2,N2的混合体气体20克,完全反应后生成18克水,则剩余气体不可 2020-11-11 …