早教吧作业答案频道 -->化学-->
硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4•7H2O的工艺流
题目详情
硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4•7H2O的工艺流程如下:
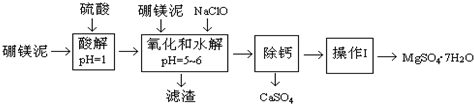
已知:NaClO与Mn2+反应产生MnO2沉淀.
根据题意回答下列问题:
(1)实验中需用1.00mol/L的硫酸80.0mL,若用98%的浓硫酸来配制,除量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器有___、___.
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3外,还有___、___.
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式:___.
在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为:___.
(4)为了检验滤液中Fe3+是否被除尽,可选用的试剂是___.
A.KSCN溶液 B.淀粉KI溶液 C.H2O2 D.KMnO4稀溶液
(5)已知MgSO4、CaSO4的溶解度如下表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤___、___.
(6)如果测得提供的硼镁泥的质量为100.0g,得到的MgSO4•7H2O196.8g,则MgSO4•7H2O的产率为___(相对分子质量:MgSO4•7H2O-246 MgO-40).

已知:NaClO与Mn2+反应产生MnO2沉淀.
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 2.3 | 4.0 | 7.6 |
| 完全沉淀pH | 4.1 | 5.2 | 9.6 |
(1)实验中需用1.00mol/L的硫酸80.0mL,若用98%的浓硫酸来配制,除量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器有___、___.
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3外,还有___、___.
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式:___.
在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为:___.
(4)为了检验滤液中Fe3+是否被除尽,可选用的试剂是___.
A.KSCN溶液 B.淀粉KI溶液 C.H2O2 D.KMnO4稀溶液
(5)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(6)如果测得提供的硼镁泥的质量为100.0g,得到的MgSO4•7H2O196.8g,则MgSO4•7H2O的产率为___(相对分子质量:MgSO4•7H2O-246 MgO-40).
▼优质解答
答案和解析
(1)用98%的浓硫酸来配制1.00mol/L的硫酸80.0mL,应选择100ml容量瓶,一般步骤为:计算、量取、稀释、移液、洗涤、定容、摇匀等,用到的仪器有:量筒、胶头滴管、烧杯、玻璃棒、100ml容量瓶,
还需要的玻璃仪器:烧杯、100mL容量瓶;
故答案为:烧杯、100mL容量瓶;
(2)二氧化锰和二氧化硅不与稀硫酸反应,所以滤渣中还含有MnO2,SiO2;
故答案为:MnO2,SiO2;
(3)NaClO溶液在加热条件下将溶液中的Mn2+氧化成MnO2,反应的离子方程式为Mn2++ClO-+H2O=MnO2↓+2H++Cl-,溶液中含有Fe2+,具有还原性,可与NaClO发生氧化还原反应,反应的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H2O,
故答案为:Mn2++ClO-+H2O═MnO2↓+2H++Cl-;2Fe2++ClO-+2H+═2Fe3++Cl-+H2O;
(4)三价铁离子遇到KSCN溶液显血红色,通常利用KSCN溶液检验三价铁离子的存在,故选:A;
(5)有温度对硫酸镁、硫酸钙的溶解度影响,温度越高,硫酸钙溶解度越小,可以采用蒸发浓缩,趁热过滤方法除去硫酸钙;
故答案为:蒸发浓缩,趁热过滤;
(6)100g硼镁泥中氧化镁的物质的量为:
=1mol,根据镁原子守恒,生成MgSO4•7H2O的物质的量为1mol,质量为246g/mol×1mol=246g,MgSO4•7H2O的产率为:
×100%=80.0%,
故答案为:80.0%.
还需要的玻璃仪器:烧杯、100mL容量瓶;
故答案为:烧杯、100mL容量瓶;
(2)二氧化锰和二氧化硅不与稀硫酸反应,所以滤渣中还含有MnO2,SiO2;
故答案为:MnO2,SiO2;
(3)NaClO溶液在加热条件下将溶液中的Mn2+氧化成MnO2,反应的离子方程式为Mn2++ClO-+H2O=MnO2↓+2H++Cl-,溶液中含有Fe2+,具有还原性,可与NaClO发生氧化还原反应,反应的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H2O,
故答案为:Mn2++ClO-+H2O═MnO2↓+2H++Cl-;2Fe2++ClO-+2H+═2Fe3++Cl-+H2O;
(4)三价铁离子遇到KSCN溶液显血红色,通常利用KSCN溶液检验三价铁离子的存在,故选:A;
(5)有温度对硫酸镁、硫酸钙的溶解度影响,温度越高,硫酸钙溶解度越小,可以采用蒸发浓缩,趁热过滤方法除去硫酸钙;
故答案为:蒸发浓缩,趁热过滤;
(6)100g硼镁泥中氧化镁的物质的量为:
| 100g×40% |
| 40g/mol |
| 196.2g |
| 246g |
故答案为:80.0%.
看了 硼镁泥是一种工业废料,主要成...的网友还看了以下:
对于复数Z1=m(m-1﹚﹢﹙m-﹚i,Z2=﹙m+1﹚﹢﹙m-1﹚i,﹙m∈R﹚大神们帮帮忙对于 2020-04-26 …
C语言问题关于素数voidnum(intm,intk,intxx[]){intdata=m+1;i 2020-05-17 …
inti,j,k,l,m,n;floatx,y,z,w;i=8;j=5;k=-5;x=5;l=i% 2020-06-05 …
谁能帮我看下这个程序问题出在哪?function[variancebsbkbnsigma]=tra 2020-06-21 …
matlab 得到一个矩阵M(:,:),能否执行语句的条件是M中从小到大的数的排列:M(i,j)从 2020-06-27 …
三道C语言题,请高手指点第一道:#includedoublef(intn){inti;double 2020-07-23 …
C语言求鞍点,哪里错了#include<stdio.h>intmain(){inti,j,k,ma 2020-07-23 …
英语翻译一:A=imread('图像.bmp');I=double(A);[m,n]=size(I) 2020-11-01 …
(口ivi•揭阳一模)已知复数zv=si下口x+λi,z口=m+(m−3cos口x)i(λ,m,x∈ 2020-11-12 …
用matlab解一下这个微分方程!急.di/dt=(480*m+15*n+20*k*i)*(1+a- 2020-12-12 …