早教吧作业答案频道 -->化学-->
砷(33As)在元素周期表中与氮同主族,砷及其化合物被运用在农药、防腐剂、染料和医药等领域,及其多种合金中.(1)砷原子次外层上的电子数为,砷化氢的电子式为.(2)成语“
题目详情
砷(33As)在元素周期表中与氮同主族,砷及其化合物被运用在农药、防腐剂、染料和医药等领域,及其多种合金中.
(1)砷原子次外层上的电子数为___,砷化氢的电子式为___.
(2)成语“饮鸩止渴”中的“鸩”是指放了砒霜(As2O3)的酒.As2O3是两性偏酸性的氧化物,写出As2O3溶于浓盐酸的化学方程式___.
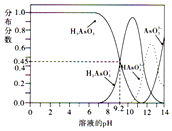
(3)As2O3溶于热水生成的亚砷酸(H3AsO3),具有较强的还原性,分可用于治疗白血病,其水溶液存在多种微粒形态,各微粒的分布分数与溶液pH的关系如图:
①向亚砷酸溶液中缓缓加入NaOH溶液至pH=11时,反应的离子方程式为___.
②电离平衡常数Ka1(H3AsO3)=___.
③Na2HAsO3溶液呈碱性,该溶液中c(H2AsO3-)___c(AsO33-)(填“>”、“<”或“=”).
④向含有HAsO32-的溶液中滴加氯水反应的离子方程式为___.

(1)砷原子次外层上的电子数为___,砷化氢的电子式为___.
(2)成语“饮鸩止渴”中的“鸩”是指放了砒霜(As2O3)的酒.As2O3是两性偏酸性的氧化物,写出As2O3溶于浓盐酸的化学方程式___.
(3)As2O3溶于热水生成的亚砷酸(H3AsO3),具有较强的还原性,分可用于治疗白血病,其水溶液存在多种微粒形态,各微粒的分布分数与溶液pH的关系如图:
①向亚砷酸溶液中缓缓加入NaOH溶液至pH=11时,反应的离子方程式为___.
②电离平衡常数Ka1(H3AsO3)=___.
③Na2HAsO3溶液呈碱性,该溶液中c(H2AsO3-)___c(AsO33-)(填“>”、“<”或“=”).
④向含有HAsO32-的溶液中滴加氯水反应的离子方程式为___.
▼优质解答
答案和解析
(1)As的原子序数为33,基态原子的电子排布式为1s22s22p63s23p63d104s24p3,次外层为3s23p63d10,所以砷原子次外层上的电子数为18,AsH3的结构中3个H原子和As原子间形成3条共价键,电子式为: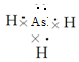 ,
,
故答案为:18;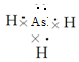 ;
;
(2)砒霜(As2O3)是两性偏酸性的氧化物,和酸反应体现碱性氧化物的性质,和盐酸反应生成AsCl3、H2O,反应方程式为:As2O3+6HCl=2AsCl3+3H2O,
故答案为:As2O3+6HCl=2AsCl3+3H2O;
(3)①根据各微粒的分布分数与溶液pH的关系图可知,pH=11时,生成H2AsO3-,所以向亚砷酸溶液中缓缓加入NaOH溶液至pH=11时,离子方程式为:H3AsO3+OH-=H2AsO3-+H2O,
故答案为:H3AsO3+OH-=H2AsO3-+H2O;
②电离平衡常数为生成物浓度幂之比与反应物浓度幂之积的比值,H3AsO3的第一级电离方程式为H3AsO3⇌H++H2AsO3-,图象中pH=9.2时,H3AsO3和H2AsO3-浓度相同,K=
=10-9.2,
故答案为:10-9.2;
③Na2HAsO3溶液呈碱性,说明H2AsO3-以水解为主,所以该溶液中c(H2AsO3-)>c(AsO33-),
故答案为:>;
④HAsO32-中的As显+3价,具有还原性,氯水中的氯气具有氧化性,两者发生氧化还原反应,As(+3→+5),Cl(0→-1),根据得失电子守恒和原子守恒,离子方程式为:HAsO32-+H2O+Cl2=H3AsO4+2Cl-,
故答案为:HAsO32-+H2O+Cl2=H3AsO4+2Cl-.
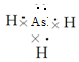 ,
,故答案为:18;
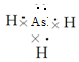 ;
;(2)砒霜(As2O3)是两性偏酸性的氧化物,和酸反应体现碱性氧化物的性质,和盐酸反应生成AsCl3、H2O,反应方程式为:As2O3+6HCl=2AsCl3+3H2O,
故答案为:As2O3+6HCl=2AsCl3+3H2O;
(3)①根据各微粒的分布分数与溶液pH的关系图可知,pH=11时,生成H2AsO3-,所以向亚砷酸溶液中缓缓加入NaOH溶液至pH=11时,离子方程式为:H3AsO3+OH-=H2AsO3-+H2O,
故答案为:H3AsO3+OH-=H2AsO3-+H2O;
②电离平衡常数为生成物浓度幂之比与反应物浓度幂之积的比值,H3AsO3的第一级电离方程式为H3AsO3⇌H++H2AsO3-,图象中pH=9.2时,H3AsO3和H2AsO3-浓度相同,K=
| C(H+)•C(H2ASO3-) |
| C(H3ASO3) |
故答案为:10-9.2;
③Na2HAsO3溶液呈碱性,说明H2AsO3-以水解为主,所以该溶液中c(H2AsO3-)>c(AsO33-),
故答案为:>;
④HAsO32-中的As显+3价,具有还原性,氯水中的氯气具有氧化性,两者发生氧化还原反应,As(+3→+5),Cl(0→-1),根据得失电子守恒和原子守恒,离子方程式为:HAsO32-+H2O+Cl2=H3AsO4+2Cl-,
故答案为:HAsO32-+H2O+Cl2=H3AsO4+2Cl-.
看了 砷(33As)在元素周期表中...的网友还看了以下:
砷的电子排布式 2020-04-25 …
(2014•同心县模拟)第VA族元素及其化合物在生产、生活中有着广泛的应用(1)砷的电子排布式为, 2020-07-07 …
自从人类发明了电扇以后,电扇便在许多领域之中开始了它为人类服务的历程.下面不属于电扇的功能作用一项 2020-07-28 …
第VA族元素及其化合物在生产、生活中有着广泛的应用(1)砷的电子排布式为,N、P、As三种元素的最常 2020-11-01 …
材料的开发、应用和发展是科技进步的结果,同时,材料的发展也促进了科技的进步和发展.(1)高纯度砷可用 2020-11-01 …
压电陶瓷是一种具有压电效应功能的陶瓷材料,已被用于许多领域。对压电陶瓷挤压或拉伸时,它的两端就会形成 2020-11-02 …
压电陶瓷是一种具有压电效应功能的陶瓷材料,已被用于许多领域.对压电陶瓷挤压或拉伸时,它的两端就会形成 2020-11-02 …
在多电子的原子中,电子在离核远近不同的区域运动.电子运动的区域不同是因为—— 2020-11-27 …
背景设定:电视已经深入到我们生活的每个领域.随着社会的发展,人们看电视的时间也越来越多.电视既给我们 2020-12-29 …
《2014年政府工作报告》中指出:在金融、石油、电力、铁路、电信、资源开发、公用事业等领域,向非国有 2020-12-30 …