早教吧作业答案频道 -->化学-->
氮化硅是一种重要的结构陶瓷材料,具有优良性能.(1)基态氮原子的电子排布式为,基态硅原子未成对电子数是,碳、氮、硅的电负性由大到小的顺序是.(2)碳热还原法制氮化
题目详情
氮化硅是一种重要的结构陶瓷材料,具有优良性能.
(1)基态氮原子的电子排布式为___,基态硅原子未成对电子数是___,碳、氮、硅的电负性由大到小的顺序是___.
(2)碳热还原法制氮化硅是在氮气中用碳还SiO2,写出该反应的化学方程式:___.氮化硅一般不与酸反应,但能与氢氟酸反应,写出氮化硅与过 量氢氟酸反应的化学方程式:___.
(3)三氯化硅烷(SiHCl3)也可用于制备氮化硅,三氯硅烷分子的空间构型为___,其分子中硅原子的杂化轨道类型为___.
(4)氮化硅与碳化硅、氮化硼等作用可产生结合材料,改善性能.氮化硅、碳化硅的化学性质都很稳定,其原因是___.
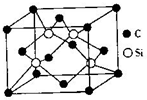
(5)碳化硅立方晶系晶胞如图所示,C-Si-C键的夹角是___,其晶体类型是___,若立方晶系的碳化硅密度为ρg•cm-3,NA表示阿伏加德罗常数的值,则晶胞的棱长为___.

(1)基态氮原子的电子排布式为___,基态硅原子未成对电子数是___,碳、氮、硅的电负性由大到小的顺序是___.
(2)碳热还原法制氮化硅是在氮气中用碳还SiO2,写出该反应的化学方程式:___.氮化硅一般不与酸反应,但能与氢氟酸反应,写出氮化硅与过 量氢氟酸反应的化学方程式:___.
(3)三氯化硅烷(SiHCl3)也可用于制备氮化硅,三氯硅烷分子的空间构型为___,其分子中硅原子的杂化轨道类型为___.
(4)氮化硅与碳化硅、氮化硼等作用可产生结合材料,改善性能.氮化硅、碳化硅的化学性质都很稳定,其原因是___.
(5)碳化硅立方晶系晶胞如图所示,C-Si-C键的夹角是___,其晶体类型是___,若立方晶系的碳化硅密度为ρg•cm-3,NA表示阿伏加德罗常数的值,则晶胞的棱长为___.
▼优质解答
答案和解析
(1)N原子核外电子数为7,由能量最低原理可知核外电子排布式为1s22s22p3,2p能级3个电子分别占据1个轨道,单电子数目为3,同周期自左而右电负性增大,同主族自上而下电负性减小,故电负性N>C>Si,
故答案为:1s22s22p3;3;N>C>Si;
(2)碳热还原法制氮化硅是在氮气中用碳还SiO2,反应生成Si3N4、CO,化学方程式为:6C+2N2+3SiO2
Si3N4+6CO,氮化硅一般不与酸反应,但能与氢氟酸反应,反应生成SiF4与NH4F,反应方程式为:Si3N4+16HF=3SiF4+4NH4F,
故答案为:6C+2N2+3SiO2
Si3N4+6CO;Si3N4+16HF=3SiF4+4NH4F;
(3)三氯化硅烷(SiHCl3)分子中Si原子形成4个σ键,没有孤对电子,三氯硅烷分子的空间构型为四面体形,杂化轨道数目为4,Si原子采取sp3杂化,
故答案为:四面体形;sp3杂化;
(4)氮化硅、碳化硅晶体中原子之间形成共价键,键能大,键牢固,化学性质稳定,
故答案为:晶体中原子之间形成共价键,键能大,键牢固;
(5)碳化硅立方晶系晶胞中,体内Si原子与周围的4个C原子形成正四面体结构,C-Si-C键的夹角是109°28′;原子之间形成共价键,向空间延伸的立体网状结构,属于原子晶体;
晶胞中Si原子数目为4、C原子数目为8×
+6×
=4,则晶胞质量为
g,化硅密度为ρg•cm-3,则晶胞棱长=
=
cm,
故答案为:109°28′;原子晶体;
.
故答案为:1s22s22p3;3;N>C>Si;
(2)碳热还原法制氮化硅是在氮气中用碳还SiO2,反应生成Si3N4、CO,化学方程式为:6C+2N2+3SiO2
| ||
故答案为:6C+2N2+3SiO2
| ||
(3)三氯化硅烷(SiHCl3)分子中Si原子形成4个σ键,没有孤对电子,三氯硅烷分子的空间构型为四面体形,杂化轨道数目为4,Si原子采取sp3杂化,
故答案为:四面体形;sp3杂化;
(4)氮化硅、碳化硅晶体中原子之间形成共价键,键能大,键牢固,化学性质稳定,
故答案为:晶体中原子之间形成共价键,键能大,键牢固;
(5)碳化硅立方晶系晶胞中,体内Si原子与周围的4个C原子形成正四面体结构,C-Si-C键的夹角是109°28′;原子之间形成共价键,向空间延伸的立体网状结构,属于原子晶体;
晶胞中Si原子数目为4、C原子数目为8×
| 1 |
| 8 |
| 1 |
| 2 |
| 4×(28+12) |
| NA |
| 3 |
| ||||
| 3 |
| ||
故答案为:109°28′;原子晶体;
| 3 |
| ||
看了 氮化硅是一种重要的结构陶瓷材...的网友还看了以下:
空城计里的一个士兵作文400字快,是要以一个士兵的见闻写的,要有神态,动作,语言,记住400字 2020-04-26 …
关于小动物的作文300字以上要有静态和动态 2020-05-13 …
雪后的景色?越多越好语句要超级优美要有静态和动态描写.急. 2020-05-13 …
写给20年后的自己(要有神态细节描写,神态动作)300-400字左右.急-.- 2020-06-06 …
写一篇关于写景的作文要求写具体;写出景物的位置、形状、颜色;要有动态、静态描写,要给人如临其境的感 2020-07-07 …
我敬佩的一个人写警察的,要有神态,动作,语言描写,事例要具体 2020-07-10 …
小学五年级下次155页小练笔用一段话,写写家乡的某处景或某个物,要写出特点来.不少于300字也不要 2020-07-18 …
描写人上课很认真的句子要有神态动作要多些 2020-11-01 …
描写人上课很认真的句子要有神态动作要多些 2020-11-01 …
物质的三态变化我们化学老师说,只要有三态变化的都是物理变化。那只有两态变化的(如:铁变成铁水)是物理 2020-11-04 …