早教吧作业答案频道 -->化学-->
氯元素的单质及其化合物在生产生活中应用极其广泛.请完成下列填空:Ⅰ:氯气性质探究设计如图实验装置来制备并验证氯气的性质(部分夹持装置未画出).(1)A中放置固体二氧化锰
题目详情
氯元素的单质及其化合物在生产生活中应用极其广泛.请完成下列填空:
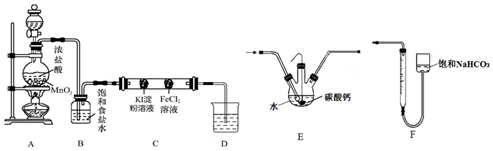
Ⅰ:氯气性质探究
设计如图实验装置来制备并验证氯气的性质(部分夹持装置未画出).
(1)A中放置固体二氧化锰的装置名称是___.
(2)装置B的作用是___.
(3)硬质玻璃管C中事先装有两个沾有相关试剂的棉球,左侧棉球的实验现象为___.
(4)D中的NaOH溶液用来吸收尾气,向反应后的D中加入足量稀硫酸会产生气体,写出该反应的离子方程式___.
Ⅱ:制备HClO
(5)设计装置E代替如图的装置C,用于制备较高浓度的HClO溶液.在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙.
①该方案可以制得较高浓度HClO的原因是(结合必要的化学语言回答)___.
②反应结束后将塑料网中剩余的石灰石提出液面,所得的溶液与稀盐酸混合,立即产生大量CO2气体,则反应所得溶液中的溶质除HClO外,还含有___、___(写两种钙盐的化学式,一种正盐,一种酸式盐);该小组同学测得反应中碳酸钙质量减少M g,反应后从所得的200mL溶液中取用10mL与足量稀盐酸混合,连接F装置测得产生的气体体积为V L(已换算成标准状况),则原溶液中含钙正盐的浓度为___mol•L-1(用含M、V的代数式表示).

Ⅰ:氯气性质探究
设计如图实验装置来制备并验证氯气的性质(部分夹持装置未画出).
(1)A中放置固体二氧化锰的装置名称是___.
(2)装置B的作用是___.
(3)硬质玻璃管C中事先装有两个沾有相关试剂的棉球,左侧棉球的实验现象为___.
(4)D中的NaOH溶液用来吸收尾气,向反应后的D中加入足量稀硫酸会产生气体,写出该反应的离子方程式___.
Ⅱ:制备HClO
(5)设计装置E代替如图的装置C,用于制备较高浓度的HClO溶液.在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙.
①该方案可以制得较高浓度HClO的原因是(结合必要的化学语言回答)___.
②反应结束后将塑料网中剩余的石灰石提出液面,所得的溶液与稀盐酸混合,立即产生大量CO2气体,则反应所得溶液中的溶质除HClO外,还含有___、___(写两种钙盐的化学式,一种正盐,一种酸式盐);该小组同学测得反应中碳酸钙质量减少M g,反应后从所得的200mL溶液中取用10mL与足量稀盐酸混合,连接F装置测得产生的气体体积为V L(已换算成标准状况),则原溶液中含钙正盐的浓度为___mol•L-1(用含M、V的代数式表示).
▼优质解答
答案和解析
Ⅰ:氯气性质探究
(1)装置A是制备氯气的发生装置,二氧化锰为固体和滴入的盐酸加热反应生成氯气,盛放二氧化锰的仪器为圆底烧瓶,故答案为:圆底烧瓶;
(2)生成的氯气含有水蒸气和氯化氢,氯化氢极易溶于水,氯化钠溶液中氯离子抑制氯气和水的反应,通过饱和食盐水除去氯化氢气体杂质,
故答案为:除去氯气中的氯化氢;
(3)氯气有氧化性可以氧化碘化钾生成碘单质,2KI+Cl2=I2+2KCl,碘单质遇到淀粉变蓝色,故答案为:变蓝色;
(4)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,加入酸发生归中反应生成氯气,反应的离子方程式为:ClO-+Cl-+2H+=Cl2↑+H2O,
故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
Ⅱ.(5)①该方案可以制得较高浓度HClO的原因是溶液中存在化学平衡:Cl2+H2O H++Cl-+HClO,碳酸钙与H+反应,使平衡向右移动,HClO浓度增大,得到较高浓度HClO,
故答案为:Cl2+H2O⇌H++Cl-+HClO,碳酸钙与H+反应,使平衡向右移动,HClO浓度增大;
②反应结束后将塑料网中剩余的石灰石提出液面,所得的溶液与稀盐酸混合,立即产生大量CO2气体,说明溶液中含有碳酸氢钙,是生成的二氧化碳和碳酸钙反应生成的碳酸氢钙,所以溶液中存在次氯酸、氯化钙、次氯酸钙;该小组同学测得反应中碳酸钙质量减少M g为碳酸钙,反应后从所得的200mL溶液中取用10mL与足量稀盐酸混合,连接F装置测得产生的气体体积为V L(已换算成标准状况),依据反应定量关系,CaCO3~Ca(HCO3)2~2CO2计算200ml溶液中生成二氧化碳的碳酸钙质量=(
×
)mol×
×100g/mol,则原溶液中含钙正盐的浓度=
=
-
,
故答案为:CaCl2、Ca(HCO3)2、
-
.
(1)装置A是制备氯气的发生装置,二氧化锰为固体和滴入的盐酸加热反应生成氯气,盛放二氧化锰的仪器为圆底烧瓶,故答案为:圆底烧瓶;
(2)生成的氯气含有水蒸气和氯化氢,氯化氢极易溶于水,氯化钠溶液中氯离子抑制氯气和水的反应,通过饱和食盐水除去氯化氢气体杂质,
故答案为:除去氯气中的氯化氢;
(3)氯气有氧化性可以氧化碘化钾生成碘单质,2KI+Cl2=I2+2KCl,碘单质遇到淀粉变蓝色,故答案为:变蓝色;
(4)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,加入酸发生归中反应生成氯气,反应的离子方程式为:ClO-+Cl-+2H+=Cl2↑+H2O,
故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
Ⅱ.(5)①该方案可以制得较高浓度HClO的原因是溶液中存在化学平衡:Cl2+H2O H++Cl-+HClO,碳酸钙与H+反应,使平衡向右移动,HClO浓度增大,得到较高浓度HClO,
故答案为:Cl2+H2O⇌H++Cl-+HClO,碳酸钙与H+反应,使平衡向右移动,HClO浓度增大;
②反应结束后将塑料网中剩余的石灰石提出液面,所得的溶液与稀盐酸混合,立即产生大量CO2气体,说明溶液中含有碳酸氢钙,是生成的二氧化碳和碳酸钙反应生成的碳酸氢钙,所以溶液中存在次氯酸、氯化钙、次氯酸钙;该小组同学测得反应中碳酸钙质量减少M g为碳酸钙,反应后从所得的200mL溶液中取用10mL与足量稀盐酸混合,连接F装置测得产生的气体体积为V L(已换算成标准状况),依据反应定量关系,CaCO3~Ca(HCO3)2~2CO2计算200ml溶液中生成二氧化碳的碳酸钙质量=(
| V |
| 22.4 |
| 1 |
| 2 |
| 200 |
| 10 |
M-
| ||
| 100g/mol×0.2L |
| M |
| 20 |
| V |
| 0.448 |
故答案为:CaCl2、Ca(HCO3)2、
| M |
| 20 |
| V |
| 0.448 |
看了 氯元素的单质及其化合物在生产...的网友还看了以下:
氧化还原反应中氧化产物和还原产物的质量比2NH4ClO4=======4H2O+Cl2+2O2氧化 2020-05-16 …
急.如果在一个氧化还原反应中.氧化产物和还原产物是同一物质.那生成的氧化产物和还原产物的质量是不是 2020-05-21 …
氢化钠(NaH)是一种生氢剂,可发生如下反应:NaH+H2O=NaOH+H2↑,对这一反应的描述正 2020-05-24 …
氢化钠是一种生氢剂可发生如下反应:NaH+H2O=NaOH+H2,下列选项正确的是A.NaH是氧化 2020-06-30 …
在同量的下列营养物质中,前者体外燃烧和体内氧化产热量相等,且总耗氧量较少,后者体外燃烧和体内氧化产 2020-07-03 …
社会主义的文化产品具有不同于物质产品的特殊属性,它坚持选项:题号:3题型:单选题(请在以下几个选项中 2020-11-02 …
九下.科学.糖类的消化位置,消化产物,代谢终产物分别是什么?蛋白质的消化位置,消化产物,代谢终产物分 2020-11-11 …
阅读下面的文字,完成后面题。(9分)守护阅读文化的价值质点艾斐所谓文化价值的质点,是指文化的原生价值 2020-12-19 …
根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题氧化剂和还原剂的分子个数比?氧化剂与氧化 2020-12-26 …
人教版的9年级化学有哪些物质产生白烟?哪些物质是产生白烟,哪些物质是产生白雾,包括反应现象和放在空气 2021-02-05 …