早教吧作业答案频道 -->化学-->
某化学兴趣小组用如图所示装置制取氯酸钾、次氯酸钠和氯水并进行探究实验.实验I.制取氮酸钾、次氯酸钠和氯水(1)写出装置A实验室制取Cl2的化学反应方程式.(2)制取实验结束后
题目详情
某化学兴趣小组用如图所示装置制取氯酸钾、次氯酸钠和氯水并进行探究实验.
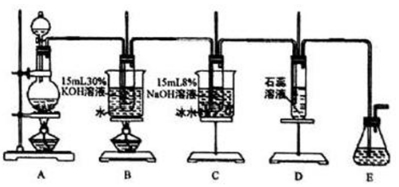
实验I.制取氮酸钾、次氯酸钠和氯水
(1)写出装置A实验室制取Cl2的化学反应方程式___.
(2)制取实验结束后,取出装置B中的试管,冷却结晶、过滤、洗涤,该实验操作过程需要的玻璃仪器有胶头滴管、烧杯、___、___.为提高氯酸钾和次氯酸钠的产率,在实验装置中还需要改进的是___.
(3)装置 C 中反应需要在冰水浴中进行,其原因是___.
(4)装置D中的实验现象是溶液先变红后褪色,最后又变为___色.
实验Ⅱ尾气处理
实验小组利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理.
(5)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响)
①提出合理假设
假设1:只存在SO32-;
假设2:既不存在SO32-也不存在ClO-;
假设 3:___.
②设计实验方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3mol/L H2SO4、1mol/LNaOH 溶液、0.01mol/L 酸性 KMnO4 溶液、淀粉 KI 溶液.

实验I.制取氮酸钾、次氯酸钠和氯水
(1)写出装置A实验室制取Cl2的化学反应方程式___.
(2)制取实验结束后,取出装置B中的试管,冷却结晶、过滤、洗涤,该实验操作过程需要的玻璃仪器有胶头滴管、烧杯、___、___.为提高氯酸钾和次氯酸钠的产率,在实验装置中还需要改进的是___.
(3)装置 C 中反应需要在冰水浴中进行,其原因是___.
(4)装置D中的实验现象是溶液先变红后褪色,最后又变为___色.
实验Ⅱ尾气处理
实验小组利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理.
(5)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响)
①提出合理假设
假设1:只存在SO32-;
假设2:既不存在SO32-也不存在ClO-;
假设 3:___.
②设计实验方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3mol/L H2SO4、1mol/LNaOH 溶液、0.01mol/L 酸性 KMnO4 溶液、淀粉 KI 溶液.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3mol•L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中 | ___ |
| 步骤2: ___ | (1)若溶液褪色,则假设1成立 (2)若溶液不褪色,则假设2或3成立 |
| 步骤3: ___ | (1)若溶液变蓝,则假设成立 (2)若溶液不变蓝,综合步骤中的(2),则假设2成立 |
▼优质解答
答案和解析
(1)实验室用二氧化锰和浓盐酸共热制备氯气,反应为:Mn2O+4HCl(浓)
MnCl2+Cl2↑+2H2O;
故答案为:Mn2O+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(2)制取实验结束后,取出装置B中的试管,冷却结晶、过滤、洗涤,该实验操作过程需要的玻璃仪器有胶头滴管、烧杯、漏斗、玻璃棒;制备的氯气含有氯化氢,所以为提高氯酸钾和次氯酸钠的产率,在A和B之间添加盛有饱和NaCl的洗气装置;
故答案为:漏斗、玻璃棒;在A和B之间添加盛有饱和NaCl的洗气装置;
(3)温度较高时生成氯酸盐,C装置制备次氯酸钠,故用冷水浴;
故答案我:温度升高会生成氯酸钠;
(4)装置D中为石蕊试液,通入氯气,部分氯气生成盐酸和次氯酸,显酸性,石蕊显红色,次氯酸漂白性,红色褪去,最终形成氯水溶液,呈现黄绿色;
故答案为:黄绿色;
(5)①用刚吸收过少量SO2的NaOH溶液吸收氯气,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-,SO32-具有还原性,ClO-具有氧化性,二者不能共存,可能假设1:只存在SO32-;假设2:既不存在SO32-也不存在ClO-;假设 3:只存在ClO;
故答案为:只存在ClO;
②因为吸收液呈碱性,先取少量吸收液于试管中,滴加3moL-L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中先加入硫酸的试管,若存在SO32-、ClO-,分别生成了H2SO3和HClO,H2SO3的还原性能使酸性高锰酸钾褪色,HClO的氧化性能氧化碘离子为碘单质,使淀粉显蓝色,故具体步骤和结论为:
故答案为:
| ||
故答案为:Mn2O+4HCl(浓)
| ||
(2)制取实验结束后,取出装置B中的试管,冷却结晶、过滤、洗涤,该实验操作过程需要的玻璃仪器有胶头滴管、烧杯、漏斗、玻璃棒;制备的氯气含有氯化氢,所以为提高氯酸钾和次氯酸钠的产率,在A和B之间添加盛有饱和NaCl的洗气装置;
故答案为:漏斗、玻璃棒;在A和B之间添加盛有饱和NaCl的洗气装置;
(3)温度较高时生成氯酸盐,C装置制备次氯酸钠,故用冷水浴;
故答案我:温度升高会生成氯酸钠;
(4)装置D中为石蕊试液,通入氯气,部分氯气生成盐酸和次氯酸,显酸性,石蕊显红色,次氯酸漂白性,红色褪去,最终形成氯水溶液,呈现黄绿色;
故答案为:黄绿色;
(5)①用刚吸收过少量SO2的NaOH溶液吸收氯气,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-,SO32-具有还原性,ClO-具有氧化性,二者不能共存,可能假设1:只存在SO32-;假设2:既不存在SO32-也不存在ClO-;假设 3:只存在ClO;
故答案为:只存在ClO;
②因为吸收液呈碱性,先取少量吸收液于试管中,滴加3moL-L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中先加入硫酸的试管,若存在SO32-、ClO-,分别生成了H2SO3和HClO,H2SO3的还原性能使酸性高锰酸钾褪色,HClO的氧化性能氧化碘离子为碘单质,使淀粉显蓝色,故具体步骤和结论为:
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3mol•L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中 | ---------- |
| 步骤2:向A试管中滴入1-2mL0.01mol/L 酸性 KMnO4 溶液 | (1)若溶液褪色,则假设1成立 (2)若溶液不褪色,则假设2或3成立 |
| 步骤3:向B试管中滴加1-2滴淀粉-KI溶液 | (1)若溶液变蓝,则假设成立 (2)若溶液不变蓝,综合步骤中的(2),则假设2成立 |
| 实验步骤 | 预期现象和结论 |
| --------- | |
| 步骤2:向A试管中滴入1-2mL0.01mol/L 酸性 KMnO4 溶液 | |
| 步骤3:向B试管中滴加1-2滴淀粉-KI溶液 |
看了 某化学兴趣小组用如图所示装置...的网友还看了以下:
有关化学计算题镁条在空气中燃烧生成MgO和Mg3N2,将产物溶解在60ml2mol/L的盐酸中,用2 2020-03-30 …
请问一下这一题化学题怎样做?为什么缓冲溶液中醋酸钠总浓度为1.0mol配制pH=5.0的缓冲溶液1 2020-05-13 …
实验室用铁粉和稀硫酸反应制取氧气,现在用10g的铁和100g9.8%的稀硫酸反应,能制的多少L氢气 2020-05-14 …
4mol/L盐酸和3mol/L氨水怎么配.4mol/L盐酸和3mol/L氨水怎么配.哪位知道的赶紧 2020-05-16 …
比较以下反应放出CO2的速率1)A大理石块和2mol/L盐酸B大理石块和2mol/L醋酸(2)A大 2020-06-16 …
某工厂采用含硫酸和氢氟酸的溶液作为矿物中稀有元素的萃取液,生产要求该萃取液中硫酸的浓度3MOL/L 2020-06-27 …
分子筛中B酸和L酸的催化功能?请问分子筛的B酸中心是起异构化作用的吗?L酸中心是起裂化的作用吗?那 2020-07-08 …
足量铁和下列酸反应,生成氢气的物质的量最多的是A.18.4mol/l硫酸10mlB.2mol/l硫 2020-07-29 …
下列操作能达成实验目的是()A.溴乙烷与氢氧化钠溶液共煮后,加入硝酸银检验Br-B.用CuSO4溶 2020-07-29 …
0.1mol/l磷酸缓冲液配制方法请问0.1mol/l,PH=7.4的磷酸缓冲液怎么配制。为什么有的 2020-11-07 …