早教吧作业答案频道 -->化学-->
某化学小组从理论上初步探究“已知质量比的硝酸钾和氯化钠的混合物中提纯硝酸钾”.分析提纯方法表一:常温下(20℃)溶解度和溶解性的关系溶解度SS≥10g1g≤S<10g0
题目详情
某化学小组从理论上初步探究“已知质量比的硝酸钾和氯化钠的混合物中提纯硝酸钾”.
【分析提纯方法】
表一:常温下(20℃)溶解度和溶解性的关系
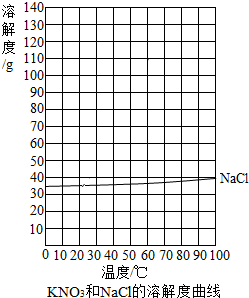
表二:硝酸钾和氯化钠在不同温度时的溶解度
(1)常温下,KNO3和NaCl的溶解性均为___.
(2)根据表中数据,绘制KNO3的溶解度曲线.
(3)根据KNO3的溶解度曲线,获得KNO3在70℃时的溶解度约为___g.
【设计提纯步骤】
(1)选取样品(95gKNO3和5gNaCl的混合物)
(2)配制80℃时KNO3的饱和溶液(加水约56.2mL,水的密度约为1g•mL-1)
(3)降温至20℃
(4)得到晶体
【设计提纯方案】
为了证明(4)中得到的晶体为纯净的KNO3,该小组同学结合已有知识,从理论上初步设计了以下方案;(不考虑不同溶质对溶解度的相互影响及实验过程中水铬固体的损失等影响因素)
方案一 通过化学实验进行检验,取少量(4)中得到的晶体于试管中,加水配成溶液,滴加___,观察实验现象.
方案二 计算析出KNO3晶体的质量约为___g(精确到0.1g)与(4)中得到晶体的质量进行比较
方案三___与95%进行比较.
方案四___.
【分析提纯方法】
表一:常温下(20℃)溶解度和溶解性的关系
| 溶解度S | S≥10g | 1g≤S<10g | 0.01g≤S<1g | S<0.01g |
| 溶解性 | 易溶 | 可溶 | 微溶 | 难溶 |
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(2)根据表中数据,绘制KNO3的溶解度曲线.
(3)根据KNO3的溶解度曲线,获得KNO3在70℃时的溶解度约为___g.
【设计提纯步骤】

(1)选取样品(95gKNO3和5gNaCl的混合物)
(2)配制80℃时KNO3的饱和溶液(加水约56.2mL,水的密度约为1g•mL-1)
(3)降温至20℃
(4)得到晶体
【设计提纯方案】
为了证明(4)中得到的晶体为纯净的KNO3,该小组同学结合已有知识,从理论上初步设计了以下方案;(不考虑不同溶质对溶解度的相互影响及实验过程中水铬固体的损失等影响因素)
方案一 通过化学实验进行检验,取少量(4)中得到的晶体于试管中,加水配成溶液,滴加___,观察实验现象.
方案二 计算析出KNO3晶体的质量约为___g(精确到0.1g)与(4)中得到晶体的质量进行比较
方案三___与95%进行比较.
方案四___.
▼优质解答
答案和解析
(1)常温下,KNO3和NaCl的溶解度分别是31.6g、36g,所以溶解性均为易溶;
(2)根据表格中硝酸钾在不同温度下的溶解度,用横坐标表示温度,纵坐标表示物质的溶解度,可画出其溶解度曲线如下,
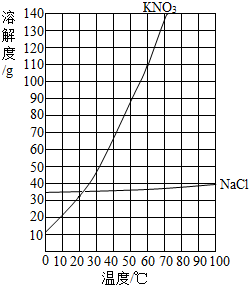
(3)根据KNO3的溶解度曲线,获得KNO3在70℃时的溶解度约为138g;
【设计提纯方案】
方案一 通过化学实验进行检验,取少量(4)中得到的晶体于试管中,加水配成溶液,滴加硝酸银,观察实验现象;
方案二 设56.2g水在20℃是溶解的硝酸钾为x
100g:31.6g=56.2g:x
x=17.8g
所以析出KNO3晶体的质量约为77.2g,
计算析出KNO3晶体的质量约为77.2g与(4)中得到晶体的质量进行比较;
设56.2g水在20℃是溶解的氯化钠为y
100g:36g=56.2g:y
y=20.2g
所以析出氯化钠晶体质量为:
方案三析出晶体中硝酸钾所占的比例
×100%=82%,
82%与95%进行比较;
方案四通过计算可知56.2g水可以溶解20.2g的氯化钠,
利用20.2g与5g进行比较.
故答案为:(1)易溶;
(2)

(3)138;
【设计提纯方案】
方案一 硝酸银;
方案二 77.2g;
方案三82%;
方案四利用20.2g与5g进行比较.
(2)根据表格中硝酸钾在不同温度下的溶解度,用横坐标表示温度,纵坐标表示物质的溶解度,可画出其溶解度曲线如下,

(3)根据KNO3的溶解度曲线,获得KNO3在70℃时的溶解度约为138g;
【设计提纯方案】
方案一 通过化学实验进行检验,取少量(4)中得到的晶体于试管中,加水配成溶液,滴加硝酸银,观察实验现象;
方案二 设56.2g水在20℃是溶解的硝酸钾为x
100g:31.6g=56.2g:x
x=17.8g
所以析出KNO3晶体的质量约为77.2g,
计算析出KNO3晶体的质量约为77.2g与(4)中得到晶体的质量进行比较;
设56.2g水在20℃是溶解的氯化钠为y
100g:36g=56.2g:y
y=20.2g
所以析出氯化钠晶体质量为:
方案三析出晶体中硝酸钾所占的比例
| 77.2g |
| 95g |
82%与95%进行比较;
方案四通过计算可知56.2g水可以溶解20.2g的氯化钠,
利用20.2g与5g进行比较.
故答案为:(1)易溶;
(2)

(3)138;
【设计提纯方案】
方案一 硝酸银;
方案二 77.2g;
方案三82%;
方案四利用20.2g与5g进行比较.
看了 某化学小组从理论上初步探究“...的网友还看了以下:
1.化学反应中反应物生成物间存在着一定的质量关系这种质量关系与物质的______和______密不 2020-05-16 …
关于氧化还原反应.处理它们的关系有点乱.什么是氧化性和还原性.什么事氧化剂和还原剂.什么是氧化物关 2020-05-17 …
老师布置了一个关于音程的作业,好像是变化音程,好难音程有自然音程和变化音程,变化音程有那个什么纯一 2020-06-10 …
变配电系统图中,有一条:2个进线开关和1个母联开关采用电气和钥匙联琐,实现3合2功能是什么意思?第 2020-06-25 …
关于离子键、化学键、分子间作用力和熔沸点的问题1.氯化钠和氯化钾的熔沸点与钠和钾的原子半径有关,钾 2020-07-06 …
隐形眼镜洗液有效成分是过氧化氢(H2O2),下列有关过氧化氢正确的是()A.过氧化氢由氢气和氧气组 2020-07-15 …
(1)工业上可利用“甲烷蒸气转化法”生产氢气,反应为甲烷和水蒸气在高温和催化剂存在的条件下生成一氧化 2020-11-04 …
[大学物化]逸度系数和1的关系?f大于1,等于1,小于1分别可以说明气体怎样的分子间作用力?化工热力 2020-11-05 …
相对介电常数和极化率关系引用:(1)定义:相对介电常数εr与电极化率χe的关系为εr=1+χe.(2 2020-11-08 …
铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒.有关含铬化合物的相互转化关 2020-12-19 …