早教吧作业答案频道 -->化学-->
叠氮化钠(NaN3)常作为汽车安全气囊的药剂,其固体易溶于水,微溶于乙醇,不溶于乙醚.(1)实验室制取叠氮化钠的原理、装置及主要步骤如下.ⅰ.2Na+NH3
题目详情
叠氮化钠 (NaN3) 常作为汽车安全气囊的药剂,其固体易溶于水,微溶于乙醇,不溶于乙醚.
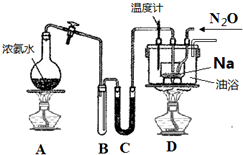
(1)实验室制取叠氮化钠的原理、装置及主要步骤如下.
ⅰ.2Na+NH3
2NaNH2+H2ⅱ.
NaNH2+N2O
NaN3+H2O,
①组装仪器检查装置气密性后,装入药品.装置C中盛放的药品是___.
②实验过程应先点燃___(填“A”或“D”)的酒精灯,理由是___.
③在反应ⅰ充分进行后,通入N2O气体,加热.此时采用油浴而不用水浴的主要原因是___.
(2)装置D反应完全结束后,取出混合物进行以下操作,得到NaN3固体:
D中混合物
NaN3
已知:NaNH2能与水反应生成NaOH和氨气.
操作ⅱ的目的是___;操作ⅳ最好选用的试剂是___.
(3)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数.测定过程反应方程式为
2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑.Ce4++Fe2+=Ce3++Fe3+
首先将2.50g试样配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入50.00mL 0.1000mol•L-1(NH4)2Ce(NO3)6,充分反应后,将溶液稍稀释,向溶液中加入5mL浓硫酸,滴入2滴邻菲哕啉指示液,用0.0500mol•L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为24.00mL.
①则试样中含NaN3的质量分数为___.
②为了提高该实验的精确度,该实验需要补充___.
(4)消防时,销毁NaN3常用NaClO溶液,该反应过程中只有N2一种气体生成,写出反应方程式___.

(1)实验室制取叠氮化钠的原理、装置及主要步骤如下.
ⅰ.2Na+NH3
| ||
NaNH2+N2O
| ||
①组装仪器检查装置气密性后,装入药品.装置C中盛放的药品是___.
②实验过程应先点燃___(填“A”或“D”)的酒精灯,理由是___.
③在反应ⅰ充分进行后,通入N2O气体,加热.此时采用油浴而不用水浴的主要原因是___.
(2)装置D反应完全结束后,取出混合物进行以下操作,得到NaN3固体:
D中混合物
| 加水 |
| |
| Ⅰ |
| 加乙醇 |
| |
| Ⅱ |
| 过滤 |
| |
| Ⅲ |
| 洗涤 |
| |
| Ⅳ |
| 干燥 |
| |
| Ⅴ |
已知:NaNH2能与水反应生成NaOH和氨气.
操作ⅱ的目的是___;操作ⅳ最好选用的试剂是___.
(3)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数.测定过程反应方程式为
2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑.Ce4++Fe2+=Ce3++Fe3+
首先将2.50g试样配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入50.00mL 0.1000mol•L-1(NH4)2Ce(NO3)6,充分反应后,将溶液稍稀释,向溶液中加入5mL浓硫酸,滴入2滴邻菲哕啉指示液,用0.0500mol•L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为24.00mL.
①则试样中含NaN3的质量分数为___.
②为了提高该实验的精确度,该实验需要补充___.
(4)消防时,销毁NaN3常用NaClO溶液,该反应过程中只有N2一种气体生成,写出反应方程式___.
▼优质解答
答案和解析
(1)①A中产生的氨气混有水蒸气,干燥氨气选择碱石灰,则在C中盛放的药品是碱石灰,
故答案为:碱石灰;
②实验过程中先点燃A产生氨气将装置内空气驱赶除去,防止产品不纯,
故答案为:A;先产生NH3,将装置内空气驱赶除去,防止产品不纯;
③NaNH2+N2O
NaN3+H2O,水浴温度达不到反应所需的温度210℃-220℃,
故答案为:水浴温度达不到反应所需的温度210℃-220℃;
(2)D中混合物加水后,根据叠氮化钠 (NaN3)固体易溶于水,微溶于乙醇,不溶于乙醚,NaN3溶解在水中,NaNH2与水反应生成NaOH和氨气,可知操作Ⅱ加乙醇可降低NaN3的溶解度促使NaN3析出;乙醚洗涤叠氮化钠可减少叠氮化钠的损失,
故答案为:降低NaN3的溶解量或溶解度或促使NaN3析出;乙醚;
(3)①计算n[(NH4)2Ce(NO3)6],n[(NH4)2Fe(SO4)2],结合滴定过程,叠氮化钠和六硝酸铈铵反应,剩余的六硝酸铈铵,加入浓硫酸,用0.0500mol•L-1(NH4)2Fe(SO4)2(硫酸亚铁铵)标准滴定溶液滴定过量的Ce4+,结合化学方程式定量关系计算:
n[(NH4)2Ce(NO3)6]=0.1000mol•L-1×50.00×10-3L=5.000×10-3mol,
n[(NH4)2Fe(SO4)2]=0.0500mol•L-1×24.00×10-3L=1.200×10-3mol,
与NaN3反应的n[(NH4)2Ce(NO3)6]=5.000×10-3mol-1.200×10-3mol=3.800×10-3mol,
ω=
×100%=98.8%,
故答案为:98.8%;
②为了提高该实验的精确度,氧化还原反应滴定实验一般要用平行实验,求平均值,
故答案为:平行实验;
(4)根据氮元素化合价高,氯元素化合价降低且只有N2一种气体生成,则氯只能从+1降到-1价,其他元素化合价不变,水参加反应,生成氯化钠、氮气、氢氧化钠,
则反应方程式为:2NaN3+NaClO+H2O=NaCl+3N2↑+2NaOH,
故答案为:2NaN3+NaClO+H2O=NaCl+3N2↑+2NaOH.
故答案为:碱石灰;
②实验过程中先点燃A产生氨气将装置内空气驱赶除去,防止产品不纯,
故答案为:A;先产生NH3,将装置内空气驱赶除去,防止产品不纯;
③NaNH2+N2O
| ||
故答案为:水浴温度达不到反应所需的温度210℃-220℃;
(2)D中混合物加水后,根据叠氮化钠 (NaN3)固体易溶于水,微溶于乙醇,不溶于乙醚,NaN3溶解在水中,NaNH2与水反应生成NaOH和氨气,可知操作Ⅱ加乙醇可降低NaN3的溶解度促使NaN3析出;乙醚洗涤叠氮化钠可减少叠氮化钠的损失,
故答案为:降低NaN3的溶解量或溶解度或促使NaN3析出;乙醚;
(3)①计算n[(NH4)2Ce(NO3)6],n[(NH4)2Fe(SO4)2],结合滴定过程,叠氮化钠和六硝酸铈铵反应,剩余的六硝酸铈铵,加入浓硫酸,用0.0500mol•L-1(NH4)2Fe(SO4)2(硫酸亚铁铵)标准滴定溶液滴定过量的Ce4+,结合化学方程式定量关系计算:
n[(NH4)2Ce(NO3)6]=0.1000mol•L-1×50.00×10-3L=5.000×10-3mol,
n[(NH4)2Fe(SO4)2]=0.0500mol•L-1×24.00×10-3L=1.200×10-3mol,
与NaN3反应的n[(NH4)2Ce(NO3)6]=5.000×10-3mol-1.200×10-3mol=3.800×10-3mol,
ω=
| 3.800×10-3mol×65g/mol | ||
2.50g×
|
故答案为:98.8%;
②为了提高该实验的精确度,氧化还原反应滴定实验一般要用平行实验,求平均值,
故答案为:平行实验;
(4)根据氮元素化合价高,氯元素化合价降低且只有N2一种气体生成,则氯只能从+1降到-1价,其他元素化合价不变,水参加反应,生成氯化钠、氮气、氢氧化钠,
则反应方程式为:2NaN3+NaClO+H2O=NaCl+3N2↑+2NaOH,
故答案为:2NaN3+NaClO+H2O=NaCl+3N2↑+2NaOH.
看了 叠氮化钠(NaN3)常作为汽...的网友还看了以下:
作为汽车动力燃料的汽油,其主要成份是异辛烷。下列各式可以肯定与上述异辛烷互称为同系物的是A.C8H 2020-05-13 …
作为汽车动力燃料的汽油,其主要成份是异辛烷,其结构简式如图下列各式可以肯定与上述异辛烷互称为同系物 2020-05-13 …
汽油机和柴油机统称为两者在构造相似其主要不同点是前者有后者有汽油机和柴油机工作的不同点是1吸收冲程 2020-05-16 …
作为汽车动力燃料的汽油,其主要成份是异辛烷.下列各式可以肯定与上述异辛烷互称为同系物的是A.C8H 2020-06-06 …
文言文高手请过来赵简子上羊肠之阪,群臣皆偏袒推车,而虎会独担戟行歌,不推车.简子曰:“寡人上阪,群 2020-06-20 …
近年来,雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.(1)汽 2020-06-29 …
2014年初,雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.( 2020-06-29 …
2015年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.(1) 2020-06-29 …
2014年初雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.(1 2020-06-29 …
上海的卢浦大桥是世界上跨径最大的拱形桥.其主跨径为550m,比世界上最大的美国西弗吉尼亚大桥还长3 2020-07-02 …