(10分)I、常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。回
(10分)I、常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。

回答下列问题:
(1)在同一溶液中,H2CO3、HCO3-、CO32-(填:“能”或“不能”) 大量共存。
(2)已知在25℃时,CO32-水解反应的平衡常数(即水解常数用Kh表示)
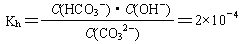
当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH= 。
(3)当混合液的pH=________时,开始放出CO2气体。
II、(1)常温下向25mL含HCl 0.01mol的溶液中滴加氨水至过量,该过程中水的电离平衡____________________(填写电离平衡移动情况)。当滴加氨水到25mL时,测得溶液中水的电离度最大,则氨水的浓度为______________。
(2)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH________7(填“>”、“<”或“=”)。
(3)25 ℃时,将a mol NH4NO3溶于水,向所得溶液中滴加b L氨水后溶液呈中性,则所滴加氨水的浓度是________mol·L-1。(用含a 、b 的式子表示)(NH3·H2O的电离平衡常数取Kb=2×10-5 mol·L-1)
分 析:
I、(1)由图象可知,常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,先反应生成碳酸氢钠,碳酸氢根再与盐酸反应生成碳酸,进而分解产生二氧化碳、水,①由反应及图象可知,在同一溶液中H2CO3与CO32-转化为HCO3-,故H2CO3、HCO3-、CO32-不能大量共存,故答案为:不能;(2)当溶液中c(HCO3-):c(CO32-)=2:1时,根据Kh==2×10-4,则有:c(OH-)==1×10-4,c(H+)==1×10-10,PH=-lg(10-10)=10,故答案为:10;(3)当溶液中H2CO3达到饱和后,开始放出CO2气体,由图象可以看出,当PH=6时,H2CO3达到饱和,开始放出CO2气体,故答案为:6;II、(1)常温下向25mL含HCl 0.01mol的溶液中滴加氨水时生成了铵根离子降低了溶液中的氢离子浓度此时平衡先正向移动,当盐酸反应完后溶液呈碱性时又对水的电离起到了抑制作用,使水的电离平衡逆向移动。当滴加氨水到25mL时,测得溶液中水的电离度最大说明恰好生成了氯化铵此时氨气的物质的量和氯化氢的物质的量相同都为0.01mol,则氨水的浓度为0.01/0.025=0.4mol/Lmol·L-1。(2) 将HA溶液加到Na2CO3溶液中有气体放出,说明HA的酸性比碳酸的强,NH4A溶液为中性,说明相同条件下,氨水和HA的电离程度相同,所以(NH4)2CO3中铵根离子的水解程度小于碳酸根离子的水解程度,所以溶液的pH>7;(3)由NH3·H2O的电离平衡常数得表达式Kb=c(NH4+)× c(OH-)/ c(NH3·H2O) 将数据带入c(NH4+)×1×10-7/ c(NH3·H2O)= 2×10-5 ,则c(NH4+) = 200c(NH3·H2O)所以在同一溶液中n(NH4+) = 200 n(NH3·H2O) = a mol,n(NH3·H2O)= a /200 所加氨水的浓度为a / 200b mol·L-1。
考点:
离子共存、盐类的水解、弱电解质的电离
已知Po原子核的质量为209.98287u,Pb原子核的质量为205.97446u,He原子核的质 2020-04-05 …
设有钚核Pu静止在匀强磁场中,当沿与磁场垂直的方向放出α粒子后,衰变成一个铀核,同时放出能量为E= 2020-04-05 …
实验室需要配置溶质质量分数为1%的下列溶液,若用自来水配置所配出的溶液中溶质质量分数不受影响的是{ 2020-05-24 …
1932年查德威克用α粒子去轰击铍核发现了中子,并产生一个新核.已知铍核的质量为9.01219u, 2020-07-01 …
边长为a的正方体木块(己知木块密度为ρ0)放入装有适量液体的烧杯中,待其静止后测出露出液面的高度为 2020-07-04 …
某工厂排放的废水中含有硫酸,原来采用氢氧化钠溶液处理,通过调节流量阀,使最终排出的溶液呈中性(如图 2020-07-11 …
分液漏斗分液时正确操作是哪个若分液时不小心有少量上层液体流下来,补救措施是用滴管将其从烧杯中吸出分离 2020-12-03 …
用量筒量取溶液,视线与量筒内液体的凹液面最低处保持水平,读数为15毫升;倒出部分液体后,俯视凹液面的 2020-12-05 …
如图是用来加速带电粒子的回旋加速器的示意图,其核心部分是两个D形金属盒,在加速带电粒子时,两金属盒置 2021-01-17 …
生活中的下列现象,用微粒的相关知识解释不正确的是()A.湿衣服晾在太阳底下干得快,说明微粒运动速率与 2021-01-28 …