早教吧作业答案频道 -->化学-->
(1)基态Ni原子的电子排布式为,该元素位于元素周期表的第族.(2)N、S形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是、(填化学式);酸根呈三角锥结构的酸是
题目详情
(1)基态Ni原子的电子排布式为___,该元素位于元素周期表的第___族.
(2)N、S形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是___、___(填化学式);酸根呈三角锥结构的酸是___.(填化学式)
(3)1molNH4BF4含有___mol配位键,Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有___mol σ键.
(4)过渡金属配合物Fe(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=___
(5)OF2分子构型为___,其中氧原子的杂化方式为___.
(6)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___形象化描述.在基态14C原子中,核外存在___对自旋相反的电子.
(2)N、S形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是___、___(填化学式);酸根呈三角锥结构的酸是___.(填化学式)
(3)1molNH4BF4含有___mol配位键,Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有___mol σ键.
(4)过渡金属配合物Fe(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=___
(5)OF2分子构型为___,其中氧原子的杂化方式为___.
(6)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___形象化描述.在基态14C原子中,核外存在___对自旋相反的电子.
▼优质解答
答案和解析
(1)Ni的原子序数为28,根据能量最低原理可写出电子排布式为1S22S22P63S23P63d84s2或[Ar]3d84s2,位于第四周期,第Ⅷ族,
故答案为:1s22s22p63s23p63d84s2或[Ar]3d84s2;Ⅷ;
(2)N、S元素形成的含氧酸有HNO2 HNO3、H2SO3、H2SO4,
NO2-中N原子价层电子对数是2+
=3,含1对孤电子对,所以为V形结构,
NO3-中N原子价层电子对数是3+
=3,不含孤电子对,所以为平面三角形,
SO32-中N原子价层电子对数是3+
=4,含1对孤电子对,所以为三角锥形,
SO42-中N原子价层电子对数是4+
=4,不含孤电子对,所以为正四面体,
故答案为:HNO2、HNO3、H2SO3;
(3)一个NH4BF4中N原子和其中一个H原子之间存在配位键、B原子和其中一个F原子之间存在一个配位键,所以含有2个配位键,则1mol NH4BF4含有2mol配位键,配合物Ni(CO)4的配离子中Ni原子和C原子之间有4个σ键,CO分子中C和O之间存在1个σ键,1个π键,1个配位键,因此4个CO有4个σ键,故1mol Ni(CO)4中含有8molσ键,
故答案为:2、8;
(4)过渡金属配合物Fe(CO)n的中心原子是铁原子,Fe是26元素,Fe原子核外电子排布为1s22s22p63s23p63d64s2,其价电子数是8,每个配体CO分子提供电子数为2,则8+2n=18,故n=5,
故答案为:5;
(5)OF2分子中O原子价层电子对个数=2+
(6-2)=4,为sp3杂化,且含有2个孤电子对,所以其空间构型为角形或V形,
故答案为:角形或V形;sp3;
(6)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用电子云形象化描述,离核近的区域电子云密度较大,离核远的区域电子云密度较小,C原子核外电子排布为1s22s22p2,轨道式为如图所示: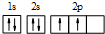 ,则在基态14C原子中,核外存在2对自旋相反的电子,
,则在基态14C原子中,核外存在2对自旋相反的电子,
故答案为:电子云;2.
故答案为:1s22s22p63s23p63d84s2或[Ar]3d84s2;Ⅷ;
(2)N、S元素形成的含氧酸有HNO2 HNO3、H2SO3、H2SO4,
NO2-中N原子价层电子对数是2+
| 5+1-2×2 |
| 2 |
NO3-中N原子价层电子对数是3+
| 5+1-2×3 |
| 2 |
SO32-中N原子价层电子对数是3+
| 6+2-2×3 |
| 2 |
SO42-中N原子价层电子对数是4+
| 6+2-2×4 |
| 2 |
故答案为:HNO2、HNO3、H2SO3;
(3)一个NH4BF4中N原子和其中一个H原子之间存在配位键、B原子和其中一个F原子之间存在一个配位键,所以含有2个配位键,则1mol NH4BF4含有2mol配位键,配合物Ni(CO)4的配离子中Ni原子和C原子之间有4个σ键,CO分子中C和O之间存在1个σ键,1个π键,1个配位键,因此4个CO有4个σ键,故1mol Ni(CO)4中含有8molσ键,
故答案为:2、8;
(4)过渡金属配合物Fe(CO)n的中心原子是铁原子,Fe是26元素,Fe原子核外电子排布为1s22s22p63s23p63d64s2,其价电子数是8,每个配体CO分子提供电子数为2,则8+2n=18,故n=5,
故答案为:5;
(5)OF2分子中O原子价层电子对个数=2+
| 1 |
| 2 |
故答案为:角形或V形;sp3;
(6)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用电子云形象化描述,离核近的区域电子云密度较大,离核远的区域电子云密度较小,C原子核外电子排布为1s22s22p2,轨道式为如图所示:
 ,则在基态14C原子中,核外存在2对自旋相反的电子,
,则在基态14C原子中,核外存在2对自旋相反的电子,故答案为:电子云;2.
看了 (1)基态Ni原子的电子排布...的网友还看了以下:
填写长方形、正方形的周长及面积公式.图形长方形正方形周长面积题型①:一根铁丝能围成一个长36厘米, 2020-04-09 …
用字母表示下面的计算公式和运算定律.正方形面积计算公式:长方形周长计算公式:乘法分配律用字母表示下 2020-05-13 …
三年级下的一道填空题:把4个边长是5厘米的正方形拼成一个长方形,周长减少()或()我算出来原来正方 2020-05-13 …
小弟提问:弧形周长、扇形周长、扇形面积公式、圆锥侧面积公式、圆柱面积都怎么求?还有几个等式小弟以前 2020-05-17 …
平面图形正方形周长公式和立体图形正方形周长公式相同吗? 2020-05-21 …
什么叫前柱式、前后柱式、周柱式、伪周柱式、双重周柱式、伪双重周柱式、圆形柱廊式 2020-06-27 …
小华用边长1厘米的正方形纸片分别摆出下面的图形,并依次写出计算每个图形周长的算式.小华是怎样想的? 2020-07-18 …
周长为20厘米的正方形,从中间剪开成为两个大小相等的长方形,这个小长方形周长是多少厘米?求列算式周 2020-07-20 …
1扇形周长公式因为扇形周长=半径×2+弧长,若半径为r,直径为R,扇形所对的圆心角的度数为n°为啥 2020-07-26 …
一、请写出周一至周日的英语缩写形式.二、填空.1、Therearedaysinaweek.2、ist 2021-02-15 …