早教吧作业答案频道 -->化学-->
钼酸钠(Na2MoO4)具有广泛的用途.可做新型水处理荆、优良的金属缓蚀剂及可用于局部过热的循环水系统;Al(OH)3工业和医药上都具有重要用途.现从某废钼催化剂(主要成分MoO3、Al2O3、F
题目详情
钼酸钠(Na2MoO4)具有广泛的用途.可做新型水处理荆、优良的金属缓蚀剂及可用于局部过热的循环水系统;Al(OH)3工业和医药上都具有重要用途.现从某废钼催化剂(主要成分MoO3、Al2O3、Fe2O3等)中回收Na2MoO4和Al(OH)3,其工艺如图:
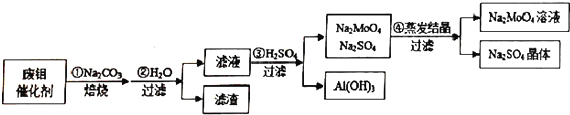
回答下列问题:
(1)已知MoO3、Al2O3与SiO2相似,均能在高温下跟Na2CO3发生类似反应,试写出MoO3与Na2CO3反应的化学方程式:___.
(2)第②步操作所后的滤液中,溶质有Na2MoO4、___和过量的Na2CO3;检验第②步操作所得滤渣中含有三价铁的方法是___.
(3)第③步操作H2SO4需要适量,通常是通过___来调控H2SO4的用量;与Na2SO4相比,Na2MoO4的溶解度受温度的影响变化___(填“较大”或“较小”).
(4)利用铝热反应可回收金属钼.将所得钼酸钠溶液用酸处理得到沉淀,再加热可得MoO3.写出MoO3发生铝热反应的化学方程式:___.
(5)取废钼催化剂5.00g,加入5.30gNa2CO3(足量),经上述实验操作后,最终得到2.34g Al(OH)3和6.39gNa2SO4晶体,则废钼催化剂中Al2O3、MoO3的物质的量的比值为___.

回答下列问题:
(1)已知MoO3、Al2O3与SiO2相似,均能在高温下跟Na2CO3发生类似反应,试写出MoO3与Na2CO3反应的化学方程式:___.
(2)第②步操作所后的滤液中,溶质有Na2MoO4、___和过量的Na2CO3;检验第②步操作所得滤渣中含有三价铁的方法是___.
(3)第③步操作H2SO4需要适量,通常是通过___来调控H2SO4的用量;与Na2SO4相比,Na2MoO4的溶解度受温度的影响变化___(填“较大”或“较小”).
(4)利用铝热反应可回收金属钼.将所得钼酸钠溶液用酸处理得到沉淀,再加热可得MoO3.写出MoO3发生铝热反应的化学方程式:___.
(5)取废钼催化剂5.00g,加入5.30gNa2CO3(足量),经上述实验操作后,最终得到2.34g Al(OH)3和6.39gNa2SO4晶体,则废钼催化剂中Al2O3、MoO3的物质的量的比值为___.
▼优质解答
答案和解析
(1)MoO3、Al2O3与Na2CO3的反应和SiO2与Na2CO3的反应相似,加入碳酸钠焙烧时可生成Na2MoO4和NaAlO2,MoO3与Na2CO3反应的化学方程式为MoO3+Na2CO3
Na2MoO4+CO2↑,
故答案为:MoO3+Na2CO3
Na2MoO4+CO2↑;
(2)高温条件下,氧化铝和碳酸钠反应生成NaAlO2,滤液中含有焙烧后生成Na2MoO4、NaAlO2以及过量的Na2CO3,检验第②步操作所得滤渣中含有三价铁,取少量滤渣洗涤液于试管中滴加几滴KSCN溶液,若溶液变红,则证明含三价铁,
故答案为:NaAlO2;取少量滤渣洗涤液于试管中滴加几滴KSCN溶液,若溶液变红,则证明含三价铁;
(3)第③步操作H2SO4需要适量,避免氢氧化铝溶解,通常是通过测溶液的pH来调控H2SO4的用量,转化关系中④蒸发结晶溶液得到硫酸钠晶体和Na2MoO4溶液,与Na2SO4相比,Na2MoO4的溶解度受温度的影响变化较小,硫酸钠溶解度收温度影响大,先析出晶体,
故答案为:测溶液的pH;较小;
(4)MoO3发生铝热铝反应,高温下和铝反应生成钼和氧化铝,反应的化学方程式为:4Al+2MoO3
2Mo+2Al2O3,
故答案为:4Al+2MoO3
2Mo+2Al2O3;
(5)加入稀硫酸后,滤渣为Al(OH)3,滤液中含有Na2SO4和Na2MoO4,已知:n(Na2CO3)=
=0.05mol,n(Na2SO4)=
=0.045mol,则Na2MoO4,由Na守恒可知n(Na2MoO4)=0.005mol,据此算出MoO3的物质的量为0.005mol,2.34g Al(OH)3的物质的量为
=0.03mol,据此算出Al2O3的物质的量为0.015mol,所以Al2O3、MoO3的物质的量的比值为0.015mol:0.005mol=3:1,
故答案为:3:1.
| ||
故答案为:MoO3+Na2CO3
| ||
(2)高温条件下,氧化铝和碳酸钠反应生成NaAlO2,滤液中含有焙烧后生成Na2MoO4、NaAlO2以及过量的Na2CO3,检验第②步操作所得滤渣中含有三价铁,取少量滤渣洗涤液于试管中滴加几滴KSCN溶液,若溶液变红,则证明含三价铁,
故答案为:NaAlO2;取少量滤渣洗涤液于试管中滴加几滴KSCN溶液,若溶液变红,则证明含三价铁;
(3)第③步操作H2SO4需要适量,避免氢氧化铝溶解,通常是通过测溶液的pH来调控H2SO4的用量,转化关系中④蒸发结晶溶液得到硫酸钠晶体和Na2MoO4溶液,与Na2SO4相比,Na2MoO4的溶解度受温度的影响变化较小,硫酸钠溶解度收温度影响大,先析出晶体,
故答案为:测溶液的pH;较小;
(4)MoO3发生铝热铝反应,高温下和铝反应生成钼和氧化铝,反应的化学方程式为:4Al+2MoO3
| ||
故答案为:4Al+2MoO3
| ||
(5)加入稀硫酸后,滤渣为Al(OH)3,滤液中含有Na2SO4和Na2MoO4,已知:n(Na2CO3)=
| 5.30g |
| 106g/mol |
| 6.39g |
| 142g/mol |
| 2.34g |
| 78g/mol |
故答案为:3:1.
看了 钼酸钠(Na2MoO4)具有...的网友还看了以下:
钼是稀有矿产资源,主要用于航天合金材料制作。在元素周期表中钼元素的某些信息如图所示。下列有关钼的说 2020-05-13 …
这句话用英语要怎么讲?“难道我能实现小时候的理想,注意是理想,这也太不公平了吧”,准确一点,就是注 2020-05-16 …
金属铬和钼的电阻哪个大 2020-05-17 …
如图,点O为平行四边形ABCD的对称中心,过点O任作直线EF,分别交AD,BC于点E,F.请问用平 2020-05-17 …
学习了鱼游到了纸上,我明白了什么道理?⊙ o ⊙ 急用( ⊙ o ⊙ 2020-05-17 …
下列代理行为中,属于滥用代理权的有( )o A.超越代理权进行代理 B.代理人与第三人恶 2020-05-19 …
已知:如图,PA切⊙O于A点,PO∥AC,BC是⊙O的直径.请问:直线PB是否与⊙O相切?说明你的 2020-06-15 …
钼(元素符号Mo)是银灰色的难熔金属,常见化合价为+6、+5、+4,常温下钼在空气中很稳定,高于6 2020-06-26 …
2011年,瑞士洛桑联邦工学院无理学家发现后用一种辉钼(MoS2)单分子层材料制造半导体,比传统硅 2020-06-26 …
三氧化钼和二氧化钼的区别 2020-06-28 …