早教吧作业答案频道 -->化学-->
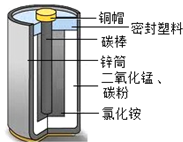
酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是有碳粉、MnO2、NH4Cl等组成的糊状填充物,其结构如下图.该电池在放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2
题目详情
酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是有碳粉、MnO2、NH4Cl等组成的糊状填充物,其结构如下图.该电池在放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH
回收处理该废旧电池可以得到多种化工原料,有关数据下图所示:溶解度/(g/100g水)
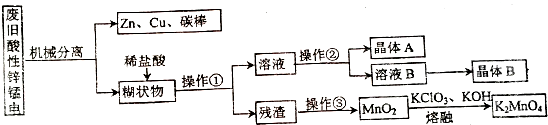
某化学课外小组设计了如下废旧电池综合利用工艺(不考虑废旧电池中实际存在的少量其他金属):
回答下列问题:
(1)该酸性锌锰干电池放电时的正极反应式为___;
(2)晶体A的化学式为___;
(3)操作③的名称为___;
(4)从MnO2获得K2MnO4的反应方程式为___;
(5)用废电池的锌皮制作ZnSO4•7H2O,需去除少量杂质铁,其方法是:
①加入足量的稀H2SO4和H2O2溶解.加入H2O2反应的离子方程式是___;
②加碱调节pH为___,使铁刚好完全沉淀,过滤.向滤液中继续加碱调节pH使锌刚好完全沉淀.过滤、洗涤.
③将沉淀溶于稀H2SO4,经过___(答操作名称)、过滤、洗涤、干燥得到ZnSO4•7H2O,晶体用冷水洗涤的原因是___.
回收处理该废旧电池可以得到多种化工原料,有关数据下图所示:溶解度/(g/100g水)
| 温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |

回答下列问题:

(1)该酸性锌锰干电池放电时的正极反应式为___;
(2)晶体A的化学式为___;
(3)操作③的名称为___;
(4)从MnO2获得K2MnO4的反应方程式为___;
(5)用废电池的锌皮制作ZnSO4•7H2O,需去除少量杂质铁,其方法是:
①加入足量的稀H2SO4和H2O2溶解.加入H2O2反应的离子方程式是___;
②加碱调节pH为___,使铁刚好完全沉淀,过滤.向滤液中继续加碱调节pH使锌刚好完全沉淀.过滤、洗涤.
③将沉淀溶于稀H2SO4,经过___(答操作名称)、过滤、洗涤、干燥得到ZnSO4•7H2O,晶体用冷水洗涤的原因是___.
▼优质解答
答案和解析
(1)原电池的正极应是氧化剂发生还原反应,根据原电池的总反应Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH可知正极反应式为MnO2+e-+NH4+=MnOOH+NH3,
故答案为:MnO2+e-+NH4+=MnOOH+NH3;
(2)废电池经机械分离后,糊状物主要为MnO2、MnOOH、NH4Cl、碳粉、Zn(NH3)2Cl2等.加稀盐酸溶解得到氯化铵和氯化锌溶液,过滤得残渣主要为MnO2、MnOOH、碳粉,残渣在空气中灼烧碳被氧化成二氧化碳,MnOOH被氧化成二氧化锰,二氧化锰在碱性高温的条件下被氯酸钾氧化成锰酸钾,根据氯化铵和氯化锌的溶解度可知,混合溶液经浓缩后过滤可得晶体A为NH4Cl,再将滤液蒸发结晶可得晶体B为氯化锌,
故答案为:NH4Cl;
(3)根据(2)中的分析可知操作③的名称为在空气中灼烧,
故答案为:在空气中灼烧;
(4)根据流程可知,二氧化锰在碱性高温的条件下被氯酸钾氧化成锰酸钾,反应的化学方程式为3MnO2+KClO3+6KOH
3K2MnO4+KCl+3H2O,
故答案为:3MnO2+KClO3+6KOH
3K2MnO4+KCl+3H2O;
(5)锌皮含有少量杂质铁,溶于稀硫酸和双氧水,得硫酸锌和硫酸铁混合溶液,调节pH值使铁刚好完全沉淀,锌不沉淀,过滤除去铁,再调节pH值使锌生成氢氧化锌沉淀,将氢氧化锌溶于硫酸得硫酸锌溶液,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到ZnSO4•7H2O,
①加入H2O2氧化亚铁离子,反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②根据Fe(OH)3的Ksp可知,铁离子沉淀完全时,溶液中c(OH-)=
=1×10-11 mol/L,所以溶液的pH值为3,使铁刚好完全沉淀,
故答案为:3;
③硫酸锌溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到ZnSO4•7H2O,晶体用冷水洗涤的原因是降低晶体的溶解度,减少损失,
故答案为:蒸发浓缩、冷却结晶;降低晶体的溶解度,减少损失.
故答案为:MnO2+e-+NH4+=MnOOH+NH3;
(2)废电池经机械分离后,糊状物主要为MnO2、MnOOH、NH4Cl、碳粉、Zn(NH3)2Cl2等.加稀盐酸溶解得到氯化铵和氯化锌溶液,过滤得残渣主要为MnO2、MnOOH、碳粉,残渣在空气中灼烧碳被氧化成二氧化碳,MnOOH被氧化成二氧化锰,二氧化锰在碱性高温的条件下被氯酸钾氧化成锰酸钾,根据氯化铵和氯化锌的溶解度可知,混合溶液经浓缩后过滤可得晶体A为NH4Cl,再将滤液蒸发结晶可得晶体B为氯化锌,
故答案为:NH4Cl;
(3)根据(2)中的分析可知操作③的名称为在空气中灼烧,
故答案为:在空气中灼烧;
(4)根据流程可知,二氧化锰在碱性高温的条件下被氯酸钾氧化成锰酸钾,反应的化学方程式为3MnO2+KClO3+6KOH
| ||
故答案为:3MnO2+KClO3+6KOH
| ||
(5)锌皮含有少量杂质铁,溶于稀硫酸和双氧水,得硫酸锌和硫酸铁混合溶液,调节pH值使铁刚好完全沉淀,锌不沉淀,过滤除去铁,再调节pH值使锌生成氢氧化锌沉淀,将氢氧化锌溶于硫酸得硫酸锌溶液,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到ZnSO4•7H2O,
①加入H2O2氧化亚铁离子,反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②根据Fe(OH)3的Ksp可知,铁离子沉淀完全时,溶液中c(OH-)=
| 3 |
| ||
故答案为:3;
③硫酸锌溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到ZnSO4•7H2O,晶体用冷水洗涤的原因是降低晶体的溶解度,减少损失,
故答案为:蒸发浓缩、冷却结晶;降低晶体的溶解度,减少损失.
看了 酸性锌锰干电池是一种一次性电...的网友还看了以下:
“壳”的读音‘壳’有两个读音,qiào和ké,两个都是‘坚硬的外皮’的意思,那么,应该何时读qià 2020-04-05 …
最近电茶壶等不锈钢食具容器安全问题引起消费者关注.不锈钢中有铁、碳、硅和锰.有些食具容器所用不锈钢 2020-06-14 …
有谁了解锰?金属锰粉,加极少量胶水,压结成一个个3厘米见方的块状,然后放入烤箱内高温烘烤数小时.这 2020-06-26 …
下列词语中划线字的读音,全都正确的的一组是(3分)()A.攻讦jié耸峙shì鹰隼shǔn干瘪bi 2020-07-02 …
下列词语中加点的字,读音全部正确的一项是()A.顷刻(qǐnɡ)混沌(hún)狩猎(shòu)悬崖 2020-07-28 …
锰酸根怎么写?您好,问你个问题,高锰酸根和锰酸根是不是除了化合价以及所带电荷数不同,其余的书写方面的 2020-11-20 …
1.下图是几种软体动物的贝壳。大多数的软体动物都具有贝壳,这些贝壳有着独特的形状和美丽的色彩,深受人 2020-11-24 …
A.桎梏gùB.标识zhìC.蹑足nièD.估价gū按捺nà卡壳kǎ胡诌zhōu训诂gǔ撂手不管li 2020-12-09 …
选出下面各项中字音有误的一项:A诡谲jué角逐jué咀嚼jué龟裂jūnB龟兹qiūcí皲裂jūn玷 2020-12-17 …
金属锰具有广泛的用途,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO 2021-02-19 …