早教吧作业答案频道 -->化学-->
氧化还原反应在生产和生活中使用非常广泛.I、NaNO2外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O.(1)上述反应中用单线桥标出电
题目详情
氧化还原反应在生产和生活中使用非常广泛.
I、NaNO2外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:
2NaNO2+4HI═2NO↑+I2+2NaI+2H2O.
(1)上述反应中用单线桥标出电子转移的方向和数目.
(2)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是___.
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
II.过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.根据下列反应回答问题:
A.Na2O2+2HCl═2NaCl+H2O2
B.Ag2O+H2O2═2Ag+O2↑+H2O
C.2H2O2═2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
(3)上述反应中,H2O2仅体现氧化性的反应是(填序号)___.
(4)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是___
(5)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO4-、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.
①将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中
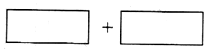
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为___mol.
I、NaNO2外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:
2NaNO2+4HI═2NO↑+I2+2NaI+2H2O.
(1)上述反应中用单线桥标出电子转移的方向和数目.
(2)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是___.
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
II.过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.根据下列反应回答问题:
A.Na2O2+2HCl═2NaCl+H2O2
B.Ag2O+H2O2═2Ag+O2↑+H2O
C.2H2O2═2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
(3)上述反应中,H2O2仅体现氧化性的反应是(填序号)___.
(4)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是___
(5)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO4-、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.
①将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中
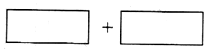
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为___mol.
▼优质解答
答案和解析
(1)N元素的化合价由+3降低为+2,I元素的化合价由-1升高为0,则双线桥表示电子转移的方向和数目为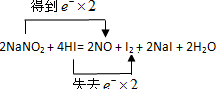 ,
,
故答案为: ;
;
(2)NaNO2→N2是被还原,必须加还原剂;N元素氧化性弱于O和Cl元素,故只能加NH4Cl作还原剂.方程式为NaNO2+NH4Cl═NaCl+N2↑+2H2O,亚硝酸钠中氮得到3电子指向氮气中的氮,氯化铵中氮失去3电子指向氮气中的氮,
故答案为:B;
(3)A中无元素的化合价变化,B中Ag元素的化合价降低、双氧水中O元素的化合价升高,B中过氧化氢具有还原性,C中双氧水中氧元素化合价升高也降低,体现还原性和氧化性,只有D中双氧水中氧元素化合价降低,说明双氧水作氧化剂,体现了氧化性,故答案为:D;
(4)反应Ag2O+H2O2=2Ag+O2↑+H2O中,氧化银做氧化剂,双氧水作还原剂,则氧化性Ag2O>H2O2,反应3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O中,双氧水做氧化剂,铬酸钾做氧化产物,则氧化性H2O2>K2CrO4,则氧化性顺序为Ag2O>H2O2>K2CrO4,
故答案为:Ag2O>H2O2>K2CrO4.
(5)①该反应过程中,高锰酸根的氧化性和双氧水的还原性导致二者间发生氧化还原反应,高锰酸根离子中锰元素从+7变为+2价,化合价降低5价,双氧水中氧元素化合价从-1价变为0价,化合价至少升高2价,则高锰酸根离子的系数为2,双氧水的系数为5,然后利用质量守恒配平可得该反应的离子方程式为:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,
故答案为:2MnO4-+5H2O2;
②上述反应中生成5mol氧气转移电子10mol,当反应中有6.72L(标准状况)即0.3mol氧气生成时,则转移的电子为:10mol×
=0.6mol,
故答案为:0.6.
 ,
,故答案为:
 ;
;(2)NaNO2→N2是被还原,必须加还原剂;N元素氧化性弱于O和Cl元素,故只能加NH4Cl作还原剂.方程式为NaNO2+NH4Cl═NaCl+N2↑+2H2O,亚硝酸钠中氮得到3电子指向氮气中的氮,氯化铵中氮失去3电子指向氮气中的氮,
故答案为:B;
(3)A中无元素的化合价变化,B中Ag元素的化合价降低、双氧水中O元素的化合价升高,B中过氧化氢具有还原性,C中双氧水中氧元素化合价升高也降低,体现还原性和氧化性,只有D中双氧水中氧元素化合价降低,说明双氧水作氧化剂,体现了氧化性,故答案为:D;
(4)反应Ag2O+H2O2=2Ag+O2↑+H2O中,氧化银做氧化剂,双氧水作还原剂,则氧化性Ag2O>H2O2,反应3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O中,双氧水做氧化剂,铬酸钾做氧化产物,则氧化性H2O2>K2CrO4,则氧化性顺序为Ag2O>H2O2>K2CrO4,
故答案为:Ag2O>H2O2>K2CrO4.
(5)①该反应过程中,高锰酸根的氧化性和双氧水的还原性导致二者间发生氧化还原反应,高锰酸根离子中锰元素从+7变为+2价,化合价降低5价,双氧水中氧元素化合价从-1价变为0价,化合价至少升高2价,则高锰酸根离子的系数为2,双氧水的系数为5,然后利用质量守恒配平可得该反应的离子方程式为:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,
故答案为:2MnO4-+5H2O2;
②上述反应中生成5mol氧气转移电子10mol,当反应中有6.72L(标准状况)即0.3mol氧气生成时,则转移的电子为:10mol×
| 0.3mol |
| 5 |
故答案为:0.6.
看了氧化还原反应在生产和生活中使用...的网友还看了以下:
选出每组单词中划括号部分读音不同的一项.1.A:t(o)day.B:t(o)morrow.C:st 2020-04-26 …
用所给字母拼成单词.1.a,l,a,d,s.2.a,d,o,s.3.c,o,r,p,n用所给字母拼 2020-05-15 …
英语单词辨音找出画()部分读音与其余不同的单词()1.A .kn(ee) B.n(e)ck C.r 2020-05-17 …
矩阵A为4阶方阵,R(A)=3,A^2+A=O,求|A+2E|如题 2020-06-06 …
设直线l的方程为(a+1)x-y+2-a=o(a∈R)(1)若L在两坐标轴上截距相等,求L的方程( 2020-06-07 …
点A、B、O分别以5个单位/s,2单位/s,1单位/s的速度向右移运动,几秒后,o点恰好成为线段中 2020-06-15 …
质点沿X轴运动,其加速器和位置的关系为a=2+6x∧2,a的单位为m╱s∧2,质点沿X轴运动,其加 2020-06-22 …
y=a^2与函数y=|a^x-2|(a>o,且a不等于一)的图像有两个公共点则a的取值范围是? 2020-06-27 …
2/a是单项式,系数是2,对吗?ab/2是二项式,系数是1/2对吗?a2-b2是多项式,其各项系数和 2020-12-23 …
2/a是单项式,系数是2,ab/2是二项式,系数是1/2对吗?a2-b2是多项式,其各项系数和等于0 2020-12-23 …