2gCu2S和CuS的混合物在酸性溶液中用400mL0.075mol·L-1KMnO4溶液处理,发生反应如下:8+5Cu2S+44H+10Cu2++5SO2+8Mn2++22H2O6+5CuS+28H+5Cu2++5SO2+6Mn2++14H2O反应后煮沸
8![]() +5Cu 2 S+44H +
+5Cu 2 S+44H + ![]() 10Cu 2+ +5SO 2 +8Mn 2+ +22H 2 O
10Cu 2+ +5SO 2 +8Mn 2+ +22H 2 O
6![]() +5CuS+28H +
+5CuS+28H + ![]() 5Cu 2+ +5SO 2 +6Mn 2+ +14H 2 O
5Cu 2+ +5SO 2 +6Mn 2+ +14H 2 O
反应后煮沸溶液,赶尽SO 2 ,剩余的KMnO 4 恰好与350 mL 0.1 mol·L -1 (NH 4 ) 2 Fe(SO 4 ) 2 溶液完全反应。
(1)配平KMnO 4 与(NH 4 ) 2 Fe(SO 4 ) 2 反应的离子方程式:
□![]() +□Fe 2+ +□H +
+□Fe 2+ +□H + ![]() □Mn 2+ +□Fe 3+ +□H 2 O
□Mn 2+ +□Fe 3+ +□H 2 O
(2)KMnO 4 溶液与混合物反应后,剩余KMnO 4 的物质的量为_____________mol。
(3)欲配制500 mL 0.1 mol·L -1 Fe 2+ 溶液,需称取(NH 4 ) 2 Fe(SO 4 ) 2 ·6H 2 O(M=
(4)混合物中Cu 2 S的质量分数为_____________。
解析:方程式可用化合价升降法、观察法配平。与(NH 4 ) 2 Fe(SO 4 ) 2 反应的KMnO 4 即为与混合物反应剩余的,依据(1)所配平的反应方程式![]() +5Fe 2+ +8H +
+5Fe 2+ +8H + ![]() Mn 2+ +5Fe 3+ +4H 2 O,可以看出反应的KMnO 4 与(NH 4 ) 2 Fe(SO 4 ) 2 的物质的量之比为1∶5,故剩余的KMnO 4 为0.007 mol。
Mn 2+ +5Fe 3+ +4H 2 O,可以看出反应的KMnO 4 与(NH 4 ) 2 Fe(SO 4 ) 2 的物质的量之比为1∶5,故剩余的KMnO 4 为0.007 mol。
由(2)可知与混合物反应的高锰酸钾的物质的量为:
设原混合物中含Cu 2 S的质量为x,CuS的质量为y。
8KMnO 4 —5Cu 2 S 6KMnO 4 —5CuS
x/160 y/96
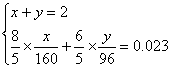
解得x=0.8,故Cu 2 S的质量分数为40%。
答案:(1)1 5 8 1 5 4 (2)0.007 (3)19.6 (4)40%
250C,将O.4mol/LCH3COOH溶液和O.2mol/LNaOH溶液各1OOmL混合后,p 2020-05-13 …
::”:“:”:若PH=3的酸溶液和PH=11的碱溶液等体积混合后溶液呈酸性 其原因可能是A 弱酸 2020-05-16 …
化学的酚酞石蕊.下列各组物质中,能用紫色石蕊溶液鉴别的是 [ ] A.稀硫酸和醋酸溶液 B.稀盐酸 2020-05-17 …
实验①:向盛有0.1mol/LAgNO3溶液的试管中滴加0.1mol/L的NaCl溶液至不再有白色 2020-05-17 …
室温下,某一定量的水中最多溶解10gNaCO3.先预向这一定量的水中加入8gNa2CO3,所得溶液 2020-06-25 …
下列各组物质能反应,且充分反应后所得溶液质量比反应前溶液总质量增大的是()A.铁粉和硫酸铜溶液B. 2020-07-16 …
什么碱溶液和盐什么溶液反应生成蓝色固体A溶液是盐B溶液是碱C溶液是氯化物A溶液+B溶液=无色液体+ 2020-07-29 …
〔1〕氢溴酸与碳酸钙〔2〕氢氧化钡与二氧化碳〔3〕镁条与氢溴酸〔4〕氢氧化钡溶液和氯化钡溶液〔5〕铁 2020-11-05 …
一道化学平衡问题常温下,将0.2mol/L的某一元酸HA溶液和0.1mol/LNaOH溶液等体积混合 2021-01-22 …
下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是()A.铁和稀硫酸B.氢氧化钾溶液中 2021-02-18 …