一定温度下,有两个体积均为2L的恒容密闭容器I和Ⅱ,向I中加入1molCO和2molH2,向Ⅱ中加入2molCO和4molH2,均发生下列反应并建立平衡:CO(g)+2H2(g)⇌CH3OH(g).测得不同温度下CO平衡
一定温度下,有两个体积均为2L的恒容密闭容器I和Ⅱ,向I中加入1 mol CO和2 mol H2,向Ⅱ中加入2 mol CO和4 mol H2,均发生下列反应并建立平衡:CO(g)+2H2(g)⇌CH3OH(g).测得不同温度下CO平衡转化率如图所示.下列说法正确的是( )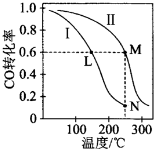
A. 该反应的△H>0
B. N点化学平衡常数K=0.59
C. L、M两点容器内压强:P(M)>2P(L)
D. 向N点平衡体系中再加入1 mol CH3OH,建立新平衡时被分解的CH3OH物质的量小于0.4 mol
B.依据化学平衡三行计算列式计算M点平衡浓度,CO转化率为60%,
CO(g)+2H2(g)⇌CH3OH(g)
起始量(mol/L) 1 2 0
变化量(mol/L) 0.6 1.2 0.6
平衡量(mol/L) 0.4 0.8 0.6
计算平衡常数K=
| c(CH3OH) |
| c(CO)c(H2)2 |
| 0.6 |
| 0.4×0.82 |
C.L、M两点是不同温度下的平衡,压强和气体物质的量成正比,CO转化率为60%,
CO(g)+2H2(g)⇌CH3OH(g)
起始量(mol) 1 2 0
变化量(mol) 0.6 1.2 0.6
平衡量(mol) 0.4 0.8 0.6
CO(g)+2H2(g)⇌CH3OH(g)
起始量(mol) 2 4 0
变化量(mol) 1.2 2.4 1.2
平衡量(mol) 0.8 1.6 1.2
所以L、M两点容器内压强之比等于气体物质的量之比=(0.4+0.8+0.6):( 0.8+1.6+1.2)=1.8:3.6=1:2
P(M)=2P(L),但温度升高,M点压强增大,P(M)>2P(L),故C正确;
D.N点平衡体系中再加入1 mol CH3OH,相当于Ⅰ中再加入1molmol CO和2 mol H2,最后达到平衡状态和向Ⅱ中加入2 mol CO和4 mol H2的平衡状态相同,甲醇最后平衡状态为1.2mol,CO转化率60%,则相当于逆向进行甲醇分解率为40%,加入1mol甲醇增大压强平衡正向进行,则分解率小于40%,分解的甲醇小于0.4 mol,故D正确;
故选CD.
)(1111:44:57) 以下关于加速度的说法中,正确的是()A.加速度为0的物体一定处于静止状 2020-04-27 …
正电荷在B点 和O点的加速度哪个大?为什么我看到的电场线密度是O的大?O点在水平的那条电场线上, 2020-05-16 …
物体在粗糙的斜面低端O以初速度v沿斜面上滑,到最高点P后又滑回到O点说法正确的是:A:上滑下滑加速 2020-07-01 …
如图所示,O点为弹簧振子的平衡位置,小球在B、C间做无摩擦的往复运动.在小球向O点运动的过程中,小球 2020-11-01 …
一个物体从静止开始以a1的加速度从O点出发做匀加速直线运动,经过某一点A,又以a2的加速度做匀减速直 2020-11-29 …
说明理由1.已知反应2O3→O2+O的反应机理为O3→O2+O(慢),O3+O→2O2(快),当O2 2020-12-09 …
关于速度和加速度的下列说法中,正确的是()A.速度越大,加速度一定越大B.速度为零时,加速度一定为零 2020-12-09 …
关于速度与加速度,下列说法中正确的()A.物体加速度不为零,速度一定为零B.加速度为零,物体的速度也 2021-01-29 …
比较正在做直线运动的两个物体的速度和加速度,下列说法中正确的是()A.速度较大的物体加速度一定大B. 2021-01-29 …
关于物体运动的速度和加速度的关系,下列说法正确的是()A.物体的加速度为零,速度一定为零B.速度变化 2021-01-29 …