早教吧作业答案频道 -->化学-->
X、Y、Z、R、W为前四周期元素且原子序数依次增大.Y和R同主族;X、R原子中未成对电子数之比为3:2;Z与Y可以形成两种原子个数比分别为1:1和2:1固态化合物;W3+中有5个未成对电子.请回
题目详情
X、Y、Z、R、W为前四周期元素且原子序数依次增大.Y和R同主族;X、R原子中未成对电子数之比为3:2;Z与Y可以形成两种原子个数比分别为1:1和2:1固态化合物;W 3+中有5个未成对电子.
请回答下列问题:
(1)写出Z和Y原子个数比为1:1的化合物的电子式___.
(2)W基态原子的核外电子排布式是___.
(3)X、Y、R原子的第一电离能从小到大的关系为(用元素符号,下同)___,
(4)与X的气态氢化物互为等电子体的分子、离子有___、___(各举一例)
(5)W单质与足量的Y单质在点燃条件下充分发生反应,生成一种黑色固体.为了确定该固体的组成,先将固体溶于足量稀硫酸中,向所得溶液中分别滴入下列试剂即可,符合试剂是___.(代号填空)
A.氯水 B.NaOH溶液 C.KSCN溶液 D.KMnO4溶液
(6)W的一种含氧酸根WO42-具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是___.
(7)在离子晶体中正、负离子间力求尽可能多的接触,以降低体系的能量,使晶体稳定存在.已知Na+半径是Cl-的a倍,Cs+半径是Cl-的b倍,请回顾课本上NaCl和CsCl的晶胞,其晶胞边长比为___.
请回答下列问题:
(1)写出Z和Y原子个数比为1:1的化合物的电子式___.
(2)W基态原子的核外电子排布式是___.
(3)X、Y、R原子的第一电离能从小到大的关系为(用元素符号,下同)___,
(4)与X的气态氢化物互为等电子体的分子、离子有___、___(各举一例)
(5)W单质与足量的Y单质在点燃条件下充分发生反应,生成一种黑色固体.为了确定该固体的组成,先将固体溶于足量稀硫酸中,向所得溶液中分别滴入下列试剂即可,符合试剂是___.(代号填空)
A.氯水 B.NaOH溶液 C.KSCN溶液 D.KMnO4溶液
(6)W的一种含氧酸根WO42-具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是___.
(7)在离子晶体中正、负离子间力求尽可能多的接触,以降低体系的能量,使晶体稳定存在.已知Na+半径是Cl-的a倍,Cs+半径是Cl-的b倍,请回顾课本上NaCl和CsCl的晶胞,其晶胞边长比为___.
▼优质解答
答案和解析
X、Y、Z、R、W为前四周期元素且原子序数依次增大.Z与Y可以形成两种原子个数比分别为1:1和2:1固态化合物,则Z为钠元素,Y为氧元素;Y和R同主族,则R为硫元素;X、R原子中未成对电子数之比为3:2,则X为氮元素,W3+中有5个未成对电子,只能处于第四周期,则W为铁元素.
(1)Z和Y原子个数比为1:1的化合物为过氧化钠,它的电子式为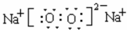 ,
,
故答案为: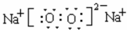 ;
;
(2)W为铁元素,26号元素,它的基态原子的核外电子排布式是 1s22s22p63s23p63d63s2,
故答案为:1s22s22p63s23p63d63s2;
(3)氮原子中2p能级容纳3个电子,为半充满状态,能量较低,所以氮的第一电离能高于相邻的同周期元素,O、S同主族,自上而下第一电离能减小,故第一电离能从小到大的关系为:S故答案为:S(4)原子总数相同、价电子总数相同的微粒互为等电子体,与NH3互为等电子体的分子PH3 等、离子有H3O+或等,
故案为:PH3;H3O+;
(5)Fe单质与足量的氧气在点燃条件下充分发生反应,生成一种黑色固体可能为FeO、Fe3O4或二者混合物,为了确定该固体的组成,先将固体溶于足量稀硫酸中,因为所得溶液中有铁离子和亚铁离子,可以通过KSCN溶液呈血红色来检验铁离子的存在,通过KMnO4溶液能褪色,证明亚铁离子的存在,
故答案为:CD;
(6)含氧酸根FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,有Fe3+生成,并有无色气体产生,结合电子转移守恒可知,只有氧元素被氧化,故该无色气体为O2,反应离子方程式为:4FeO42-+20 H+=4Fe3++3O2↑+10H2O,
故答案为:4FeO42-+20 H+=4Fe3++3O2↑+10H2O;
(7)设Cl-的半径为1,则Na+半径为a,Cs+半径为b,氯化钠的晶胞结构如图所示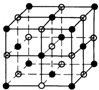 ,晶胞的边长为2(1+a);氯化铯的晶胞结构为
,晶胞的边长为2(1+a);氯化铯的晶胞结构为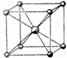 ,晶胞的体对角线长度为2(1+b),则晶胞的边长为
,晶胞的体对角线长度为2(1+b),则晶胞的边长为
×2(1+b),所以氯化钠与氯化铯的晶胞边长比为2(1+a):
×2(1+b)=
,
故答案为:
.
(1)Z和Y原子个数比为1:1的化合物为过氧化钠,它的电子式为
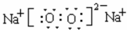 ,
,故答案为:
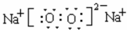 ;
;(2)W为铁元素,26号元素,它的基态原子的核外电子排布式是 1s22s22p63s23p63d63s2,
故答案为:1s22s22p63s23p63d63s2;
(3)氮原子中2p能级容纳3个电子,为半充满状态,能量较低,所以氮的第一电离能高于相邻的同周期元素,O、S同主族,自上而下第一电离能减小,故第一电离能从小到大的关系为:S
故案为:PH3;H3O+;
(5)Fe单质与足量的氧气在点燃条件下充分发生反应,生成一种黑色固体可能为FeO、Fe3O4或二者混合物,为了确定该固体的组成,先将固体溶于足量稀硫酸中,因为所得溶液中有铁离子和亚铁离子,可以通过KSCN溶液呈血红色来检验铁离子的存在,通过KMnO4溶液能褪色,证明亚铁离子的存在,
故答案为:CD;
(6)含氧酸根FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,有Fe3+生成,并有无色气体产生,结合电子转移守恒可知,只有氧元素被氧化,故该无色气体为O2,反应离子方程式为:4FeO42-+20 H+=4Fe3++3O2↑+10H2O,
故答案为:4FeO42-+20 H+=4Fe3++3O2↑+10H2O;
(7)设Cl-的半径为1,则Na+半径为a,Cs+半径为b,氯化钠的晶胞结构如图所示
 ,晶胞的边长为2(1+a);氯化铯的晶胞结构为
,晶胞的边长为2(1+a);氯化铯的晶胞结构为 ,晶胞的体对角线长度为2(1+b),则晶胞的边长为
,晶胞的体对角线长度为2(1+b),则晶胞的边长为
| ||
| 3 |
| ||
| 3 |
| ||
| (1+b) |
故答案为:
| ||
| (1+b) |
看了X、Y、Z、R、W为前四周期元...的网友还看了以下:
如图是大豆种子结构示意图,请据图回答(1)能贮藏营养物质的结构是4(2)我们吃的黄豆芽的主要部分就 2020-05-17 …
1.盲人皮肤内的()感受器比视力正常的人敏锐,它在人体的什么部位比较集中?2.能感受空气中气体的分 2020-06-07 …
某淘宝商城专营店经销某种产品,已知每个月的利润Y(单位:万元)是关于该月的交易量X(单位:件)的一 2020-06-11 …
五、选词填空.依然毅然竟然1.他()不顾大家的反对,()冲进了大雨中.2.在这千钧一五、选词填空. 2020-06-23 …
选择加黑词语的正确意思1.“沉思”的“沉”字的正确意思应是[]A.重量大B.深入,程度深C.没入水 2020-06-27 …
黄金周旅游人数2800年比2007年同期增长2.3%说2.3%的具体意义今年产量比去年增产二成.黄 2020-07-15 …
写出适当的符号或符号中“2”的意义①构成氯化钠的粒子、;②画出镁离子的结构示意图;③O2-中“2” 2020-07-22 …
请根据下列提示写出相应短语。1.在狱中2.一定会3.不会遭到 2020-11-10 …
生态系统中的能量流动的特点是()A.循环流动,逐级递减B.循环流动,逐级增加C.单向流动,逐级增中D 2020-11-28 …
谁能帮我回答一下啊一、单选题1.如果流动资产大于流动负债,则月末用现金偿还一般应付账款会使()。A. 2020-12-15 …