早教吧作业答案频道 -->化学-->
丙烷制备丙烯已成为制备丙烯的重要方法之一.方法I:丙烷脱氢制丙烯:①C3H8(g)催化剂△C3H6(g)+H2(g)△H1方法II:丙烷氧化脱氢制
题目详情
丙烷制备丙烯已成为制备丙烯的重要方法之一.
方法 I:丙烷脱氢制丙烯:
①C3H8(g)
C3H6(g)+H2(g)△H1
方法 II:丙烷氧化脱氢制丙烯:(投料为C3H8和CO2)
②C3H8(g)+CO2(g)
C3H6(g)+CO(g)+H2O(g)△H2=165kJ•mol-1
③CO2(g)+H2(g)
CO(g)+H2O(g)△H3=41kJ•mol-1
已知:
(1)计算△H1=___kJ•mol-1
(2)模拟方法 I制丙烯,在体积可变的反应器中,恒温,维持体系总压强恒定为0.1MPa,加入1mol C3H8(g)时体积为50L,再加入8.5mol水蒸汽作为稀释剂,反应t分钟达到平衡,测得丙烷0.5mol,已知:分压=物质的量分数×总压强.
①计算该温度下反应I的平衡常数K=___.
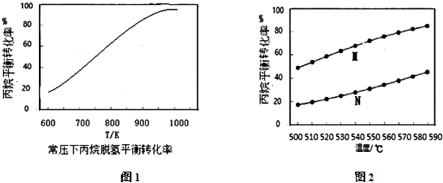
②常压下,温度为600K~1000K,水烃比M=10(水烃比是指投料中水蒸汽和丙烷的物质的量之比)时丙烷脱氢平衡转化率与温度变化的曲线如图1,在图1中画出水烃比M=8时的曲线.
(3)模拟方法 II制丙烯,在恒温恒容条件下充入物质的量之比为1:1的丙烷和二氧化碳气体,一段时间后达到平衡,则下列可以判断容器内反应体系达到平衡的是___.
A.v正(C3H8)=v逆(C3H6) B.平均相对分子质量不再变化
C.气体密度不再变化 D.丙烷和二氧化碳的物质的量比值不再变化
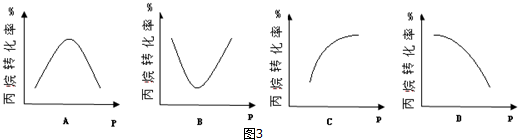
(4)在相同条件下模拟方法 I与方法 II,测得丙烷的平衡转化率与温度的关系如图2所示,图2中方法 II对应的曲线是___(填“M”或“N”),从化学平衡的角度解释丙烷平衡转化率M高于N的原因___.
(5)恒温,密闭容器中投入丙烷发生反应①,某压强下反应t时刻后测得丙烷的转化率,然后保持其它初始实验条件不变,分别在不同压强下,重复上述实验,经过相同时间测得丙烷的转化率随压强变化趋势图可能图3中的是___.
方法 I:丙烷脱氢制丙烯:
①C3H8(g)
| 催化剂 |
| |
| △ |
方法 II:丙烷氧化脱氢制丙烯:(投料为C3H8和CO2)
②C3H8(g)+CO2(g)
| 催化剂 |
| |
| △ |
③CO2(g)+H2(g)
| 催化剂 |
| |
| △ |
已知:
| 化学键 | C-H | C-C | C═C | H-H |
| 键能/kJ•mol-1 | 412 | 348 | 612 | 436 |
(2)模拟方法 I制丙烯,在体积可变的反应器中,恒温,维持体系总压强恒定为0.1MPa,加入1mol C3H8(g)时体积为50L,再加入8.5mol水蒸汽作为稀释剂,反应t分钟达到平衡,测得丙烷0.5mol,已知:分压=物质的量分数×总压强.
①计算该温度下反应I的平衡常数K=___.
②常压下,温度为600K~1000K,水烃比M=10(水烃比是指投料中水蒸汽和丙烷的物质的量之比)时丙烷脱氢平衡转化率与温度变化的曲线如图1,在图1中画出水烃比M=8时的曲线.
(3)模拟方法 II制丙烯,在恒温恒容条件下充入物质的量之比为1:1的丙烷和二氧化碳气体,一段时间后达到平衡,则下列可以判断容器内反应体系达到平衡的是___.
A.v正(C3H8)=v逆(C3H6) B.平均相对分子质量不再变化
C.气体密度不再变化 D.丙烷和二氧化碳的物质的量比值不再变化
(4)在相同条件下模拟方法 I与方法 II,测得丙烷的平衡转化率与温度的关系如图2所示,图2中方法 II对应的曲线是___(填“M”或“N”),从化学平衡的角度解释丙烷平衡转化率M高于N的原因___.

(5)恒温,密闭容器中投入丙烷发生反应①,某压强下反应t时刻后测得丙烷的转化率,然后保持其它初始实验条件不变,分别在不同压强下,重复上述实验,经过相同时间测得丙烷的转化率随压强变化趋势图可能图3中的是___.

▼优质解答
答案和解析
(1)焓变等于反应物总键能-生成物总键能=8×412kJ/mol+2×348kJ/mol-6×312kJ/mol-348kJ/mol-612kJ/mol-436kJ/mol=124kJ/mol,
故答案为:+124;
(2)①恒温恒压条件下,体积与物质的量成正比,加入1mol C3H8(g)时体积为50L,达到平衡状态时丙烷0.5mol,则参加反应的n(C3H8)=n(C3H6)=n(H2)=1mol-0.5mol=0.5mol,平衡时混合气体总物质的量=(0.5mol+0.5mol+0.5mol+8.5mol)=10mol,平衡状态时容器体积=
×50L=500L,则平衡时c(C3H8)=c(C3H6)=c(H2)=
=0.001mol/L,
化学平衡常数Kc=
=
=0.001;
平衡时P(C3H8)=P(C3H6)=P(H2)=
×0.1MPa=0.005MPa,
化学平衡常数Kp=
=
=0.005MPa,
故答案为:KP=0.005MPa或KC=0.001;
②根据图知,升高温度丙烷脱氢率增大,说明该反应是吸热反应,水烃比减小,丙烷的脱氢率减小,升高温度平衡正向移动,丙烷脱氢率增大,所以其图象为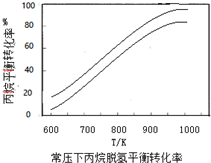 ,
,
故答案为: ;
;
(3)A.v正(C3H8)=v逆(C3H6)=v逆(C3H8),正逆反应速率相等,反应达到平衡状态,故正确; B.反应前后气体总物质的量增大、总质量不变,则反应前后平均相对分子质量减小,当混合气体平均相对分子质量不变时,正逆反应速率相等,反应达到平衡状态,故正确;
C.反应前后总质量、容器体积都不变,则气体密度始终不变,不能据此判断平衡状态,故错误;
D.丙烷和二氧化碳的物质的量比值始终不变,不能据此判断平衡状态,故错误;
故选AB;
(4)方法 II 可看成是发生反应①和反应③,由于反应③会消耗氢气,使得反应①的化学平衡向右移动,所以丙烷去除率增大,则M是方法 II对应的曲线,
故答案为:M;方法 II 可看成是发生反应①和反应③,由于反应③会消耗氢气,使得反应①的化学平衡向右移动;
(5)该反应前后气体物质的量增大,在没有达到平衡之前,平衡正向移动,反应物转化率增大,达到平衡状态后增大压强平衡逆向移动,丙烷的转化率降低,所以符合的图形有ACD,
故答案为:ACD.
故答案为:+124;
(2)①恒温恒压条件下,体积与物质的量成正比,加入1mol C3H8(g)时体积为50L,达到平衡状态时丙烷0.5mol,则参加反应的n(C3H8)=n(C3H6)=n(H2)=1mol-0.5mol=0.5mol,平衡时混合气体总物质的量=(0.5mol+0.5mol+0.5mol+8.5mol)=10mol,平衡状态时容器体积=
| 10mol |
| 1mol |
| 0.5mol |
| 500L |
化学平衡常数Kc=
| c(C3H6).c(H2) |
| c(C3H8) |
| 0.001×0.001 |
| 0.001 |
平衡时P(C3H8)=P(C3H6)=P(H2)=
| 0.5mol |
| 10mol |
化学平衡常数Kp=
| P(C3H6).P(H2) |
| P(C3H8) |
| 0.005MPa×0.005MPa |
| 0.005MPa |
故答案为:KP=0.005MPa或KC=0.001;
②根据图知,升高温度丙烷脱氢率增大,说明该反应是吸热反应,水烃比减小,丙烷的脱氢率减小,升高温度平衡正向移动,丙烷脱氢率增大,所以其图象为
 ,
,故答案为:
 ;
;(3)A.v正(C3H8)=v逆(C3H6)=v逆(C3H8),正逆反应速率相等,反应达到平衡状态,故正确; B.反应前后气体总物质的量增大、总质量不变,则反应前后平均相对分子质量减小,当混合气体平均相对分子质量不变时,正逆反应速率相等,反应达到平衡状态,故正确;
C.反应前后总质量、容器体积都不变,则气体密度始终不变,不能据此判断平衡状态,故错误;
D.丙烷和二氧化碳的物质的量比值始终不变,不能据此判断平衡状态,故错误;
故选AB;
(4)方法 II 可看成是发生反应①和反应③,由于反应③会消耗氢气,使得反应①的化学平衡向右移动,所以丙烷去除率增大,则M是方法 II对应的曲线,
故答案为:M;方法 II 可看成是发生反应①和反应③,由于反应③会消耗氢气,使得反应①的化学平衡向右移动;
(5)该反应前后气体物质的量增大,在没有达到平衡之前,平衡正向移动,反应物转化率增大,达到平衡状态后增大压强平衡逆向移动,丙烷的转化率降低,所以符合的图形有ACD,
故答案为:ACD.
看了丙烷制备丙烯已成为制备丙烯的重...的网友还看了以下:
重铬酸跟和过氧化氢反应的方程式里过氧化氢配的3这说明两个氧都参与反应,但是过氧化氢不是应该只有一个 2020-05-15 …
本装置设置循环氢脱硫设施,目的是降低循环氢中的H2S浓度,提高脱硫反应深度,一般要求脱硫后循环氢 2020-05-31 …
汽油加氢装置首先将汽油切割为轻汽油和重汽油,重汽油加氢脱硫,与轻汽油混合进行脱( )处理,以达 2020-05-31 …
设置循环氢脱硫设施,降低循环氢中的( ) 浓度,提高脱硫反应深度。 2020-05-31 …
循环氢中硫化氢会抑制加氢脱硫反应,同时硫化氢还会与汽油中的烯烃反应生成( ),应保证循环氢中硫 2020-05-31 …
(16分)化工工业中常用乙苯脱氢的方法制备苯乙烯。已知某温度下:反应①:CO2(g)+H2(g)C 2020-07-18 …
(2ss4•泉港区质检)炼油厂酸性气体必须sss%回收制硫,制硫尾气应达到国家和地方3排放标准.有毒 2020-11-02 …
(12分)苯乙烯是重要的基础有机化工原料。工业中以乙苯(C6H5-CH2CH3)为原料,采用催化脱氢 2020-11-20 …
脱式计算(1+二分之一)(1+三分之一)(1+四分之一)…(1+2001分之一)2减2的2次方减2的 2020-12-17 …
1、一种脱粒机10分之9小时脱粒3分之5吨,1小时脱粒多少吨?脱粒1吨要多少小时?2、一辆汽车行驶3 2021-02-01 …