早教吧作业答案频道 -->化学-->
现有A、B、C、D、E、F六种短周期主族元素,原子序数依次增大.已知A的气态氢化物能与其最高价氧化物的水化物反应,B原子最外层电子数是电子层数的3倍,C+和D3+离子的电子层结构相同,B
题目详情
现有A、B、C、D、E、F六种短周期主族元素,原子序数依次增大.已知A的气态氢化物能与其最高价氧化物的水化物反应,B原子最外层电子数是电子层数的3倍,C+和D3+离子的电子层结构相同,B与E属于同一主族.
请回答下列问题:
(1)E在元素周期表中的位置是___.
(2)上述元素形成的简单离子中,半径最小的是___(填离子符号).
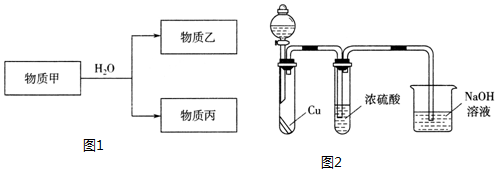
(3)由上述元素中的一种或几种组成的物质甲可以发生如图1反应:
①若乙具有漂白性,则乙的电子式为___.
②若丙的水溶液是强碱性溶液,则甲为___或___(填化学式).
③若乙为二元弱酸,丙既能溶于强酸、又能溶于强碱,则乙的名称为___;用电离方程式表示丙既能溶于强酸、又能溶于强碱的原因___.
④乙遇空气变为红棕色,有同学认为“浓硫酸可以干燥气体甲”,为验证其观点是否正确.用如图2装置进行实验时,分液漏斗中应加入___(填试剂名称).实验过程中,浓硫酸中未发现有气体逸出,且溶液变为红棕色,由此得出的结论是___.
请回答下列问题:

(1)E在元素周期表中的位置是___.
(2)上述元素形成的简单离子中,半径最小的是___(填离子符号).
(3)由上述元素中的一种或几种组成的物质甲可以发生如图1反应:
①若乙具有漂白性,则乙的电子式为___.
②若丙的水溶液是强碱性溶液,则甲为___或___(填化学式).
③若乙为二元弱酸,丙既能溶于强酸、又能溶于强碱,则乙的名称为___;用电离方程式表示丙既能溶于强酸、又能溶于强碱的原因___.
④乙遇空气变为红棕色,有同学认为“浓硫酸可以干燥气体甲”,为验证其观点是否正确.用如图2装置进行实验时,分液漏斗中应加入___(填试剂名称).实验过程中,浓硫酸中未发现有气体逸出,且溶液变为红棕色,由此得出的结论是___.
▼优质解答
答案和解析
A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,A的气态氢化物能与其最高价氧化物的水化物反应,则A是N元素;
B原子最外层电子数是电子层数的3倍,B为O元素;
B与E属于同一主族,则E是S元素,F为短周期主族元素且原子序数大于E,则F为Cl元素;
C+和D3+离子的电子层结构相同,为第三周期元素,C、D分别为Na、Al元素;
(1)E是S元素,S原子核外电子层数等于其周期数、最外层电子数等于其族序数,S原子核外有3个电子层、最外层电子数是6,所以S位于第三周期第VIA族,故答案为:第三周期第VIA族;
(2)上述元素形成的简单离子中,电子层数越少的原子半径越小,电子层结构相同的离子,离子半径随着原子序数增大而减小,这几种元素形成的离子半径大小顺序是S 2->Cl->N3->O 2->Na+>Al 3+,所以离子半径最小的是Al 3+,故答案为:Al 3+;
(3)①若乙具有漂白性,为HClO,则甲是氯气、丙是HCl,HClO分子中O原子和H、Cl原子之间分别共用一对电子,电子式为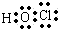 ,故答案为:
,故答案为: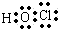 ;
;
②若丙的水溶液是强碱性溶液,则甲为Na或Na2O2,丙为NaOH,乙为氢气或氧气,故答案为:Na;Na2O2;
③若乙为二元弱酸,丙既能溶于强酸、又能溶于强碱,丙为氢氧化铝,乙为硫化氢,则甲是硫化铝,乙名称为硫化氢或氢硫酸,氢氧化铝能发生酸式电离也能发生碱式电离,电离方程式为AlO2-+H2O+H+⇌Al(OH)3⇌Al3++3OH-,所以氢氧化铝能溶于强碱和强酸溶液,故答案为:硫化氢或氢硫酸;AlO2-+H2O+H+⇌Al(OH)3⇌Al3++3OH-;
④乙遇空气变为红棕色,则乙为NO,甲为二氧化氮,有同学认为“浓硫酸可以干燥气体甲”,为验证其观点是否正确.用如图2装置进行实验时,浓硝酸和Cu反应生成二氧化氮,所以分液漏斗中液体是浓硝酸,实验过程中,浓硫酸中未发现有气体逸出,且溶液变为红棕色,则二氧化氮溶于浓硫酸,说明二氧化氮能溶于浓硫酸或浓硫酸不能干燥二氧化氮,
故答案为:浓硝酸;浓硫酸不能干燥二氧化氮或二氧化氮能溶于浓硫酸.
B原子最外层电子数是电子层数的3倍,B为O元素;
B与E属于同一主族,则E是S元素,F为短周期主族元素且原子序数大于E,则F为Cl元素;
C+和D3+离子的电子层结构相同,为第三周期元素,C、D分别为Na、Al元素;
(1)E是S元素,S原子核外电子层数等于其周期数、最外层电子数等于其族序数,S原子核外有3个电子层、最外层电子数是6,所以S位于第三周期第VIA族,故答案为:第三周期第VIA族;
(2)上述元素形成的简单离子中,电子层数越少的原子半径越小,电子层结构相同的离子,离子半径随着原子序数增大而减小,这几种元素形成的离子半径大小顺序是S 2->Cl->N3->O 2->Na+>Al 3+,所以离子半径最小的是Al 3+,故答案为:Al 3+;
(3)①若乙具有漂白性,为HClO,则甲是氯气、丙是HCl,HClO分子中O原子和H、Cl原子之间分别共用一对电子,电子式为
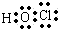 ,故答案为:
,故答案为: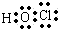 ;
;②若丙的水溶液是强碱性溶液,则甲为Na或Na2O2,丙为NaOH,乙为氢气或氧气,故答案为:Na;Na2O2;
③若乙为二元弱酸,丙既能溶于强酸、又能溶于强碱,丙为氢氧化铝,乙为硫化氢,则甲是硫化铝,乙名称为硫化氢或氢硫酸,氢氧化铝能发生酸式电离也能发生碱式电离,电离方程式为AlO2-+H2O+H+⇌Al(OH)3⇌Al3++3OH-,所以氢氧化铝能溶于强碱和强酸溶液,故答案为:硫化氢或氢硫酸;AlO2-+H2O+H+⇌Al(OH)3⇌Al3++3OH-;
④乙遇空气变为红棕色,则乙为NO,甲为二氧化氮,有同学认为“浓硫酸可以干燥气体甲”,为验证其观点是否正确.用如图2装置进行实验时,浓硝酸和Cu反应生成二氧化氮,所以分液漏斗中液体是浓硝酸,实验过程中,浓硫酸中未发现有气体逸出,且溶液变为红棕色,则二氧化氮溶于浓硫酸,说明二氧化氮能溶于浓硫酸或浓硫酸不能干燥二氧化氮,
故答案为:浓硝酸;浓硫酸不能干燥二氧化氮或二氧化氮能溶于浓硫酸.
看了现有A、B、C、D、E、F六种...的网友还看了以下:
1.诗歌在我国朝十分盛行,除李白之外,还有与他同行时代的著名诗人和.2.诗的每行字数一样,每句末尾 2020-06-05 …
试找出满足下列条件的二叉树:1)先序序列与后序序列相同;2)中序序列与后序序列相同;3)先序序列与 2020-06-18 …
(2014•金山区一模)图一为含有目的基因的DNA(外源DNA),图二为某质粒,表中是几种限制酶识 2020-06-27 …
1、滕王阁序有的《滕王阁序》而有名,岳阳楼因有的《岳阳楼记》更为人知.有关黄鹤楼的诗文有的《黄鹤楼 2020-07-23 …
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1.a-的电子层结构与氦 2020-07-29 …
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1.a-的电子层结构与氦 2020-07-29 …
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的电子层结构与氦 2020-07-29 …
W、X、Y、Z为原子序数依次增大的四种短周期主族元素,它们的最外层电子数之和为22,W与Y同主族, 2020-07-29 …
W、X、Y、Z为原子序数依次增大的四种短周期主族元素,它们的最外层电子数之和为22,W与Y同主族, 2020-07-29 …
(2014•四川模拟)X、Y、Z、W、R.均为前四周期元素且原子序数依次增大,X的基态原子核外有7种 2020-10-31 …