早教吧作业答案频道 -->化学-->
焦亚硫酸钠(Na2S2O5)常用作食品漂白剂.其制备工艺流程如图:已知:反应II包含2NaHSO3═Na2S2O5+H2O等多步反应.(1)反应I的总化学方程式为,反应I进行时应先通入的气体是,反应I产生
题目详情
焦亚硫酸钠(Na2S2O5)常用作食品漂白剂.其制备工艺流程如图:
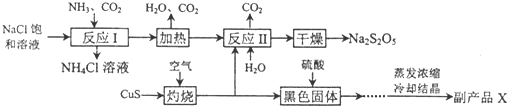
已知:反应II包含2NaHSO3═Na2S2O5+H2O等多步反应.
(1)反应I的总化学方程式为___,反应I进行时应先通入的气体是___,反应I产生的NH4Cl可用作___.
(2)灼烧时发生反应的化学方程式为___,若灼烧时生 成SO21.12×l06 L(标准状况下),则转移电子___mol.
(3)己知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为___;
(4)副产品X的化学式是___,在上述流程中可循环使用的物质是___;
(5)为了减少产品Na2S2O5中杂质含量,需控制反应II中气体与固体的物质的量之比约为___,检验产品中含有碳酸钠杂质所需试剂___(填编号).
①澄清石灰水 ②饱和碳酸氢钠溶液 ③氢氧化钠 ④酸性高锰酸钾 ⑤稀硫酸.

已知:反应II包含2NaHSO3═Na2S2O5+H2O等多步反应.
(1)反应I的总化学方程式为___,反应I进行时应先通入的气体是___,反应I产生的NH4Cl可用作___.
(2)灼烧时发生反应的化学方程式为___,若灼烧时生 成SO21.12×l06 L(标准状况下),则转移电子___mol.
(3)己知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为___;
(4)副产品X的化学式是___,在上述流程中可循环使用的物质是___;
(5)为了减少产品Na2S2O5中杂质含量,需控制反应II中气体与固体的物质的量之比约为___,检验产品中含有碳酸钠杂质所需试剂___(填编号).
①澄清石灰水 ②饱和碳酸氢钠溶液 ③氢氧化钠 ④酸性高锰酸钾 ⑤稀硫酸.
▼优质解答
答案和解析
(1)流程确定反应物为NaCl、NH3、CO2,产物为NH4Cl和碳酸氢钠,反应Ⅰ的化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,反应Ⅰ进行时应先通入氨气,增大HCO3-的浓度,便于NaHCO3析出,氯化铵常用作氮肥,
故答案为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;NH3;氮肥;
(2)硫化铜灼烧一定生成氧化铜和二氧化硫,反应的化学方程式为:2CuS+3O2
2CuO+2SO2,在该反应中每产生2mol二氧化硫则转移12mol电子,所以生成SO21.12×l06 L(标准状况下)即5×l04 mol,则转移电子3×l05 mol
故答案为:2CuS+3O2
2CuO+2SO2;3×l05;
(3)根椐提示可知生成二氧化硫和水,Na2S2O5与稀硫酸反应放出SO2和水,反应的离子方程式为S2O52-+2H+=2SO2↑+H2O,
故答案为:S2O52-+2H+=2SO2↑+H2O;
(4)上述分析可知,氧化铜与硫酸反应生成硫酸铜,蒸发浓缩,冷却结晶,过滤洗涤,得出硫酸铜晶体,副产品X的化学式是CuSO4•5H2O,根据流程图可知,可循环使用的物质是CO2,
故答案为:CuSO4•5H2O;CO2;
(5)从生产过程可以看出是硫酸铜晶体;从图示中可以看出二氧化碳和水可以再次利用,反应Ⅱ中气体与固体分别是二氧化硫和碳酸钠,这两种物质反应必须生成亚硫酸氢钠:反应Ⅱ中反应应是二氧化硫与碳酸钠反应生成NaHSO3,NaHSO3再生成Na2S2O5,反应方程式为Na2CO3+2SO2+H2O=2NaHSO3+CO2,因此气体与固体的物质的量之比为:2:1,检验产品中含有碳酸钠杂质,需加酸反应检验二氧化碳生成,即用的澄清石灰水,但加酸会生成二氧化硫,二氧化硫也能使澄清石灰水变浑浊,故应先除去,用酸性高锰酸钾溶液根据颜色不褪色确定二氧化硫除净,故选①④⑤,
故答案为:2:1;①④⑤.
故答案为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;NH3;氮肥;
(2)硫化铜灼烧一定生成氧化铜和二氧化硫,反应的化学方程式为:2CuS+3O2
| ||
故答案为:2CuS+3O2
| ||
(3)根椐提示可知生成二氧化硫和水,Na2S2O5与稀硫酸反应放出SO2和水,反应的离子方程式为S2O52-+2H+=2SO2↑+H2O,
故答案为:S2O52-+2H+=2SO2↑+H2O;
(4)上述分析可知,氧化铜与硫酸反应生成硫酸铜,蒸发浓缩,冷却结晶,过滤洗涤,得出硫酸铜晶体,副产品X的化学式是CuSO4•5H2O,根据流程图可知,可循环使用的物质是CO2,
故答案为:CuSO4•5H2O;CO2;
(5)从生产过程可以看出是硫酸铜晶体;从图示中可以看出二氧化碳和水可以再次利用,反应Ⅱ中气体与固体分别是二氧化硫和碳酸钠,这两种物质反应必须生成亚硫酸氢钠:反应Ⅱ中反应应是二氧化硫与碳酸钠反应生成NaHSO3,NaHSO3再生成Na2S2O5,反应方程式为Na2CO3+2SO2+H2O=2NaHSO3+CO2,因此气体与固体的物质的量之比为:2:1,检验产品中含有碳酸钠杂质,需加酸反应检验二氧化碳生成,即用的澄清石灰水,但加酸会生成二氧化硫,二氧化硫也能使澄清石灰水变浑浊,故应先除去,用酸性高锰酸钾溶液根据颜色不褪色确定二氧化硫除净,故选①④⑤,
故答案为:2:1;①④⑤.
看了焦亚硫酸钠(Na2S2O5)常...的网友还看了以下:
如图是五种日常生活中常用的化工产品.请回答下列问题:(1)彩漂液(图1)的有效成分为过氧化氢,长期 2020-04-06 …
漂白粉是一种很好的消毒剂和漂白剂.制取漂白粉是用和反应,请写出其化学方程式.漂白粉的有效成分是.漂 2020-05-13 …
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,该晶体具有Na2 2020-05-16 …
根据故障管理流程图2-1,填写(1)到(5)的空白。 2020-05-26 …
如图是三种日常生活中常用的化工产品.请回答下列问题:(1)彩漂液(图1)的有效成分为过氧化氢,长期 2020-06-13 …
试题图书漂流图书漂流宣传标语某校九年级(”班拟开展名为“图书漂流”的读书活动.班主任李老师说:“‘ 2020-06-21 …
英语翻译1指纹识别基本流程图2指纹图像预处理流程图都是论文中图的下标,但不是程序流程图,是框图.翻 2020-06-25 …
工业上制漂粉精的化学方程式是什么?1.漂粉精的有效成分是什么?2.漂粉精在空气中久置失效的原理是( 2020-07-06 …
过碳酸钠(2Na2CO3•3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂.某兴趣小组制备过 2020-07-25 …
(1)工业上如何用石灰石、水和食盐为原料制漂白粉?写出化学方程式。(2)漂白粉暴露在空气中为什么会失 2021-01-12 …