早教吧作业答案频道 -->化学-->
氮、磷、硫、氯、砷等是农药中的重要组成元素.回答下列问题:(1)基态砷的价电子排布式是.(2)下列有关氮、磷、硫、氯的说法不正确的是.a.第一电离能由小到大的顺序是S&l
题目详情
氮、磷、硫、氯、砷等是农药中的重要组成元素.回答下列问题:
(1)基态砷的价电子排布式是___.
(2)下列有关氮、磷、硫、氯的说法不正确的是___.
a.第一电离能由小到大的顺序是S<P<Cl
b.NH3、PH3、AsH3三种物质中沸点最低的是AsH3
c.PO43-、SO42-、ClO4-互为等电子体,它们的空间构型均为四面体
d.化合物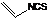 是一种天然植物杀虫剂,其中N原子的杂化方式为sp3
是一种天然植物杀虫剂,其中N原子的杂化方式为sp3
(3)对CoCl3•5NH3的研究表明:①CoCl3•5NH3和硝酸银溶液作用时,其中两个氯离子迅速沉淀,第三个氯离子沉淀缓慢;②溶液导电性测量表明,含1mol CoCl3•5NH3的溶液中含有3mol离子,则配合物中配离子的化学式是___.
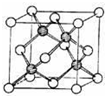
(4)磷化硼是一种受到高度关注的耐磨涂料,其晶胞结构如图,则磷化硼中磷原子周围距离最近的磷原子的数目是___,晶体结构中存在的化学键有___(填序号)
a.离子键b.共价键c.分子间作用力d.配位键
(5)肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g)△H=-1038.7kJ•mol-1若该反应中有4mol N-H键断裂,则形成的π键有___mol.

(1)基态砷的价电子排布式是___.
(2)下列有关氮、磷、硫、氯的说法不正确的是___.
a.第一电离能由小到大的顺序是S<P<Cl
b.NH3、PH3、AsH3三种物质中沸点最低的是AsH3
c.PO43-、SO42-、ClO4-互为等电子体,它们的空间构型均为四面体
d.化合物
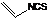 是一种天然植物杀虫剂,其中N原子的杂化方式为sp3
是一种天然植物杀虫剂,其中N原子的杂化方式为sp3(3)对CoCl3•5NH3的研究表明:①CoCl3•5NH3和硝酸银溶液作用时,其中两个氯离子迅速沉淀,第三个氯离子沉淀缓慢;②溶液导电性测量表明,含1mol CoCl3•5NH3的溶液中含有3mol离子,则配合物中配离子的化学式是___.
(4)磷化硼是一种受到高度关注的耐磨涂料,其晶胞结构如图,则磷化硼中磷原子周围距离最近的磷原子的数目是___,晶体结构中存在的化学键有___(填序号)
a.离子键b.共价键c.分子间作用力d.配位键
(5)肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g)△H=-1038.7kJ•mol-1若该反应中有4mol N-H键断裂,则形成的π键有___mol.
▼优质解答
答案和解析
(1)砷位于元素周期表的第四周期第VA族,外围电子排布为4s24p3,
故答案为:4s24p3;
(2)a、根据元素周期律,S、P、Cl三种元素位于同一周期,但P最外层处于半充满状态,故按S、P、Cl的顺序第一电离能依次增大,故a正确;
b、NH3分子间可以形成氢键,增大了熔沸点,AsH3的范德华力大于PH3,因此熔沸点从高到低的顺序为NH3、AsH3、PH3,故b错误;
c、PO43-、SO42-、ClO4-原子数相同,电子总数也相同,互为等电子体,中心原子的价层电子对数都是4,都不含孤电子对数,空间构性都是四面体形,
故c正确;
d、化合物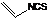 中N形成了N=C、和N-C,N原子的杂化方式为sp2,故d错误;
中N形成了N=C、和N-C,N原子的杂化方式为sp2,故d错误;
故答案为:bd;
(3)CoCl3•5NH3和硝酸银溶液作用时,其中两个氯离子迅速沉淀,第三个氯离子沉淀缓慢,说明有1个Cl做配体,含1mol CoCl3•5NH3的溶液中含有3mol离子,说明阴离子为2个氯离子,NH3作配体,配离子带两个正电荷,所以配离子的化学式为[CoCl(NH3)5]2+,
故答案为:[CoCl(NH3)5]2+;
(4)根据磷化硼的结构简式可知,以顶点上磷原子为例,与该磷原子原子周围距离最近的磷原子位于经过这个点的面的面心上原子,共有12个,B原子最外层有三个电子,而磷原子最外层有五个电子,所以形成磷化硼晶体时有配位键和共价键,故选bd,
故答案为:12;bd;
(5)1mol氮气分子中含有2molπ键,若该反应中有4mol-H键断裂,即有1mol肼参加反应,生成1.5mol氮气,所以形成的π键有1.5mol×2=3mol,
故答案为:3.
故答案为:4s24p3;
(2)a、根据元素周期律,S、P、Cl三种元素位于同一周期,但P最外层处于半充满状态,故按S、P、Cl的顺序第一电离能依次增大,故a正确;
b、NH3分子间可以形成氢键,增大了熔沸点,AsH3的范德华力大于PH3,因此熔沸点从高到低的顺序为NH3、AsH3、PH3,故b错误;
c、PO43-、SO42-、ClO4-原子数相同,电子总数也相同,互为等电子体,中心原子的价层电子对数都是4,都不含孤电子对数,空间构性都是四面体形,
故c正确;
d、化合物
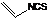 中N形成了N=C、和N-C,N原子的杂化方式为sp2,故d错误;
中N形成了N=C、和N-C,N原子的杂化方式为sp2,故d错误;故答案为:bd;
(3)CoCl3•5NH3和硝酸银溶液作用时,其中两个氯离子迅速沉淀,第三个氯离子沉淀缓慢,说明有1个Cl做配体,含1mol CoCl3•5NH3的溶液中含有3mol离子,说明阴离子为2个氯离子,NH3作配体,配离子带两个正电荷,所以配离子的化学式为[CoCl(NH3)5]2+,
故答案为:[CoCl(NH3)5]2+;
(4)根据磷化硼的结构简式可知,以顶点上磷原子为例,与该磷原子原子周围距离最近的磷原子位于经过这个点的面的面心上原子,共有12个,B原子最外层有三个电子,而磷原子最外层有五个电子,所以形成磷化硼晶体时有配位键和共价键,故选bd,
故答案为:12;bd;
(5)1mol氮气分子中含有2molπ键,若该反应中有4mol-H键断裂,即有1mol肼参加反应,生成1.5mol氮气,所以形成的π键有1.5mol×2=3mol,
故答案为:3.
看了氮、磷、硫、氯、砷等是农药中的...的网友还看了以下:
如q所示装置(燃烧匙中盛放的是红磷)可用于测定空气中氧气的含量,点燃燃烧匙内过量的红磷,立即伸入瓶 2020-05-02 …
实验是化学学科进行科学探究的重要途径.多种因素会影响化学反应的进行;(1)磷与足量的氧气反应生成五 2020-06-14 …
六年级数学题..急..帮帮忙..(要列式,不要列方程)一块西线柿的地,今年获得丰收.第一天收下全部 2020-06-18 …
次磷酸钠(NaH2PO2)是唯一的次磷酸的钠盐(不存在酸式盐).下列叙述中正确的是()A.次磷酸( 2020-07-02 …
二磷酸腺苷(ADP)连接上一个磷酸基团就是三磷酸腺苷(ATP),这个过程也叫“磷酸化”.下列不能发 2020-07-22 …
关于磷的下列叙述中,正确的是()A.红磷没有毒性而白磷剧毒B.白磷在空气中加热到260℃可转变为红 2020-07-29 …
如图所示,测定空气中的氧气含量,闭合电源开关后利用电阻丝放热引燃白磷.下列有关说法正确的是()A.实 2020-11-04 …
磷酸肌酸主要储存于动物和人的肌细胞中,是一种高能磷酸化合物.ATP和磷酸肌酸在一定条件下可相互转化. 2020-12-01 …
通常情况下,燃烧需要三个条件,如图所示.查阅资料(1)白磷和红磷燃烧,都能生成白色的五氧化二磷.(2 2020-12-03 …
(2itt•红河州)如七是小明同学用于测定空气中氧气含量七装置.下列说法错误七是()A.实验前一定要 2020-12-08 …