早教吧作业答案频道 -->化学-->
中国自古有“信口雌黄”、“雄黄入药”之说.雌黄As2S3和雄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药.(1).砷元素有+2、+3两种常见价态.
题目详情
中国自古有“信口雌黄”、“雄黄入药”之说.雌黄As2S3和雄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药.
(1).砷元素有+2、+3两种常见价态.一定条件下,雌黄和雄黄的转化关系如图1所示.
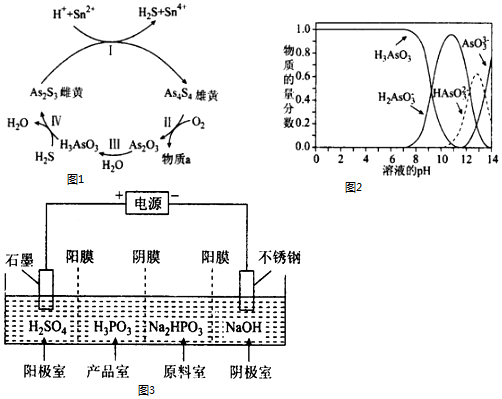
①Ⅰ中,氧化剂是___.
②Ⅱ中,若1mol As4S4反应,转移28mol e-,写出Ⅱ的化学方程式:___.
(2)Ⅲ中产物亚砷酸H3AsO3可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分
数与溶液的pH 关系如图2所示.
①人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是___.
②下列说法不正确的是___(填字母序号).
a.n(H3AsO3):n(H2AsO3-)=1:1时,溶液显碱性
b.pH=12时,溶液中:c(H2AsO3-)+2c(HAsO32-)+3c(AsO3-)+c(OH-)=c(OH+)
c.在K3AsO3溶液中,c((AsO3-)>c(HAsO32-)>c(H2AsO3-)
③将KOH溶液滴人亚砷酸溶液,当pH调至11时发生反应的离子方程式是___.
(3)P和As屈于同主族元素,存在亚磷酸(H3PO3),该酸与足量的NaOH溶液反应生成 Na2HPO3.
①Na2HPO3为___(填“正盐”或“酸式盐”),推测Na2HPO3溶液PH___7(填“>”“<”或“=”).
②工业电解Na2HPO3溶液可得到亚磷酸,装置示意图如图3:
阴极的电极反应式为,产品室中反应的离子方程式为___.
(1).砷元素有+2、+3两种常见价态.一定条件下,雌黄和雄黄的转化关系如图1所示.

①Ⅰ中,氧化剂是___.
②Ⅱ中,若1mol As4S4反应,转移28mol e-,写出Ⅱ的化学方程式:___.
(2)Ⅲ中产物亚砷酸H3AsO3可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分
数与溶液的pH 关系如图2所示.
①人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是___.
②下列说法不正确的是___(填字母序号).
a.n(H3AsO3):n(H2AsO3-)=1:1时,溶液显碱性
b.pH=12时,溶液中:c(H2AsO3-)+2c(HAsO32-)+3c(AsO3-)+c(OH-)=c(OH+)
c.在K3AsO3溶液中,c((AsO3-)>c(HAsO32-)>c(H2AsO3-)
③将KOH溶液滴人亚砷酸溶液,当pH调至11时发生反应的离子方程式是___.
(3)P和As屈于同主族元素,存在亚磷酸(H3PO3),该酸与足量的NaOH溶液反应生成 Na2HPO3.
①Na2HPO3为___(填“正盐”或“酸式盐”),推测Na2HPO3溶液PH___7(填“>”“<”或“=”).
②工业电解Na2HPO3溶液可得到亚磷酸,装置示意图如图3:
阴极的电极反应式为,产品室中反应的离子方程式为___.
▼优质解答
答案和解析
(1)①Ⅰ中Sn的化合价升高,As的化合价降低,所以As2S3在反应中得电子作氧化剂;
故答案为:As2S3;
②Ⅱ中,若1molAs4S4反应转移28mole-,则反应消耗7mol氧气,则反应的方程式为:As4S4+7O2
2As2O3+4SO2;
故答案为:As4S4+7O2
2As2O3+4SO2;
(2)①由图象可知,pH在7.35-7.45之间,溶液中含砷元素的主要微粒是H3AsO3;
故答案为:H3AsO3;
②a.n(H3AsO3):n(H2AsO3-)=1:1时,溶液的pH=9,所以溶液显碱性,故a正确;
b.pH=12时,溶液显碱性,则c(OH-)>c(H+),所以c(H2AsO3-)+2c(HAsO32-)+3c(AsO33-)+c(OH-)>c(H+),故b错误;
c.在K3AsO3溶液中,存在三步水解,以第一步水解为主,第一步水解生成HAsO32-,第二步水解生成H2AsO3-,则c(AsO33-)>c(HAsO32-)>c(H2AsO3-),故c正确;
故答案为:b;
③将KOH 溶液滴入亚砷酸溶液,当pH 调至11时,亚砷酸与氢氧根离子反应生成H2AsO3-,其反应的离子方程为:H3AsO3+OH-=H2AsO3-+H2O;
故答案为:H3AsO3+OH-=H2AsO3-+H2O;
(3)①亚磷酸(H3PO3),该酸与足量的NaOH溶液反应生成 Na2HPO3,说明盐为正盐,亚磷酸为弱酸,则 Na2HPO3为强碱弱酸盐,溶液显碱性,溶液PH>7,
故答案为:正盐;>;
②阴极上得电子发生还原反应,电极反应式为2H++2e-=H2↑;产品室中HPO32-和氢离子结合生成亚磷酸,反应离子方程式为:HPO32-+2H+=H3PO3,
故答案为:2H++2e-=H2↑;HPO32-+2H+=H3PO3.
故答案为:As2S3;
②Ⅱ中,若1molAs4S4反应转移28mole-,则反应消耗7mol氧气,则反应的方程式为:As4S4+7O2
| ||
故答案为:As4S4+7O2
| ||
(2)①由图象可知,pH在7.35-7.45之间,溶液中含砷元素的主要微粒是H3AsO3;
故答案为:H3AsO3;
②a.n(H3AsO3):n(H2AsO3-)=1:1时,溶液的pH=9,所以溶液显碱性,故a正确;
b.pH=12时,溶液显碱性,则c(OH-)>c(H+),所以c(H2AsO3-)+2c(HAsO32-)+3c(AsO33-)+c(OH-)>c(H+),故b错误;
c.在K3AsO3溶液中,存在三步水解,以第一步水解为主,第一步水解生成HAsO32-,第二步水解生成H2AsO3-,则c(AsO33-)>c(HAsO32-)>c(H2AsO3-),故c正确;
故答案为:b;
③将KOH 溶液滴入亚砷酸溶液,当pH 调至11时,亚砷酸与氢氧根离子反应生成H2AsO3-,其反应的离子方程为:H3AsO3+OH-=H2AsO3-+H2O;
故答案为:H3AsO3+OH-=H2AsO3-+H2O;
(3)①亚磷酸(H3PO3),该酸与足量的NaOH溶液反应生成 Na2HPO3,说明盐为正盐,亚磷酸为弱酸,则 Na2HPO3为强碱弱酸盐,溶液显碱性,溶液PH>7,
故答案为:正盐;>;
②阴极上得电子发生还原反应,电极反应式为2H++2e-=H2↑;产品室中HPO32-和氢离子结合生成亚磷酸,反应离子方程式为:HPO32-+2H+=H3PO3,
故答案为:2H++2e-=H2↑;HPO32-+2H+=H3PO3.
看了中国自古有“信口雌黄”、“雄黄...的网友还看了以下:
绘声绘色与有声有色的区别,要用自己的话说,不用复制网上的,浙江卫视的编导很有水平,几个综艺类节目都 2020-05-21 …
调查草原老鼠数量变化对畜牧业有一定的指导意义.假如某时期有一批田鼠迁入内蒙古草原,该田鼠以优质牧草 2020-06-11 …
赵蕊同学有绘画的特长,经常把自己的画作拿到全国去比赛,并多次获奖。有一天,她看到自己的作品刊登在一 2020-06-12 …
求作文关于挫折,绘画的就是关于学习绘画期间遇到挫折然后写怎样战胜的.不要写名人名事写叙事文有点真情 2020-06-29 …
对中国古代绘画发展历程的表述不正确的是A.绘画艺术的源头可追溯到新石器时代B.魏晋时期顾恺之的绘画 2020-07-05 …
下列关于我国隋唐时期石窟艺术的表述,正确的是①石窟艺术在隋唐时期有了很大发展②甘肃敦煌莫高窟中大部 2020-07-05 …
育才小学绘画组和手工编织组共有64人,绘画组和手工编织组人数的比是3:1,绘画组有多少人,手工编织组 2020-11-15 …
英语翻译他是一个在绘画和设计上很有才能的人,他能很轻松的将自己的想法做成实际的作品,他的设计理念非常 2020-11-22 …
洋葱是中学生物学实验常用材料之一,如图为用洋葱进行实验的部分步骤及某同学在实验中绘制的有丝分裂各时期 2020-12-04 …
测绘队小组需要24人参加测量.20人参加计算.16人参加绘图.测绘队的成员中有8人既参加测量又参加计 2020-12-12 …