早教吧作业答案频道 -->化学-->
砷化镓属于第三代半导体,其晶胞结构如如图所示.请回答下列问题:(1)下列说法中正确的是.A.电负性:As<GaB.第一电离能:As<GaC.砷和镓都属于p区元素D.
题目详情
砷化镓属于第三代半导体,其晶胞结构如如图所示.请回答下列问题:
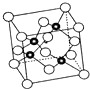
(1)下列说法中正确的是___.
A.电负性:As<Ga B.第一电离能:As<Ga
C.砷和镓都属于p区元素 D.砷和镓在不同周期
(2)砷化镓(GaAs)是将(CH3)3Ga和AsH3用MOCVD方法在700℃进行制备得到,其中(CH3)3Ga中镓原子的杂化方式为___.
(3)Ga的基态原子核外电子排布式为___.
(4)AsH3的沸点比NH3___,其原因是___.

(1)下列说法中正确的是___.
A.电负性:As<Ga B.第一电离能:As<Ga
C.砷和镓都属于p区元素 D.砷和镓在不同周期
(2)砷化镓(GaAs)是将(CH3)3Ga和AsH3用MOCVD方法在700℃进行制备得到,其中(CH3)3Ga中镓原子的杂化方式为___.
(3)Ga的基态原子核外电子排布式为___.
(4)AsH3的沸点比NH3___,其原因是___.
▼优质解答
答案和解析
A.同周期元素从左到右电负性逐渐增大,则电负性:As>Ga,故A错误;
B.同周期元素从左到右第一电离呈增大趋势,但第VA族大于第IIIA族,第IIA族大于第IIIA族,所以则第一电离能:As>Ga,故B错误;
C.砷和镓的价层电子都为sp电子,位于周期表p区,故C正确;
D.砷和镓在相同的周期,均在第四周期,故D错误,故选C;
(2)AsH3中含有3个δ键和1个孤电子对,为三角锥形,(CH3)3Ga中Ga形成3个δ键,没有孤电子对,为sp2杂化,故答案为:sp2;
(3)Ga的原子序数为31,核外电子排布式为1s22s22p63s23p63d104s24p1,故答案为:1s22s22p63s23p63d104s24p1;
(5)N原子半径较小,电负性较大,对应的NH3分子间能形成氢键,沸点较高,而As电负性小,半径大,分子间不能形成氢键,沸点较低,
故答案为:NH3分子间能形成氢键,而As电负性小,半径大,分子间不能形成氢键.
B.同周期元素从左到右第一电离呈增大趋势,但第VA族大于第IIIA族,第IIA族大于第IIIA族,所以则第一电离能:As>Ga,故B错误;
C.砷和镓的价层电子都为sp电子,位于周期表p区,故C正确;
D.砷和镓在相同的周期,均在第四周期,故D错误,故选C;
(2)AsH3中含有3个δ键和1个孤电子对,为三角锥形,(CH3)3Ga中Ga形成3个δ键,没有孤电子对,为sp2杂化,故答案为:sp2;
(3)Ga的原子序数为31,核外电子排布式为1s22s22p63s23p63d104s24p1,故答案为:1s22s22p63s23p63d104s24p1;
(5)N原子半径较小,电负性较大,对应的NH3分子间能形成氢键,沸点较高,而As电负性小,半径大,分子间不能形成氢键,沸点较低,
故答案为:NH3分子间能形成氢键,而As电负性小,半径大,分子间不能形成氢键.
看了砷化镓属于第三代半导体,其晶胞...的网友还看了以下:
下列是嫁接步骤示意图,请回答下列问题,在空格上填数字.(1)上面图示中属于枝接的接穗是,砧木是.( 2020-06-13 …
(2014•槐荫区一模)“垃圾是放错了地方的资源”.如图所示是利用金属探测仪寻找城市垃圾堆中金属的 2020-06-22 …
如图所示是高频焊接原理示意图.线圈中通以高频变化的电流时,待焊接的金属工件中就产生感应电流,感应电 2020-06-29 …
如图所示卫厨房中常见的电饭锅的结构图,回答下列问题:(1)图中所示的标示中,属于金属材料的是(填一 2020-07-14 …
已知函数f(x)=sin(wx+φ)+根号3cos(wx+φ)的部分图像如图所示、,其中w大于0, 2020-07-21 …
.试计算该草药样品中砷含量我国对中药中重金属元素和有毒元素的含量等各项指标检查是非常严格的.下面是分 2020-11-01 …
为了防止中考作弊,监考人员利用手执式金属探测仪对考生进行检查.如图所示,当扫过金属物体时,在金属导体 2020-11-06 …
英语翻译同义句转换Sheshowedthephototome.翻译我的鞋和鲍勃的鞋一样贵.(as.a 2020-11-23 …
我国对中药中重金属元素和有毒元素的含量等各项指标检查是非常严格的.下面是分析实验室对中草药中可能的残 2020-12-22 …
问:As2O3如何变得H3AsO4我知道SiO2制H2SiO3是先如下一个流程SiO2-Na2Sio 2020-12-22 …