早教吧作业答案频道 -->化学-->
CoCl2•6H2O是一种饲料营养强化剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种新工艺流程如图:已知:①钴与盐酸反应的化学方程式为:Co+2HCl═CoCl2+H2↑②CoCl2•6H2O熔点86℃,易
题目详情
CoCl2•6H2O是一种饲料营养强化剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种新工艺流程如图:
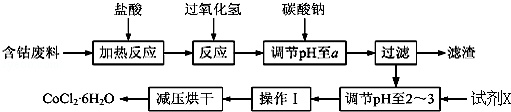
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl═CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为___(写一点).
(2)加入碳酸钠调节pH至a,a的范围是___;pH调至a后过滤,再用试剂X将滤液的pH调节至2-3,则所用的试剂X为___.
(3)操作Ⅰ包含3个基本实验操作,它们是___、___和过滤.
(4)制得的CoCl2•6H2O需减压烘干的原因是___.
(5)为测定产品中CoCl2•6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量.通过计算发现产品中CoCl2•6H2O的质量分数大于100%,其原因可能是___.
(6)在实验室中,为了从上述产品中获得纯净的CoCl2•6H2O,常将制得的产品溶解于乙醚中,然后___、___(填实验操作)获得纯净的CoCl2•6H2O.

已知:
①钴与盐酸反应的化学方程式为:Co+2HCl═CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为___(写一点).
(2)加入碳酸钠调节pH至a,a的范围是___;pH调至a后过滤,再用试剂X将滤液的pH调节至2-3,则所用的试剂X为___.
(3)操作Ⅰ包含3个基本实验操作,它们是___、___和过滤.
(4)制得的CoCl2•6H2O需减压烘干的原因是___.
(5)为测定产品中CoCl2•6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量.通过计算发现产品中CoCl2•6H2O的质量分数大于100%,其原因可能是___.
(6)在实验室中,为了从上述产品中获得纯净的CoCl2•6H2O,常将制得的产品溶解于乙醚中,然后___、___(填实验操作)获得纯净的CoCl2•6H2O.
▼优质解答
答案和解析
(1)金属和盐酸反应生成氯化物,和硝酸反应生成硝酸盐,同时生成一氧化氮,导致氯化物中含有硝酸盐杂质,且生成有毒气体,污染环境,故答案为:减少有毒气体的排放,防止大气污染;防止产品中混有硝酸盐;
(2)废料加入盐酸后生成氯化物,然后加入双氧水,二价铁离子被双氧水氧化生成三价铁离子,根据沉淀的PH值表格知,当溶液的PH值为5.2时,铁离子和铝离子被完全沉淀,当溶液的PH值为7.6时,钴离子才开始产生沉淀,所以要想将铁离子、铝离子和钴离子分离,溶液的pH值应该不小于5.2不大于7.6,pH调至a后过滤,再用试剂X将滤液的pH调节至2~3,所用的试剂X为盐酸;
故答案为:5.2---7.6;盐酸;
(3)从溶液中制取固体的方法制取氯化钴固体,其操作步骤是蒸发浓缩、冷却结晶和过滤,故答案为:蒸发浓缩、冷却结晶;
(4)根据题意知,CoCl2•6H2O常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴,为防止其分解,制得的CoCl2•6H2O需减压烘干,
故答案为:降低烘干温度,防止产品分解;
(5)根据CoCl2•6H2O的组成分析,造成产品中CoCl2•6H2O的质量分数大于100%的原因可能是:1、含有杂质,导致氯离子含量大,2、结晶水化物失去部分水,导致相同质量的固体中氯离子含量变大,故答案为:样品中含有NaCl杂质或CoCl2•6H2O烘干时失去了部分结晶水;
(6)根据CoCl2•6H2O的性质选取方法,CoCl2•6H2O熔点86℃,易溶于乙醚,所以将产品溶于乙醚,过滤后再蒸馏,从而获得较纯净的CoCl2•6H2O,故答案为:过滤;蒸馏.
(2)废料加入盐酸后生成氯化物,然后加入双氧水,二价铁离子被双氧水氧化生成三价铁离子,根据沉淀的PH值表格知,当溶液的PH值为5.2时,铁离子和铝离子被完全沉淀,当溶液的PH值为7.6时,钴离子才开始产生沉淀,所以要想将铁离子、铝离子和钴离子分离,溶液的pH值应该不小于5.2不大于7.6,pH调至a后过滤,再用试剂X将滤液的pH调节至2~3,所用的试剂X为盐酸;
故答案为:5.2---7.6;盐酸;
(3)从溶液中制取固体的方法制取氯化钴固体,其操作步骤是蒸发浓缩、冷却结晶和过滤,故答案为:蒸发浓缩、冷却结晶;
(4)根据题意知,CoCl2•6H2O常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴,为防止其分解,制得的CoCl2•6H2O需减压烘干,
故答案为:降低烘干温度,防止产品分解;
(5)根据CoCl2•6H2O的组成分析,造成产品中CoCl2•6H2O的质量分数大于100%的原因可能是:1、含有杂质,导致氯离子含量大,2、结晶水化物失去部分水,导致相同质量的固体中氯离子含量变大,故答案为:样品中含有NaCl杂质或CoCl2•6H2O烘干时失去了部分结晶水;
(6)根据CoCl2•6H2O的性质选取方法,CoCl2•6H2O熔点86℃,易溶于乙醚,所以将产品溶于乙醚,过滤后再蒸馏,从而获得较纯净的CoCl2•6H2O,故答案为:过滤;蒸馏.
看了CoCl2•6H2O是一种饲料...的网友还看了以下:
空气清新剂是在20世纪开始应用于环境卫生领域的一种化工产品.空气不流通的房间里,在一个角落喷射空气 2020-05-17 …
膜剂只适合于( )。 A.剂量大的药物B.单剂量在3克以上的药物C.单剂量在lO克以上的药 2020-05-25 …
为了消除卫生间里难闻的臭味,我们可以在卫生间里放置一些固体空气清新剂,这些固体空气清新剂发生(填物 2020-06-25 …
你了解空气清新剂吗?近日,河南长垣县一家KTV发生火灾,起火原因竟是电热器烘烤空气清新剂致其爆燃。此 2020-10-30 …
如图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C 2020-10-31 …
如图所示,淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下可以生成B(C6H12O7)或C(C6 2020-10-31 …
只用一种试剂就可以鉴别乙酸,葡萄糖,乙酸乙酯,这种试剂是()ANaOH(aq)BNa2CO3(aq) 2020-11-03 …
塑料翻新剂是什么塑料翻新剂和除黄剂是一样的么,用处是不也都一样呢,今天买了桶卡洁尔塑料除黄剂,老板说 2020-11-03 …
(2012•镇江)现在有一种叫“固体清新剂”的商品,把它放置在厕所、汽车、饭店内,能有效的清新空气、 2020-11-12 …
1、现在超市卖“固体清新剂”,把它放在各种地方可以有效清新空气,预防感冒,使居室温馨芳香,这种现象是 2020-12-12 …