早教吧作业答案频道 -->化学-->
草酸钴用途广泛,可用于指示剂和催化剂的制备.一种利用水钴矿制取草酸钴晶体(CoC2O4⋅2H2O)工艺流程如图1:已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;②
题目详情
草酸钴用途广泛,可用于指示剂和催化剂的制备.一种利用水钴矿制取草酸钴晶体(CoC2O4⋅2H2O)工艺流程如图1:
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3的 离子方程式为___
(2)NaClO3的作用是___; 调PH至5.2,沉淀的主要成分为___
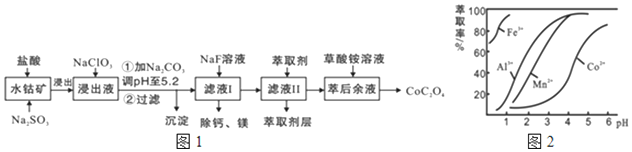
(3)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是___;使用萃取剂适宜的pH是___
A.接近2.0 B.接近3.0 C.接近5.0
(4)除钙、镁是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀,已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+):c(Ca2+)=___.
(5)已知含钴废料中含Co2O3质量分数为a%,若取mkg该含钴废料按照上述流程,理论上最多能制得草酸钴晶体的质量为___g.

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的PH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3的作用是___; 调PH至5.2,沉淀的主要成分为___
(3)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是___;使用萃取剂适宜的pH是___
A.接近2.0 B.接近3.0 C.接近5.0
(4)除钙、镁是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀,已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+):c(Ca2+)=___.
(5)已知含钴废料中含Co2O3质量分数为a%,若取mkg该含钴废料按照上述流程,理论上最多能制得草酸钴晶体的质量为___g.
▼优质解答
答案和解析
(1)亚硫酸钠具有还原性,能还原氧化性离子Co3+,反应为:2Co3++SO32-+H2O=2Co2++SO42-+2H+;
故答案为:2Co3++SO32-+H2O=2Co2++SO42-+2H+;
(2)NaClO3的作用是:将浸出液中Fe2+氧化为Fe3+,加Na2CO3调PH=5.2能使Fe3+、Al3+ 离子转化成氢氧化物沉淀Al(OH)3、Fe(OH)3;
故答案为:将 Fe2+氧化为 Fe3+;Al(OH)3、Fe(OH)3;
(3)根据流程图可知,此时溶液中存在Mn2+、Co2+金属离子;
由萃取剂对金属离子的萃取率与pH的关系可知,调节溶液PH在3.0~3.5之间,可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀;
故答案为:除去Mn2+;B;
(4)由溶度积可知,滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为CaF2、MgF2沉淀,根据溶度积可知c(Mg2+):c(Ca2+)=
=
=0.7;
故答案为:0.7;
(5)mkg含钴废料中含Co2O3质量分数为a%,则钴元素的物质的量为
mol,钴元素质量守恒则,草酸钴晶体(CoC2O4⋅2H2O)的质量为
mol×183g/mol=
g=16.6ma;
故答案为:
或16.6ma.
故答案为:2Co3++SO32-+H2O=2Co2++SO42-+2H+;
(2)NaClO3的作用是:将浸出液中Fe2+氧化为Fe3+,加Na2CO3调PH=5.2能使Fe3+、Al3+ 离子转化成氢氧化物沉淀Al(OH)3、Fe(OH)3;
故答案为:将 Fe2+氧化为 Fe3+;Al(OH)3、Fe(OH)3;
(3)根据流程图可知,此时溶液中存在Mn2+、Co2+金属离子;
由萃取剂对金属离子的萃取率与pH的关系可知,调节溶液PH在3.0~3.5之间,可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀;
故答案为:除去Mn2+;B;
(4)由溶度积可知,滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为CaF2、MgF2沉淀,根据溶度积可知c(Mg2+):c(Ca2+)=
| Ksp(MgF2) |
| Ksp(CaF2) |
| 7.35×10-11 |
| 1.05×10-10 |
故答案为:0.7;
(5)mkg含钴废料中含Co2O3质量分数为a%,则钴元素的物质的量为
| m×a%×10-3×2 |
| 166 |
| m×a%×10-3×2 |
| 166 |
| 1830ma |
| 83 |
故答案为:
| 1830ma |
| 83 |
看了草酸钴用途广泛,可用于指示剂和...的网友还看了以下:
关于抽象艺术急1抽象艺术是用哪些方式进行的制作?2抽象艺术有哪些流派?举例2-3个抽象艺术画家有哪 2020-05-13 …
如图,PB切⊙O于B点,直线PO交⊙O于点E,F,过点B作PO的垂线BA,垂足为点D,交⊙O于点A 2020-05-17 …
1、五年级两个班同学参加植树劳动,共分一批树苗,一班分得的的棵树比总数的30%多100棵,二班分得 2020-06-24 …
古往今来的大艺术家都对草根艺术保持一个尊敬的心态。世界著名指挥家小泽征尔第一次听二胡曲《二泉映月》 2020-07-07 …
如图,AB是⊙O的切线,B为切点,BC是⊙O的弦,直线AC与⊙O交于D,角C=45°,DE⊥AB, 2020-07-11 …
求给以下算法复杂度排序增长速度由慢到快1)O(n^(3/4))O(log(n)^5)O(2^n)O 2020-07-23 …
“艺”是指制茶、烹茶、品茶等艺茶之术,“道”是指艺茶过程中所()的精神,2.茶艺与茶道精神是中国茶文 2020-11-07 …
回答文艺复兴运动的有关问题。(10分)(1)文艺复兴运动开始于哪一国家?文艺复兴的先驱者是谁?(2分 2020-12-07 …
如图,O为△ABC内一点,∠A=80°,∠CBO=1/m∠CBA,∠BCO=1/m∠BCA(1)若m 2020-12-25 …
唐代的草书显示了盛唐的气象,被视为草书艺术的巅峰。此时涌现出的草书大家有①颜真卿②张旭③柳公权④怀素 2020-12-26 …