早教吧作业答案频道 -->化学-->
锌及其化合物用途广泛.火法炼锌以闪锌矿(主要成分是ZnS)为主要原料,涉及的主要反应有:2ZnS(s)+3O2(g)═2ZnO(s)+2SO2(g)△H1=-930kJ•mol-12C(s)+O2(g)═2CO(g)△H2=-221kJ•mol-1ZnO
题目详情
锌及其化合物用途广泛.火法炼锌以闪锌矿(主要成分是ZnS)为主要原料,涉及的主要反应有:
2ZnS(s)+3O2(g)═2ZnO(s)+2SO2(g)△H1=-930kJ•mol-1
2C(s)+O2(g)═2CO(g)△H2=-221kJ•mol-1
ZnO(s)+CO(g)═Zn(g)+CO2(g)△H3=198kJ•mol-1
(1)反应ZnS(s)+C(s)+2O2(g)═Zn(g)+CO2(g)+SO2(g)的△H4=___kJ•mol-1.
反应中生成的CO2与NH3混合,在一定条件下反应合成尿素:
2NH3(g)+CO2(g)
CO(NH2)2(s)+H2O(g)△H
该反应在一定条件下能自发进行的原因是___;若该反应在一恒温、恒容密闭容器内进行,判断反应达到平衡状态的标志是___.
a.CO2与H2O(g)浓度相等 b.容器中气体的压强不再改变
c.2v(NH3)正=v(H2O)逆 d.容器中混合气体的密度不再改变
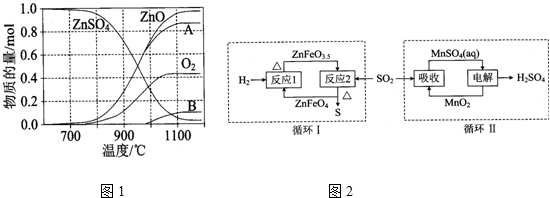
(2)硫酸锌可广泛用作印染媒染剂和木材防腐剂.ZnSO4受热分解过程中各物质物质的量随温度变化关系如图1所示.
①写出700℃~980℃时发生反应的化学方程式:___,物质B的化学式是___.
②硫酸锌分解生成的SO2经下图2中的两个循环可分别得到S和H2SO4.写出循环I中反应2的化学方程式:___;循环II中电解过程阳极反应式是___.
2ZnS(s)+3O2(g)═2ZnO(s)+2SO2(g)△H1=-930kJ•mol-1
2C(s)+O2(g)═2CO(g)△H2=-221kJ•mol-1
ZnO(s)+CO(g)═Zn(g)+CO2(g)△H3=198kJ•mol-1
(1)反应ZnS(s)+C(s)+2O2(g)═Zn(g)+CO2(g)+SO2(g)的△H4=___kJ•mol-1.
反应中生成的CO2与NH3混合,在一定条件下反应合成尿素:
2NH3(g)+CO2(g)
| 一定条件 |
| |
该反应在一定条件下能自发进行的原因是___;若该反应在一恒温、恒容密闭容器内进行,判断反应达到平衡状态的标志是___.
a.CO2与H2O(g)浓度相等 b.容器中气体的压强不再改变
c.2v(NH3)正=v(H2O)逆 d.容器中混合气体的密度不再改变
(2)硫酸锌可广泛用作印染媒染剂和木材防腐剂.ZnSO4受热分解过程中各物质物质的量随温度变化关系如图1所示.
①写出700℃~980℃时发生反应的化学方程式:___,物质B的化学式是___.
②硫酸锌分解生成的SO2经下图2中的两个循环可分别得到S和H2SO4.写出循环I中反应2的化学方程式:___;循环II中电解过程阳极反应式是___.

▼优质解答
答案和解析
(1)①2ZnS(s)+3O2(g)═2ZnO(s)+2SO2(g)△H1=-930kJ•mol-1
②2C(s)+O2(g)═2CO(g)△H2=-221kJ•mol-1
③ZnO(s)+CO(g)═Zn(g)+CO2(g)△H3=198kJ•mol-1
将方程式
+③得ZnS(s)+C(s)+2O2(g)═Zn(g)+CO2(g)+SO2(g),△H4=
+198kJ/mol=-377.5kJ/mol;
当△G=△H-T△S<0时该反应一定能自发进行,该反应前后△S<0,则焓变应该小于0;
a.CO2与H2O(g)浓度相等,正逆反应速率不一定相等,所以不一定达到平衡状态,故错误;
b.该反应前后气体物质的量减少,当容器中气体的压强不再改变时正逆反应速率相等,反应达到平衡状态,故正确;
c.当v(NH3)正=2v(H2O)逆时该反应达到平衡状态,所以当2v(NH3)正=v(H2O)逆时该反应没有达到平衡状态,故错误;
d.反应前后问题密度改变,所以当容器中混合气体的密度不再改变时该反应达到平衡状态,故正确;
故答案为:-377.5;△H<0;bd;
(2)①700℃~980℃时发生反应时,根据图知,生成ZnO、氧气和B,根据元素守恒知,B中含有S元素,因为生成氧气失电子,则S元素应该得电子发生还原反应,所以B应该是SO2,根据反应物和生成物及反应条件书写方程式为2ZnSO4
2ZnO+2SO2↑+O2↑,故答案为:2ZnSO4
2ZnO+2SO2↑+O2↑;SO2;
②ZnFeO3.5和SO2在加热条件下生成ZnFeO4、S,反应方程式为4ZnFeO3.5+SO2
4ZnFeO4+S;
电解硫酸锰时,生成二氧化锰和硫酸,阳极上失电子发生氧化反应,电极反应式为Mn2+-2e-+2H2O=MnO2+4H+,
故答案为:4ZnFeO3.5+SO2
4ZnFeO4+S;Mn2+-2e-+2H2O=MnO2+4H+.
②2C(s)+O2(g)═2CO(g)△H2=-221kJ•mol-1
③ZnO(s)+CO(g)═Zn(g)+CO2(g)△H3=198kJ•mol-1
将方程式
| ①+② |
| 2 |
| (-930-221)kJ/mol |
| 2 |
当△G=△H-T△S<0时该反应一定能自发进行,该反应前后△S<0,则焓变应该小于0;
a.CO2与H2O(g)浓度相等,正逆反应速率不一定相等,所以不一定达到平衡状态,故错误;
b.该反应前后气体物质的量减少,当容器中气体的压强不再改变时正逆反应速率相等,反应达到平衡状态,故正确;
c.当v(NH3)正=2v(H2O)逆时该反应达到平衡状态,所以当2v(NH3)正=v(H2O)逆时该反应没有达到平衡状态,故错误;
d.反应前后问题密度改变,所以当容器中混合气体的密度不再改变时该反应达到平衡状态,故正确;
故答案为:-377.5;△H<0;bd;
(2)①700℃~980℃时发生反应时,根据图知,生成ZnO、氧气和B,根据元素守恒知,B中含有S元素,因为生成氧气失电子,则S元素应该得电子发生还原反应,所以B应该是SO2,根据反应物和生成物及反应条件书写方程式为2ZnSO4
| ||
| ||
②ZnFeO3.5和SO2在加热条件下生成ZnFeO4、S,反应方程式为4ZnFeO3.5+SO2
| ||
电解硫酸锰时,生成二氧化锰和硫酸,阳极上失电子发生氧化反应,电极反应式为Mn2+-2e-+2H2O=MnO2+4H+,
故答案为:4ZnFeO3.5+SO2
| ||
看了锌及其化合物用途广泛.火法炼锌...的网友还看了以下:
(2009•龙岩)归纳总结是学习的重要方法.小明同学在学习“应用广泛的酸、碱、盐”知识后,结合常见 2020-05-13 …
操作风险评估的主要方法中,运用最广泛、方法最成熟的方法是:( ) A.自我评估法B.损失 2020-05-30 …
( )是目前操作风险识别与评估的主要方法中运用最广泛、最成熟的。 A.自我评估法B.损 2020-05-30 …
调查和统计是科学研究的重要方法,被广泛应用于生物科学研究之中.以下是调查和统计方法的某些具体应用, 2020-06-10 …
( )是目前操作风险识别与评估的主要方法中运用最广泛、最成熟的。A.自我评估法B.损失事 2020-06-27 …
集需要一片英语演讲稿关于保护动物要大学的水平,不要抄袭作文,比如百度上的保护环境也可以,但是最好是 2020-08-04 …
关于依法治国和以德治国的联系,正确的是()A.依法治国和以德治国两者没有联系B.道德调节的范围更加广 2020-11-07 …
怎么样考好电工基础,写作文,300字,不要太空泛,具体一点的我才学电工基础半学期,不要说太深奥的,我 2020-11-15 …
在高中阅读训练中经常提到精读和泛读的问题,究竟什么时候应该精读,什么时候应该泛读?对什么样的文章应该 2020-12-04 …
第二次世界大战期间,社会制度不同的国家能结成世界反法西斯同盟的最主要原因是()A.各战场战略配合的需 2020-12-28 …