T1、T2两种温度下BaSO4在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:(1)T1T2(填“>”、“<”或“=”),T2时Ksp(BaSO4)=。(
T 1 、 T 2 两种温度下BaSO 4 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:
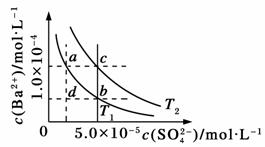
(1) T 1 ________ T 2 (填“>”、“<”或“=”), T 2 时 K sp (BaSO 4 )=____________。
(2)根据 T 1 温度时BaSO 4 的沉淀溶解平衡曲线,判断下列说法正确的是________(填序号)。
A.加入Na 2 SO 4 可由 a 点变为 b 点
B.在 T 1 曲线上方区域(不含曲线)的任意一点时,均有BaSO 4 沉淀生成
C.蒸发溶剂可能由 d 点变为 T 1 曲线上 a 、 b 之间的某一点(不含 a 、 b )
D.升温可由 b 点变为 d 点
(3)沉淀的生成、溶解和转化在无机物制备和提纯及科研等领域有着广泛应用。已知25 ℃时, K sp (BaSO 4 )=1×10 - 10 , K sp (BaCO 3 )=1×10 - 9 。
①医学上进行消化系统的X射线透视时,常使用BaSO 4 作内服造影剂。胃酸很强(pH约为1),但服用大量BaSO 4 仍然是安全的,BaSO 4 不溶于酸的原因是__________________(用沉淀溶解平衡原理解释)。万一误服了少量BaCl 2 ,应尽快用大量0.5 mol/L Na 2 SO 4 溶液洗胃,如果忽略洗胃过程中Na 2 SO 4 溶液浓度的变化,残留在胃液中的Ba 2 + 浓度仅为________mol/L。
②长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率。水垢中含有CaSO 4 ,可先用Na 2 CO 3 溶液处理,使之转化为疏松、易溶于酸的CaCO 3 ,而后用酸除去。CaSO 4 转化为CaCO 3 的离子方程式为__________________。
解析:
(1)T1下的离子积较小,所以T1<T2。T2时的溶度积可利用c点的数据进行计算求得。(2)由于存在溶解平衡,加入Na2SO4,BaSO4的沉淀溶解平衡逆向移动,Ba2+的浓度降低,A选项正确;T1曲线上方区域的离子积大于溶度积,所以会析出沉淀,B选项正确;蒸发溶剂,不饱和溶液中离子的浓度都变大,可能由d点变为T1曲线上a、b之间的某一点,C选项正确;升高温度,c(SO)会变大,D选项错误。(3)①由沉淀溶解平衡BaSO4(s)Ba2+(aq)+SO(aq)可知,H+不能减小Ba2+或SO的浓度,平衡不能向溶解方向移动。由c(SO)=0.5 mol/L和c(Ba2+)·c(SO)=1×10-10可知c(Ba2+)=2×10-10 mol/L。②CaSO4转化为CaCO3的离子方程式为CaSO4(s)+CO(aq)===CaCO3(s)+SO(aq)。 答案:(1)< 5.0×10-9 (2)ABC (3)①对于沉淀溶解平衡BaSO4(s)Ba2+(aq)+SO(aq),H+不能减小Ba2+或SO的浓度,平衡不能向溶解方向移动 2×10-10 ②CaSO4(s)+CO(aq)===CaCO3(s)+SO(aq)
矩形公园ABCD中,原有两条与ADAB平行的小路EF、GH,它们相交于Q,两条小路将公园分成了四个 2020-05-13 …
求圆柱的表面积最好步骤清楚如:侧面积:底面积:表面积:1.C=12.56米h=10米S表面积=平方 2020-06-04 …
求圆柱的表面积最好步骤清楚如:侧面积:底面积:表面积:1.C=12.56米h=10米S表面积=平方 2020-06-04 …
如图所示,S为上下振动的波源,振动频率为100Hz,所产生的横波左右传播,波速为80m/s,已知P 2020-07-26 …
如图所示,在水平地面上O点的正上方有A、B两点,已知OA=AB=h,现分别从A、B两点以20m/s和 2020-11-03 …
求教一道光学题.如图所示,M、N是两块互相垂直放置的平面镜,S是镜前的一个固定的点光源,经过两块平面 2020-11-04 …
甲乙两列火车,在两条平行的平直铁路上分别作匀速直线运动,甲的速度是15m/s,乙的速度是11m/s. 2020-11-20 …
甲乙两列火车,在两条平行的平直铁路上分别作匀速直线运动,甲的速度是15m/s,乙的速度是11m/s. 2020-11-20 …
两列火车A和B在两条平行的铁路轨道上同向平行行驶,A、B两车长分别为L1=100m,L2=120m. 2020-11-20 …
如图S是一频率为10Hz上下振动的波源,所激起的波同时向x轴正、负两方向传播,波速为20m/s,质点 2020-12-15 …