早教吧作业答案频道 -->化学-->
明矾石的主要成分是K2SO4•Al2(SO4)3•2Al2O3•6H2O,此外还含有少量Fe2O3杂质.利用明矾石制备氢氧化铝的流程如下:(1)“焙烧”过程中反应的化学方程式为2Al2(SO4)3+3S
题目详情
明矾石的主要成分是K2SO4•Al2(SO4)3•2Al2O3•6H2O,此外还含有少量Fe2O3杂质.利用明矾石制备氢氧化铝的流程如下:
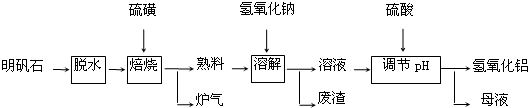
(1)“焙烧”过程中反应的化学方程式为2Al2(SO4)3+3S
2Al2O3+___.该反应的氧化剂是___.
(2)“溶解”时反应的离子方程式为___.
(3)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明已洗涤干净的实验操作和现象是___.
(4)“母液”中可回收的物质是___.

(1)“焙烧”过程中反应的化学方程式为2Al2(SO4)3+3S
| ||
(2)“溶解”时反应的离子方程式为___.
(3)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明已洗涤干净的实验操作和现象是___.
(4)“母液”中可回收的物质是___.
▼优质解答
答案和解析
(1)反应中硫元素化合价由Al2(SO4)3中S元素的+6价降低,单质硫中S的化合价升高,令产物中S的化合价为+x价,根据得失电子守恒可知6(6-x)=3(x-0),则x=4,所以生成产物为SO2,则反应的化学方程式为2Al2(SO4)3+3S
2Al2O3+9SO2,Al2(SO4)3化合价降低得电子为氧化剂,
故答案为:9SO2;Al2(SO4)3;
(2)氢氧化钠与氧化铝反应生成偏铝酸钠和水,反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;
(3)Al(OH)3沉淀具有吸附性,可吸附硫酸根离子,通过检验硫酸根离子的方法进行实验,方法为取最后一次洗涤的流出液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净,
故答案为:取最后一次洗涤的滤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净;
(4)根据流程分析可知“母液”中含有硫酸盐中含有K2SO4、Na2SO4,都可回收利用,
故答案为:K2SO4、Na2SO4.
| ||
故答案为:9SO2;Al2(SO4)3;
(2)氢氧化钠与氧化铝反应生成偏铝酸钠和水,反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;
(3)Al(OH)3沉淀具有吸附性,可吸附硫酸根离子,通过检验硫酸根离子的方法进行实验,方法为取最后一次洗涤的流出液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净,
故答案为:取最后一次洗涤的滤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净;
(4)根据流程分析可知“母液”中含有硫酸盐中含有K2SO4、Na2SO4,都可回收利用,
故答案为:K2SO4、Na2SO4.
看了 明矾石的主要成分是K2SO4...的网友还看了以下:
同物质的质量浓度的KCl、CaCl2、AlCl3,三种溶液的体积比为3:2:1,这三种溶液中Cl- 2020-04-06 …
指数的性质或对数的性质等如果log(x)(2√2)=3/4,则x=()它的分析是x^3/4=2√2 2020-05-13 …
在20℃时,下列四种物质分别溶解在水中,恰好形成饱和溶液在20℃时,下列四种物质分别溶解在水里恰好 2020-05-22 …
某商贸公司有A,B两种商品需运出,A商品每件体积为0.3m^3,质量为0.1吨;B商品每件体积为0 2020-05-23 …
今有质量分数为20%的某溶液一瓶,倒出3/4质量后加水至原质量,再倒出2/3质量后,余下溶液的质量 2020-05-23 …
一杯500克的牛奶中含有3/2500的钙质,这些钙质约占一个成年人一天所需钙质的3/4.一个成年人 2020-06-04 …
几道简单化学题,望能人志士helpme!1.氮气质量14克分子数,物质的量,和摩尔质量各是多少?2 2020-06-08 …
为了研究物质的某种特性,某同学分别测量了一些物体的质量和体积,记录数据如下表所示: 2020-06-27 …
由51个氨基酸形成某蛋白质的过程中共脱水48个,则形成的肽键数目、该蛋白质含多肽链的条数、该蛋白质 2020-07-17 …
“碳12”是指原子核内有6个质子6个中子,那“氦3”指的是氦原子核内有()A.1个质子2个中子B. 2020-07-29 …