设NA为阿伏加德罗常数的值,下列说法正确的是()A.标准状况下,5.6LO2作氧化剂时转移电子数一定为NAB.用惰性电极电解CuSO4溶液后,如果加入0.1molCu(OH)2能使溶液复原,则电路中
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,5.6L O2作氧化剂时转移电子数一定为NA
B. 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA
C. 已知3BrF3+5H2O═HBrO3+Br2+9HF+O2↑如果有5molH2O参加氧化还原反应,则由水还原的BrF3分子数目为3NA
D. 142gNa2SO4和Na2HPO4固体混合物中,阴阳离子总数为3NA
| 5.6L |
| 22.4L/mol |
B.加入0.1 mol Cu(OH)2后恰好恢复到电解前的浓度和pH,Cu(OH)2从组成上可看成CuO•H2O,根据“析出什么加入什么”的原则知,析出的物质是氧化铜和水,则阴极上析出氢气和铜,生成0.1mol铜转移电子=0.1mol×2mol=0.2mol,根据原子守恒知,生成0.1mol水需要0.1mol氢气,生成0.1mol氢气转移电子=0.1mol×2mol=0.2mol,所以电解过程中共转移电子数为0.4mol,故B错误;
C.根据反应
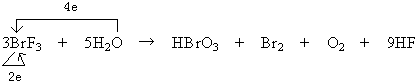 ,当有5mol水参加反应时,水中氧元素失去电子是4mol,反应一共转移电子是6mol,由水还原的BrF3的物质的量为:2mol×
,当有5mol水参加反应时,水中氧元素失去电子是4mol,反应一共转移电子是6mol,由水还原的BrF3的物质的量为:2mol×| 0.4mol |
| 0.6mol |
| 4 |
| 3 |
D.Na2SO4和Na2HPO4的摩尔质量都是142g/mol,142g Na2SO4和Na2HPO4固体混合物的物质的量为1mol,1mol该混合物中含有2mol钠离子、1mol硫酸根离子和硫酸氢根离子,总共含有3mol阴阳离子,含有阴阳离子总数为3NA,故D正确;
故选D.
课本上液体压强公式是假设液面下有一高度为h、截面积为S的圆柱形的液柱为例推导的,如果将该圆柱形液柱 2020-05-13 …
文斗乡贺家湾正在建设液化气站,估计2016年底文斗集镇基本上可使用液化然气.用燃气灶烧水时,把2. 2020-05-13 …
下列实验操作正确的是A.中和滴定实验时,滴定管用蒸馏水洗净后即可盛装标准液进行滴定B.为了测定某溶 2020-05-13 …
平面直角坐标系中,正方形ABCD四个顶点的坐标分别为(-1,-1)(1,-1)(1,1)(-1,1 2020-05-16 …
以下关于系统目标分析的描述中,不正确的是A.目标设定的标准应该是可度量的B.目标设定的标准应该 2020-05-23 …
以下关于系统目标分析的描述中,正确的是A.目标设定的标准应该是可度量的B.目标设定的标准应该符 2020-05-24 …
新农村建设中正大力推广使用瓶装液化气.如果每瓶中装入12kg液化气,液化气的热值取4.2×107J 2020-06-12 …
新农村建设中正在大力推广使用瓶装液化气.如果每瓶装10kg液化气,液化气的热值取4.2×107J/ 2020-06-12 …
实验室可以用KMnO4标准液滴定草酸(H2C2O4),测定溶液中草酸的浓度.判断下列说法不正确的是 2020-07-21 …
半理解半化学的题目配置一定物质的量浓度的硫酸溶液最后在容量瓶中加水稀释标线,塞好塞子摇动倒转混匀后 2020-07-26 …