早教吧作业答案频道 -->化学-->
磷化铝、磷化锌、磷化钙是目前常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦(PH3),PH3具有较强的还原性,能在空气中自燃.卫生安全标准规定,粮食中磷化物(以PH3计)含量≤0
题目详情
磷化铝、磷化锌、磷化钙是目前常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦(PH3),PH3具有较强的还原性,能在空气中自燃.卫生安全标准规定,粮食中磷化物(以PH3计)含量≤0.05mg/kg.某化学兴趣小组的同学通过下列方法对粮食中残留磷化物含量进行研究:
【操作流程】安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸标准溶液滴定
【实验装置】
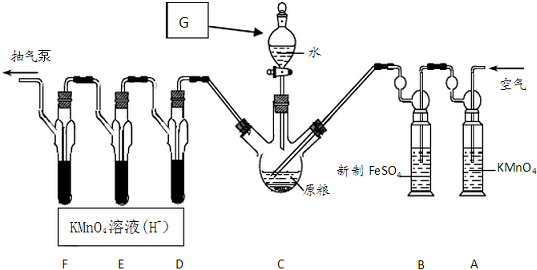
C中盛有200g原粮;D、E、F 各盛装1.00mL浓度为1.00×10-3mol/L的KMnO4溶液(H2SO4酸化).
请回答下列有关问题:
(1)仪器G的名称是___,以磷化铝为例,写出磷化物与水反应的化学方程式___.
(2)检查C装置气密性的方法是:用止水夹夹紧C装置___,取下上口活塞,漏斗中加入水,打开下口旋塞,观察到___,表明装置气密性良好.
(3)实验过程中,用抽气泵反复抽气的目的是___.
(4)A中盛装KMnO4溶液是为除去空气中可能含有的___(填“还原”或“氧化”)性气体; B中盛装新制FeSO4溶液的作用是___;
(5)已知D、E、F中发生同一反应,实验中PH3被氧化成磷酸,写出所发生的化学反应方程式:___;
收集装置D、E、F所得吸收液,并洗涤D、E、F,将吸收液、洗涤液一并置于锥形瓶中,加水稀释至25mL,用浓度为5×10-4mol/LNa2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为___mg/kg.
【操作流程】安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸标准溶液滴定
【实验装置】

C中盛有200g原粮;D、E、F 各盛装1.00mL浓度为1.00×10-3mol/L的KMnO4溶液(H2SO4酸化).
请回答下列有关问题:
(1)仪器G的名称是___,以磷化铝为例,写出磷化物与水反应的化学方程式___.
(2)检查C装置气密性的方法是:用止水夹夹紧C装置___,取下上口活塞,漏斗中加入水,打开下口旋塞,观察到___,表明装置气密性良好.
(3)实验过程中,用抽气泵反复抽气的目的是___.
(4)A中盛装KMnO4溶液是为除去空气中可能含有的___(填“还原”或“氧化”)性气体; B中盛装新制FeSO4溶液的作用是___;
(5)已知D、E、F中发生同一反应,实验中PH3被氧化成磷酸,写出所发生的化学反应方程式:___;
收集装置D、E、F所得吸收液,并洗涤D、E、F,将吸收液、洗涤液一并置于锥形瓶中,加水稀释至25mL,用浓度为5×10-4mol/LNa2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为___mg/kg.
▼优质解答
答案和解析
(1)仪器G的名称是分液漏斗,依据题干信息,磷化铝和水反应,水解生成PH3和氢氧化铝,反应的化学方程式为:AlP+3H2O=Al(OH)3↓+PH3↑,
故答案为:分液漏斗;AlP+3H2O=Al(OH)3↓+PH3↑;
(2)利用装置特征,结合气体压强变化,用止水夹夹紧C装置,用止水夹夹紧C装置左右两端的橡皮管,取下上口活塞,漏斗中加入水,打开下口旋塞,观察到水开始下滴一段时间后,不再连续下滴,证明气密性完好;
故答案为:左右两端的橡皮管;水开始下滴一段时间后,不再连续下滴;
(3)准确测定PH3的含量,需要用高锰酸钾溶液全部吸收,避免产生较大误差,所以抽气泵是保证PH3全部被吸收的措施;
故答案为:保证生成的PH3全部被酸性KMnO4溶液吸收;
(4)依据装置图中装置中的试剂选择分析判断,高锰酸钾溶液是强氧化剂可以吸收空气中的还原性气体;焦性没食子酸先和碱反应,再和氧气反应可以吸收氧气;若不吸收氧气,PH3会在氧气中燃烧,用滴定方法测定的PH3减小,结果偏低;
故答案为:还原;除去空气中的O2;
(5)加水稀释至25mL,用浓度为5×10-4mol/L Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL;依据滴定反应:2KMnO4+5Na2SO3+3H2SO4=2MnSO4+K2SO4+5Na2SO4+3H2O;2KMnO4~5Na2SO3;未反应的高锰酸钾物质的量=0.0110L×5×10-4mol/L×
=2.2×10-6mol;与PH3反应的高锰酸钾物质的量=1.00×10-3mol/L×0.0030L-2.2×10-6mol=8.0×10-7mol;根据反应 5PH3+8KMnO4+12H2SO4=5H3PO4+8MnSO4+4K2SO4+12H2O;得到定量关系为:5PH3~8KMnO4;计算得到PH3物质的量=8.0×10-7mol×
=5.0×10-7mol;则PH3的质量分数=
=0.085g/kg;
故答案为:5PH3+8KMnO4+12H2SO4=5H3PO4+8MnSO4+4K2SO4+12H2O;0.085.
故答案为:分液漏斗;AlP+3H2O=Al(OH)3↓+PH3↑;
(2)利用装置特征,结合气体压强变化,用止水夹夹紧C装置,用止水夹夹紧C装置左右两端的橡皮管,取下上口活塞,漏斗中加入水,打开下口旋塞,观察到水开始下滴一段时间后,不再连续下滴,证明气密性完好;
故答案为:左右两端的橡皮管;水开始下滴一段时间后,不再连续下滴;
(3)准确测定PH3的含量,需要用高锰酸钾溶液全部吸收,避免产生较大误差,所以抽气泵是保证PH3全部被吸收的措施;
故答案为:保证生成的PH3全部被酸性KMnO4溶液吸收;
(4)依据装置图中装置中的试剂选择分析判断,高锰酸钾溶液是强氧化剂可以吸收空气中的还原性气体;焦性没食子酸先和碱反应,再和氧气反应可以吸收氧气;若不吸收氧气,PH3会在氧气中燃烧,用滴定方法测定的PH3减小,结果偏低;
故答案为:还原;除去空气中的O2;
(5)加水稀释至25mL,用浓度为5×10-4mol/L Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL;依据滴定反应:2KMnO4+5Na2SO3+3H2SO4=2MnSO4+K2SO4+5Na2SO4+3H2O;2KMnO4~5Na2SO3;未反应的高锰酸钾物质的量=0.0110L×5×10-4mol/L×
| 2 |
| 5 |
| 5 |
| 8 |
| 5.0×10-7mol×34g/mol |
| 0.2kg |
故答案为:5PH3+8KMnO4+12H2SO4=5H3PO4+8MnSO4+4K2SO4+12H2O;0.085.
看了磷化铝、磷化锌、磷化钙是目前常...的网友还看了以下:
按要求写出化学反应的文字或符号表达式:红磷在空气中燃烧:磷+氧气点燃五氧化二磷(化学方程式为:4P 2020-04-11 …
书写下列反应的文字表达式(或用化学式表示反应):(1)磷在空气中燃烧磷+氧气点燃五氧化二磷(化学方 2020-04-11 …
同学们为验证空气中氧气的体积分数,进行实验(如图所示).请回答:(1)小红点燃红磷,观察到红磷燃烧 2020-04-11 …
用文字或化学式表示下列符合要求的反应式,并指出反应的基本类型(“化合”或“分解”):(1)磷在氧气 2020-04-11 …
白磷是一种蜡状固体,不溶于水,把白磷隔绝空气加热,变成红磷,白磷在空气中,即使在常温下,也会跟氧气 2020-04-26 …
无磷化液膜或磷化膜不易形成工件整体或局部无磷化膜,有时发蓝或有空白片(1)工件表面有硬化层,怎么解 2020-05-17 …
下列关于酶的磷酸化叙述错误的是A、磷酸化和去磷酸化都是酶促反应B、磷酸化或去磷酸化可伴有亚基下列关 2020-06-20 …
白磷(P4)是磷的单质之一,易氧化,与卤素单质反应生成卤化磷.卤化磷通常有三卤化磷或五卤化磷,五卤 2020-06-28 …
白磷(P4)是磷的单质之一,易氧化,与卤素单质反应生成卤化磷.卤化磷通常有三卤化磷或五卤化磷,五卤 2020-06-28 …
如图装置(燃烧匙中盛放的是红磷在钟罩中燃烧)可用于测定空气中氧气的含量,将红磷点燃后迅速塞好橡皮塞. 2020-12-21 …